
né do obehu.
1 x 10 ml Liprolog injekčná liekovka.
2 x 10 ml Liprolog injekčná liekovka.
5 x (1 x 10 ml) Liprolog injekčná liekovka.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnýminárodnými požiadavkami.
Návod na použitie
Injekčnú liekovku používajte s vhodnou injekčnou striekačkou označenou 100 U.
a) Príprava dávky
Skontrolujte roztok Liprologu. Má byť číry a bezfarebný. Nepoužívajte Liprolog, pokiaľ sa javí
zakalený, hustý alebo ľahko zafarbený alebo pokiaľ sú v ňom viditeľné pevné častice.
i) Liprolog
1. Umyte si ruky.
2. Ak používate novú injekčnú liekovku, odstráňte ochranný plastový kryt, ale neodstraňujte
zátku.
3. Ak liečebný režim vyžaduje podanie bazálneho inzulínu a Liprologu v tom istom čase, tieto dva inzulíny sa môžu miešať v injekčnej striekačke. Pokiaľ inzulíny miešate, sledujte inštrukcie pre miešanie, ktoré sú uvedené v časti (ii) a 6.2.
4. Do injekčnej striekačky natiahnite množstvo vzduchu totožné s množstvom predpísanej dávky Liprologu, ktoré budete aplikovať. Uzáver injekčnej liekovky potrite alkoholovým tampónom. Ihlu vbodnite do gumenej zátky injekčnej liekovky Liprologu a vzduch z injekčnej striekačky vtlačte do injekčnej liekovky.
5. Injekčnú liekovku s injekčnou striekačkou otočte dnom nahor. Držte injekčnú liekovku
a injekčnú striekačku pevne v jednej ruke.
6. Presvedčte sa, že je špička ihly v Liprologu a potrebnú dávku natiahnite do injekčnej striekačky.
7. Pred vytiahnutím ihly z injekčnej liekovky skontrolujte, či nie sú v injekčnej striekačke vzduchové bubliny, ktoré znižujú množstvo Liprologu v injekčnej striekačke. V prípade ich výskytu držte injekčnú striekačku smerom hore a poklepkávajte na jej stenu, pokiaľ všetky bubliny nevyplávajú nahor. Vytlačte ich z injekčnej striekačky von a natiahnite presnú dávku.
8. Vytiahnite ihlu z injekčnej liekovky a položte injekčnú striekačku tak, aby sa ihla ničoho
nedotýkala.
ii) Miešanie Liprologu s dlhšie pôsobiacimi ľudskými inzulínmi (pozričasť 6.2)
1. Liprolog sa smie miešať s dlhšie pôsobiacimi ľudskými inzulínmi len na odporúčanie lekára.
2. Do injekčnej striekačky natiahnite množstvo vzduchu zodpovedajúce dávke dlhšie pôsobiaceho inzulínu. Vbodnite ihlu do injekčnej liekovky s dlhšie pôsobiacim inzulínom a vtlačte vzduch dovnútra. Ihlu vytiahnite von.
3. Teraz rovnakým spôsobom injikujte vzduch do injekčnej liekovky s Liprologom, ale
nevyťahujte ihlu.
4. Otočte injekčnú liekovku i s injekčnou striekačkou dnom nahor.
5. Uistite sa, že špička ihly je v Liprologu a natiahnite správnu dávku Liprologu do injekčnej striekačky.
6. Pred vytiahnutím ihly z injekčnej liekovky skontrolujte, či nie sú v injekčnej striekačke vzduchové bubliny, ktoré znižujú množstvo Liprologu v injekčnej striekačke. V prípade ich výskytu držte injekčnú striekačku nahor a poklepkávajte na jej stenu, pokiaľ všetky bubliny nevyplávajú nahor. Vytlačte ich z injekčnej striekačky von a natiahnite presnú dávku.
7. Vytiahnite ihlu z injekčnej liekovky s Liprologom a vbodnite ju do injekčnej liekovky s dlhšie pôsobiacim inzulínom. Otočte injekčnú liekovku s injekčnou striekačkou dnom nahor. Injekčnú liekovku i injekčnú striekačku držte pevne v jednej ruke a ľahko nimi potraste. Uistite sa, že špička ihly je ponorená v inzulíne a potom natiahnite dávku dlhšie pôsobiaceho inzulínu.
8. Vytiahnite ihlu z injekčnej liekovky a položte injekčnú striekačku tak, aby sa ihla ničoho
nedotýkala.
b) Aplikácia dávky
1. Vyberte miesto vpichu.
2. Očistite kožu podľa inštrukcie.
3. Stabilizujte kožu tak, že ju buď napnete alebo vytvoríte väčšiu kožnú riasu. Ihlu vbodnite
a aplikujte podľa inštrukcie.
4. Vytiahnite ihlu a na miesto vpichu niekoľko sekúnd jemne tlačte. Miesto nemasírujte.
5. Ihlu a injekčnú striekačku bezpečne znehodnoťte.
6. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužívalo
v priemere viackrát ako raz za mesiac.
c) Miešanie inzulínov
Nemiešajte inzulín v injekčných liekovkách s inzulínom v náplniach. Pozri časť 6.2.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Eli Lilly Nederland B.V, Grootslag 1-5, 3991 RA Houten, Holandsko
8. REGISTRAČNÉ ČÍSLA
EU/1/01/195/001 1 x 10 ml Liprolog injekčná liekovka EU/1/01/195/008 2 x 10 ml Liprolog injekčné liekovky EU/1/01/195/009 5 x (1 x 10 ml) Liprolog injekčné liekovky
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 1. augusta 2001
Dátum posledného predĺženia: 1. augusta 2006
10. DÁTUM REVÍZIE TEXTU
1. NÁZOV LIEKU
Liprolog 100 U/ml, injekčný roztok v náplni
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
2.1 Všeobecný opis
Liprolog je sterilný, číry, bezfarebný vodný roztok.
2.2 Kvalitatívne a kvantitatívne zloženie
1 ml obsahuje 100 U (zodpovedá 3,5 mg) inzulínu lispro (pôvod z rekombinantnej DNA
produkovanej E.coli). Každá náplň obsahuje 3 ml, čo zodpovedá 300 U inzulínu lispro.
Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčný roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Na liečbu dospelých a detí s diabetes mellitus, ktorí potrebujú inzulín na udržanie normálnej glukózovej homeostázy. Rovnako sa Liprolog indikuje na iniciálnu stabilizáciu diabetes mellitus.
4.2 Dávkovanie a spôsob podávania
Dávkovanie stanoví lekár v súlade s potrebami pacienta.
Liprolog sa môže aplikovať krátko pred jedlom. Ak je to potrebné, Liprolog možno podať krátko po jedle. Liprolog sa má aplikovať subkutánnou injekciou alebo kontinuálnou subkutánnou infúziou pomocou pumpy (pozri časť 4.2), avšak môže sa, aj keď sa to neodporúča, podať intramuskulárne.
V prípade potreby môže byť Liprolog podaný aj intravenózne, napr. ak je potrebné kontrolovať
glykémiu počas ketoacidózy, akútneho ochorenia alebo v priebehu operácie a pooperačného stavu.
Miesta subkutánneho podania majú byť horná časť ramien, stehno, zadok alebo brucho. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužilo viackrát ako približne raz za mesiac.
Pri subkutánnej aplikácii Liprologu je potrebné sa dôkladne uistiť o tom, že nedošlo k aplikácii
do cievy. Po aplikácii sa miesto vpichu nemá masírovať. Pacient musí byť riadne poučený o správnej
aplikačnej technike.
Liprolog účinkuje po subkutánnom podaní rýchlo a kratšiu dobu (2 -5 hodín) v porovnaní s regular inzulínom. Tento rýchly nástup účinku dovoľuje podávanie injekcie Liprologu (alebo bolusu Liprologu v prípade kontinuálnej subkutánnej infúzie) veľmi krátko pred jedlom alebo po jedle. Časový priebeh aktivity akéhokoľvek inzulínu sa môže významne líšiť u rôznych osôb alebo u jednej osoby v rôznych časových intervaloch. Nástup účinku inzulínu lispro je v porovnaní s rozpustným ľudským inzulínom rýchlejší nezávisle na mieste vpichu. Rovnako ako u všetkých inzulínových prípravkov závisí trvanie účinku Liprologu na dávke, mieste vpichu, krvnom zásobovaní, teplote
a fyzickej aktivite.
Liprolog môže byť podľa rady lekára aplikovaný v kombinácii s dlhšie pôsobiacim inzulínom alebo s derivátmi sulfonylurey podaných perorálne.
Použitie Liprologu v inzulínových infúznych pumpách
Na infúzie inzulínu lispro sa môžu použiť inzulínové infúzne pumpy označené CE. Pred aplikáciou
infúzie inzulínu lispro si preštudujte inštrukcie výrobcu, aby sa zistila vhodnosť alebo iné parametre pre konkrétnu pumpu. Prečítajte si priložený návod na použitie infúznej pumpy a podľa neho postupujte. Spolu s pumpou používajte správny zásobník a katéter. Infúzny set (hadička a kanyla) sa má meniť podľa pokynov, ktoré sú súčasťou infúzneho setu. Pri zavádzaní infúzie pracujte za sterilných podmienok. V prípade hypoglykémie sa musí infúzia prerušiť až do jej odoznenia. Ak si nameriate výrazne nízke alebo opakovane nízke hladiny glukózy v krvi, upozornite svojho lekára
a zvážte, či nie je potrebné infúziu spomaliť alebo zastaviť. Porucha pumpy alebo upchatie infúzneho setu môže spôsobiť náhly vzostup hladiny glukózy. V prípade podozrenia na porušenie prietoku inzulínu riaďte sa pokynmi v návode na obsluhu, prípadne upovedomte svojho lekára. Pri používaní infúznej pumpy sa nemá Liprolog miešať s inými inzulínmi.
Intravenózna aplikácia inzulínu
Intravenózna aplikácia inzulínu lispro má byť vykonávaná podľa bežnej klinickej praxe pre
intravenózne podávanie, napr. intravenóznym bolusom alebo infúziou. Je nutná častá kontrola hladiny
glukózy v krvi.
Infúzny roztok s koncentráciou od 0,1 U/ml do1,0 U/ml inzulínu lispro v 0,9% NaCl alebo
5% sacharóze je stabilný pri izbovej teplote po dobu 48 hodín. Pred zahájením infúzie sa odporúča
infúznu súpravu prestrieknuť.
4.3 Kontraindikácie
Precitlivenosť na inzulín lispro alebo na ktorúkoľvek z pomocných látok. Hypoglykémia.
4.4 Osobitné upozornenia a opatrenia pri používaní
Prechod pacienta na iný typ alebo značku inzulínu sa musí uskutočniť pod prísnym lekárskym dohľadom. Zmeny koncentrácie, značky (výrobcu), typu (regular, NPH, lente a i.), druhu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo spôsobu výroby (rekombinantná DNA oproti inzulínu zvieracieho pôvodu) môžu mať za následok potrebu zmeny dávkovania. Každý pacient, ktorý užíva popri rýchlopôsobiacom aj bazálny inzulín, musí optimalizovať dávkovanie oboch inzulínov
k dosiahnutiu kontroly glykémie po celý deň, hlavne kontroly glykémie v noci/nalačno.
Dlhotrvajúci diabetes, intenzifikovaná inzulínová terapia, diabetická neuropatia alebo užívanie liekov, ako sú beta-blokátory, môžu zmeniť alebo zmierniť skoré varovné príznaky hypoglykémie.
Malý počet pacientov, ktorí mali hypoglykemické reakcie po prechode z inzulínu zvieracieho pôvodu na ľudský inzulín, uvádzalo, že skoré varovné príznaky hypoglykémie boli menej výrazné alebo odlišné od tých, ktoré zažili pri použití predchádzajúceho inzulínu. Nekontrolované hypoglykemické alebo hyperglykemické reakcie môžu spôsobiť stratu vedomia, kómu alebo smrť.
Použitie neadekvátnych dávok alebo prerušenie liečby, najmä u inzulín-dependentných diabetikov,
môže viesť k hyperglykémii a diabetickej ketoacidóze, ktoré sú potenciálne letálne.
Potreba inzulínu môže byť znížená pri poškodení funkcie obličiek.
Potreba inzulínu môže byť znížená u pacientov s poškodením funkcie pečene z dôvodu nižšej kapacity pre glukoneogenézu a zhoršeného odbúravania inzulínu. Avšak u pacientov s chronickým
poškodením funkcie pečene môže zvýšenie inzulínovej rezistencie viesť k vyššej potrebe inzulínu.
Potreba inzulínu sa môže zvýšiť počas choroby alebo pri emocionálnom rozrušení.
Úprava dávky môže byť tiež potrebná, pokiaľ pacienti vykonávajú zvýšenú fyzickú aktivitu alebo menia svoju zvyčajnú diétu. Cvičenie ihneď po požití potravy môže zvýšiť riziko hypoglykémie. Dôsledok farmakodynamiky rýchlopôsobiaceho analógu ľudského inzulínu je výskyt hypoglykémie, pri porovnaní s rozpustným ľudským inzulínom, sa po injekcii môže vyskytnúť skôr.
Ak je predpísaná sila 40 U/ml v injekčnej liekovke, neaplikujte inzulín z náplne 100 U/ml pomocou
injekčnej striekačky 40 U/ml.
Podanie Liprologu deťom má byť zvážené iba v prípade očakávaného prínosu v porovnaní
s rozpustným inzulínom, napr. v súvislosti so zmeneným časovým odstupom aplikácie vzhľadom na
podanie jedla.
Kombinácia Liprologu a pioglitazónu
V prípadoch, keď sa použil pioglitazón v kombinácii s inzulínom, boli zaznamenané prípady srdcového zlyhania, najmä u pacientov s rizikovými faktormi pre vznik srdcového zlyhania. Treba mať na zreteli tieto fakty v prípade, že sa zvažuje liečba kombináciou pioglitazónu a Liprologu. Ak
pacient používa danú kombináciu, je u neho potrebné sledovať znaky a symptómy srdcového zlyhania, priberanie na hmotnosti a edém. Ak sa zistí akékoľvek zhoršenie srdcových symptómov, pioglitazón
sa musí prestať podávať.
4.5 Liekové a iné interakcie
Potreba inzulínu sa môže zvýšiť liekmi s hyperglykemickým účinkom, ako je perorálna antikoncepcia, kortikosteroidy alebo hormonálna substitučná terapia pri liečbe porúch štítnej žľazy, danazol, beta2-mimetiká (ritodrín, salbutamol, terbutalín).
Potreba inzulínu sa môže znížiť pri podávaní liekov s hypoglykemickým účinkom, ako sú perorálne antidiabetiká, salicyláty (napríklad kyselina acetylosalicylová), sulfónamidy, niektoré antidepresíva (inhibítory monoaminooxidázy, selektívne inhibítory spätného vychytávania sérotonínu), niektoré inhibítory angiotenzín konvertujúceho enzýmu (kaptopril, enalapril), blokátory receptorov angiotenzínu II, beta-blokátory, oktreotid alebo alkohol.
Používanie iných liekov podávaných súčasne s Liprologom sa musí konzultovať s lekárom (pozri časť
4.4).
4.6 Fertilita, gravidita a laktácia
Údaje o veľkom počte gravidných žien užívajúcich inzulín lispro nepreukázali žiadne nežiaduce
účinky na graviditu alebo na zdravie plodu/novorodenca.
Udržanie dobrej kontroly glykémie počas gravidity je základnou požiadavkou liečby diabetu
u pacientky liečenej inzulínom pri inzulín-dependentnom alebo gestačnom diabete. Potreba inzulínu sa obvykle znižuje počas prvého trimestra a zvyšuje počas druhého a tretieho trimestra. Pacientky
s diabetom majú byť poučené o tom, aby informovali svojho lekára v prípade gravidity alebo pokiaľ graviditu zvažujú. Starostlivé monitorovanie glykémie, rovnako ako aj celkového zdravotného stavu, je základnou požiadavkou u gravidných s diabetom.
Dojčiace diabetičky môžu potrebovať úpravu dávky inzulínu, diéty alebo oboje.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta koncentrovať sa a reagovať môže byť porušená v dôsledku hypoglykémie. To môže byť riskantné v situáciách špeciálne vyžadujúcich vyššie uvedené schopnosti (napr. vedenie auta alebo obsluha strojov).
Pacient má byť poučený o nutnosti zabrániť hypoglykémii počas vedenia vozidla, čo je obzvlášť dôležité u tých osôb, ktoré majú zníženú alebo chýbajúcu vnímavosť varovných príznakov hypoglykémie alebo majú časté hypoglykemické epizódy. Za týchto okolností sa má starostlivo zvážiť vhodnosť vedenia vozidiel.
4.8 Nežiaduce účinkyNajčastejším nežiaducim účinkom inzulínovej terapie u pacienta s diabetom je hypoglykémia. Závažná hypoglykémia môže viesť ku strate vedomia a v extrémnych prípadoch ku smrti. Frekvencia výskytu hypoglykémie nie je uvedená, pretože hypoglykémia je výsledkom pôsobenia nielen dávky inzulínu ale aj iných faktorov, napr. diéta pacienta a fyzická aktivita.
Často (1/100 až <1/10) sa u pacientov objavuje lokálna precitlivenosť. V mieste aplikácie inzulínu sa môže vyskytnúť začervenanie, opuch a svrbenie. Tento stav obvykle ustúpi počas niekoľkých dní alebo týždňov. V niektorých prípadoch môže byť tento stav zapríčinený inými faktormi ako inzulínom, napríklad iritáciou kože dezinfekčným prostriedkom alebo nesprávnou injekčnou technikou. Systémová alergia, ktorá je zriedkavá (1/10 000 až <1/1 000), ale potenciálne závažnejšia,
je generalizovanou alergiou na inzulín. Môže spôsobiť vyrážky po celom tele, dýchavičnosť, pískanie, pokles krvného tlaku, zrýchlený pulz alebo potenie. Ťažké stavy generalizovanej alergie môžu ohrozovať život.
Lipodystrofia v mieste aplikácie injekcie je menej častá (1/1 000 až <1/100).
Prípady edémov počas inzulínovej liečby boli hlásené najmä vtedy, keď v dôsledku intenzívnejšej inzulinoterapie došlo k zlepšeniu predchádzajúcej zlej metabolickej kompenzácie.
Hlásenie podozrení na nežiaduce reakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.4.9 PredávkovanieInzulín nemá špecifickú definíciu predávkovania, pretože sérová hladina krvného cukru je výsledkom komplexných interakcií medzi hladinou inzulínu, dostupnosťou glukózy a ostatnými metabolickými procesmi. Hypoglykémia sa môže objaviť ako dôsledok nadbytku inzulínu v pomere k príjmu potravy a výdaju energie.
Hypoglykémia môže byť spojená s ľahostajnosťou, zmätenosťou, palpitáciami, bolesťami hlavy,
potením a vracaním.
Mierne epizódy hypoglykémie reagujú na perorálne podanie glukózy alebo iného cukru, prípadne produktu obsahujúceho sacharidy.
Korekcia stredne ťažkej hypoglykémie sa môže uskutočniť intramuskulárnou alebo subkutánnou aplikáciou glukagónu a následným perorálnym podaním uhľohydrátov, pokiaľ sa pacient dostatočne zotaví. Pacienti, ktorí nereagujú na glukagón, musia dostať infúziu glukózy intravenózne.
Pokiaľ je pacient v kóme, glukagón sa má aplikovať intramuskulárne alebo subkutánne. Pokiaľ však glukagón nie je k dispozícii alebo pacient na jeho podanie nereaguje, musí sa podať roztok glukózy intravenózne. Akonáhle sa pacient preberie z bezvedomia, musí sa najesť.
Po zdanlivej úprave klinického stavu môže byť potrebný trvalý príjem sacharidov a sledovanie
pacienta, pretože hypoglykémia sa môže opakovať.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Inzulíny a ich analógy, rýchlopôsobiace inzulíny, ATC kód: A10A B04.
Primárnym účinkom inzulínu lispro je regulácia glukózového metabolizmu.
Navyše má inzulín ďalšie anabolické a antikatabolické účinky na mnoho rôznych tkanív. V svalovom tkanive tieto účinky zahŕňajú zvýšenie syntézy glykogénu, mastných kyselín, glycerolu a proteínov
a vychytávanie aminokyselín a zároveň zníženie glykogenolýzy, glukoneogenézy, ketogenézy,
lipolýzy, proteínového katabolizmu a tvorby aminokyselín.
Inzulín lispro má rýchly nástup účinku (približne 15 minút), čo umožňuje jeho podanie krátko pred alebo po jedle (interval od 0 do 15 minút), v porovnaní s bežným rýchlopôsobiacim inzulínom (aplikácia 30 až 45 minút pred jedlom). Nástup účinku inzulínu lispro je rýchly a trvanie aktivity kratšie (2 až 5 hodín) v porovnaní s regular inzulínom.
Klinické štúdie u pacientov s diabetom typu 1 alebo 2 preukázali nižší výskyt postprandiálnej hyperglykémie u inzulínu lispro v porovnaní s rozpustným ľudským inzulínom.
Rovnako ako u všetkých inzulínových prípravkov môže byť časový priebeh účinku inzulínu lispro odlišný u rôznych jedincov alebo odlišný v rôznych časových intervaloch u rovnakého jedinca
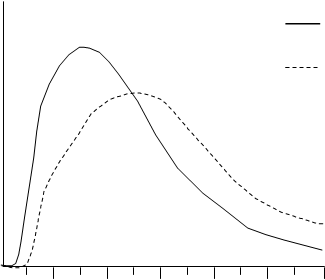
v závislosti na dávke, mieste injekcie, krvnom zásobení, teplote a fyzickej aktivite. Typický priebeh aktivity v čase po subkutánnej injekcii ilustruje nasledujúci graf.
Insulin
Lispro
Hypoglycaemic
Activity
Humulin R
0 1 2
3 4 5 6
Time (Hours)
Graf zobrazuje relatívne množstvo glukózy v závislosti na čase potrebné na udržanie celkovej
plazmatickej glukózovej koncentrácie testovaného jedinca blízko hladinám nalačno a je indikátorom efektu týchto inzulínov na glukózový metabolizmus v závislosti na čase.
Uskutočnili sa klinické štúdie u detí (61 pacientov vo veku 2 až 11 rokov) a u detí a mladistvých (481 pacientov vo veku 9 až 19 rokov) porovnávajúce inzulín lispro a ľudský rozpustný inzulín. Farmakodynamický profil inzulínu lispro u detí je podobný ako farmakodynamický profil pozorovaný u dospelých.
Liečba s inzulínom lispro preukázala nižšie hladiny glykovaného hemoglobínu pri porovnaní s rozpustným inzulínom, pri použití subkutánnou infúznou pumpou. V dvojito zaslepenej skríženej štúdii došlo ku zníženiu hladiny glykovaného hemoglobínu po 12 týždňoch o 0,37 percentuálnych bodov u inzulínu lispro v porovnaní s 0,03 percentuálnymi bodmi u rozpustného inzulínu (p=0,004).
Štúdie ukázali, že pridanie inzulínu lispro signifikantne znižuje hladinu HbA1C v porovnaní
so samotnou sulfonylureou u pacientov s diabetom typu 2 na maximálnych dávkach derivátov
sulfonylurey. Zníženie hladiny HbA1C možno očakávať takisto pri kombinácii s inými prípravkami inzulínu, napr. regular alebo izofán inzulínom.
Klinické štúdie s pacientami s diabetom typu 1 a 2 preukázali nižší počet nočných hypoglykémií
s inzulínom lispro v porovnaní s rozpustným ľudským inzulínom. V niektorých štúdiách bol nižší
počet nočných hypoglykémií spojený so zvýšeným počtom denných hypoglykémií.
Glukodynamická odpoveď na inzulín lispro nie je ovplyvnená poškodením funkcie obličiek alebo pečene. Glukodynamické rozdiely medzi inzulínom lispro a rozpustným ľudským inzulínom merané v priebehu glukózového clampu boli udržané v širokom spektre renálnych funkcií.
Bolo preukázané, že inzulín lispro je molárne ekvipotentný s ľudským inzulínom, ale jeho účinok
nastupuje rýchlejšie a má kratšiu dobu trvania.
5.2 Farmakokinetické vlastnosti
Farmakokinetika inzulínu lispro zodpovedá látke, ktorá sa rýchlo absorbuje a dosahuje najvyššie plazmatické hladiny v čase od 30 do 70 minút po subkutánnej injekcii. Pri zvažovaní klinickej relevancie tejto kinetiky je vhodnejšie vyšetriť krivky utilizácie glukózy (pozri 5.1).
Inzulín lispro je u pacientov s poškodením funkcie obličiek absorbovaný rýchlejšie ako rozpustný ľudský inzulín. U pacientov s diabetom typu 2 v širokom spektre renálnych funkcií boli všeobecne dodržané farmakokinetické rozdiely medzi inzulínom lispro a rozpustným inzulínom a ukázali sa nezávislými na renálnych funkciách. Inzulín lispro je u pacientov s poškodením funkcie pečene absorbovaný a eliminovaný rýchlejšie v porovnaní s rozpustným ľudským inzulínom.
5.3 Predklinické údaje o bezpečnosti
Pri testoch uskutočnených in vitro, zahŕňajúcich väzbu na inzulínové receptory a účinky na
rastúce bunky, sa inzulín lispro správal spôsobom, ktorý veľmi pripomínal ľudský inzulín. Štúdie tiež preukázali, že disociácia väzby inzulínu lispro na inzulínový receptor je totožná s ľudským inzulínom. Akútne, jeden mesiac a dvanásť mesiacov trvajúce toxikologické štúdie nepreukázali žiadne
významné toxikologické účinky.
V štúdiách na zvieratách inzulín lispro nespôsoboval poškodenie plodnosti, prejavy embryotoxicity alebo teratogenicity.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Metakrezol [3,15 mg/ml] Glycerol
Heptahydrát hydrogénfosforečnanu sodného
Oxid zinočnatý
Voda na injekciu
Kyselina chlorovodíková a hydroxid sodný môžu byť použité na úpravu pH na 7,0 - 7,8.
6.2 Inkompatibility
Prípravky Liprologu sa nesmú miešať s inzulínmi iných výrobcov alebo so zvieracími inzulínmi.
6.3 Čas použiteľnosti
Nepoužitá náplň
3 roky
Po vložení náplne do pera
28 dní
6.4 Špeciálne upozornenia na uchovávanie
Nepoužitá náplň
Uchovávajte v chladničke pri teplote (2°C – 8°C). Neuchovávajte v mrazničke. Nevystavujte
nadmernému teplu alebo priamemu slnečnému svetlu.
Po vložení náplne do pera
Uchovávajte pri teplote do 30°C. Neuchovávajte v chladničke. Pero obsahujúce náplň neuchovávajte
s nasadenou ihlou.
6.5 Druh obalu a obsah balenia a špeciálne zariadenie na použitie, podanie alebo implantáciu
Roztok sa plní do náplní z kremičitého skla typu I s butylovým alebo halobutylovým diskovým uzáverom s piestom, uzávery sú zabezpečené alumíniovým tesnením. Na ošetrenie piestu a/alebo skla náplne sa môže použiť dimetikón alebo silikónová emulzia.
Nie všetky veľkosti balenia musia byť uvedené do obehu.
5 x 3 ml Liprolog náplň pre 3 ml pero
2 x (5 x 3 ml) Liprolog náplň pre 3 ml pero
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými požiadavkami.
Návod na použitie
Liprolog náplne používajte s perom označeným CE značkou podľa odporúčania v informácii poskytovanej výrobcom pomôcky.
a) Príprava dávky
Skontrolujte Liprolog. Má byť číry a bezfarebný. Nepoužívajte Liprolog, pokiaľ sa javí zakalený,
zahustený alebo ľahko zafarbený alebo pokiaľ sú v ňom viditeľné pevné častice.
Nasleduje všeobecný popis použitia. U každého jednotlivého pera sa musia dodržovať inštrukcie
výrobcu na založenie náplne, pripojenie ihly a aplikáciu injekcie inzulínu.
b) Aplikácia dávky
1. Umyte si ruky.
2. Vyberte miesto vpichu.
3. Očistite kožu podľa inštrukcie.
4. Odstráňte vonkajší ochranný kryt ihly.
5. Stabilizujte kožu tak, že ju buď napnete alebo vytvoríte väčšiu kožnú riasu. Ihlu vbodnite podľa
inštrukcie.
6. Stlačte dávkovacie tlačidlo.
7. Vytiahnite ihlu a miesto vpichu niekoľko sekúnd jemne stlačte. Miesto nemasírujte.
8. S pomocou vonkajšieho ochranného krytu ihlu odskrutkujte a bezpečne znehodnoťte.
9. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužívalo
v priemere viackrát ako raz za mesiac.
c) Miešanie inzulínov
Nemiešajte inzulín v injekčných liekovkách s inzulínom v náplniach. Pozri časť 6.2.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Eli Lilly Nederland B.V, Grootslag 1-5, 3991 RA Houten, Holandsko
8. REGISTRAČNÉ ČÍSLA
EU/1/01/195/002 5 x 3 ml Liprolog náplne pre 3 ml pero
EU/1/01/195/010 2 x (5 x 3 ml) Liprolog náplne pre 3 ml pero
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 1. augusta 2001
Dátum posledného predĺženia: 1. augusta 2006
10. DÁTUM REVÍZIE TEXTU
1. NÁZOV LIEKU
Liprolog Mix25 100 U/ml, injekčná suspenzia v náplni
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
2.1 Všeobecný opis
Liprolog Mix25 je biela sterilná suspenzia.
2.2 Kvalitatívne a kvantitatívne zloženie
1 ml obsahuje 100 U (zodpovedá 3,5 mg) inzulín lispro (pôvod z rekombinantnej DNA
produkovanej E.coli). Každé balenie obsahuje 3ml, čo zodpovedá 300 U inzulínu lispro. Liprolog Mix25 tvorí 25% roztok inzulínu lispro a 75% suspenzia inzulínu lispro izofán. Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčná suspenzia.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Liprolog Mix25 je určený na liečbu pacientov s diabetes mellitus, ktorí potrebujú inzulín na udržanie normálnej glukózovej homeostázy.
4.2 Dávkovanie a spôsob podávania
Dávkovanie určí lekár v súlade s potrebami pacienta.
Liprolog Mix25 sa môže podať krátko pred jedlom. V prípade potreby sa Liprolog Mix25 môže podať i bezprostredne po jedle. Liprolog Mix25 sa aplikuje len subkutánnou injekciou. Liprolog Mix25 sa nemá nikdy podať intravenózne.
Subkutánne sa má podať v hornej časti ramien, na stehnách, zadku alebo bruchu. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužilo viackrát ako približne raz za mesiac.
Pri subkutánnej aplikácii Liprologu Mix25 je potrebné sa starostlivo uistiť o tom, že nedošlo
k aplikácii do cievy. Po aplikácii sa miesto vpichu nemá masírovať. Pacient musí byť riadne poučený
o správnej aplikačnej technike.
Po subkutánnej aplikácii Liprologu Mix25 dochádza k rýchlemu nástupu účinku a skorému dosiahnutiu vrcholu aktivity Liprologu. To umožňuje podanie Liprologu Mix25 v tesnej časovej súvislosti s jedlom. Trvanie účinku zložky suspenzie inzulínu lispro izofán (Basal) Liprologu Mix25 je veľmi podobné účinku bazálneho inzulínu (NPH).
Časový priebeh aktivity akéhokoľvek inzulínu sa môže významne líšiť u rôznych osôb alebo u jednej
osoby v rôznych časových intervaloch. Rovnako ako u všetkých inzulínových prípravkov závisí trvanie účinku Liprologu Mix25 na dávke, mieste vpichu, krvnom zásobovaní, teplote a fyzickej aktivite.
4.3 Kontraindikácie
Precitlivenosť na inzulín lispro alebo na ktorúkoľvek z pomocných látok. Hypoglykémia.
4.4 Osobitné upozornenia a opatrenia pri používaní
Liprolog Mix25 sa nesmie za žiadnych okolností podať intravenózne.
Prechod pacienta na iný typ alebo značku inzulínu sa musí uskutočniť pod prísnym lekárskym dohľadom. Zmeny koncentrácie, značky (výrobcu), typu (regular, NPH, lente a i.), druhu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo spôsobu výroby (rekombinantná DNA oproti inzulínu zvieracieho pôvodu) môžu mať za následok potrebu zmeny dávkovania.
Dlhotrvajúci diabetes, intenzifikovaná inzulínová terapia, diabetická neuropatia alebo užívanie liekov, ako sú beta-blokátory, môžu zmeniť alebo zmierniť skoré varovné príznaky hypoglykémie.
Malý počet pacientov, ktorí mali hypoglykemické reakcie po prevode z inzulínu zvieracieho pôvodu na ľudský inzulín, uvádzalo, že skoré varovné príznaky hypoglykémie boli menej výrazné alebo odlišné od tých, ktoré zažili pri použití predchádzajúceho inzulínu. Nekontrolované hypoglykemické alebo hyperglykemické reakcie môžu spôsobiť stratu vedomia, kómu alebo smrť.
Použitie nedostatočných dávok alebo prerušenie liečby, najmä u inzulín-dependentných diabetikov,
môže viesť k hyperglykémii a diabetickej ketoacidóze; stavom, ktoré môžu byť letálne.
Potreba inzulínu môže byť znížená pri poškodení funkcie obličiek.
Potreba inzulínu môže byť znížená u pacientov s poškodením funkcie pečene z dôvodov nižšej kapacity pre glukoneogenézu a zhoršeného odbúravania inzulínu; avšak u pacientov s chronickým poškodením funkcie pečene môže zvýšenie inzulínovej rezistencie viesť ku vyššej potrebe inzulínu.
Potreba inzulínu sa môže zvýšiť počas ochorenia alebo vplyvom emocionálnych stresov.
Úprava dávky môže byť rovnako potrebná, pokiaľ pacienti vykonávajú zvýšenú fyzickú aktivitu alebo menia svoju zvyčajnú diétu. Cvičenie ihneď po požití potravy môže zvýšiť riziko hypoglykémie.
Podanie inzulínu lispro deťom mladším ako 12 rokov sa má zvážiť iba v prípade očakávaného prínosu
v porovnaní s regular inzulínom.
Kombinácia Liprologu Mix25 a pioglitazónu
V prípadoch, keď sa použil pioglitazón v kombinácii s inzulínom, boli zaznamenané prípady srdcového zlyhania, najmä u pacientov s rizikovými faktormi pre vznik srdcového zlyhania. Treba
mať na zreteli tieto fakty v prípade, že sa zvažuje liečba kombináciou pioglitazónu a Liprologu Mix25. Ak pacient používa danú kombináciu, je u neho potrebné sledovať znaky a symptómy srdcového zlyhania, priberanie na hmotnosti a edém. Ak sa zistí akékoľvek zhoršenie srdcových symptómov, pioglitazón sa musí prestať podávať.
4.5 Liekové a iné interakcie
Potreba inzulínu sa môže zvýšiť látkami s hyperglykemickým účinkom, ako je
perorálna antikoncepcia, kortikosteroidy alebo hormonálna substitúcia počas liečby porúch štítnej žľazy, danazol, beta2-mimetiká (ritodrín, salbutamol, terbutalín).
Potreba inzulínu sa môže znížiť pri podávaní liekov s hypoglykemickým účinkom ako sú perorálne antidiabetiká, salicyláty (napr. kyselina acetylosalicylová), sulfónamidy, niektoré antidepresíva (inhibítory monoaminooxidázy, selektívne inhibítory spätného vychytávania sérotonínu), niektoré
inhibítory angiotenzín konvertujúceho enzýmu (kaptopril, enalapril), blokátory receptorov angiotenzínu II, beta-blokátory, oktreotid alebo alkohol.
Miešanie Liprologu Mix25 s inými inzulínmi sa neskúmalo.
Užívanie iných liekov podávaných súčasne s Liprologom Mix25 sa má konzultovať s lekárom (pozri
časť 4.4).
4.6 Fertilita, gravidita a laktácia
Údaje o veľkom počte gravidných žien užívajúcich inzulín lispro nepreukázali žiadne nežiaduce
účinky na graviditu alebo na zdravie plodu/novorodenca.
Udržanie dobrej kontroly glykémie počas gravidity je základnou požiadavkou liečby diabetu
u pacientky liečenej inzulínom pri inzulín-dependentnom alebo gestačnom diabete. Potreba inzulínu sa
zvyčajne znižuje počas prvého trimestra a zvyšuje počas druhého a tretieho trimestra. Pacientky s diabetom majú byť poučené o tom, aby informovali svojho lekára v prípade gravidity alebo ak graviditu zvažujú. Starostlivé monitorovanie glykémie, rovnako ako aj celkového zdravotného stavu, je základnou požiadavkou u gravidných s diabetom.
U dojčiacich diabetičiek môže vzniknúť potreba úpravy dávky inzulínu, diéty alebo oboje.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta koncentrovať sa a reagovať môže byť porušená v dôsledku hypoglykémie. To môže byť riskantné v situáciách špeciálne vyžadujúcich vyššie uvedené schopnosti (napr. vedenie auta alebo obsluha strojov).
Pacient má byť poučený o potrebe zabrániť hypoglykémii počas vedenia vozidla, čo je obzvlášť dôležité u tých osôb, ktoré majú zníženú alebo chýbajúcu vnímavosť varovných príznakov hypoglykémie alebo majú časté hypoglykemické epizódy. Za týchto okolností sa musí starostlivo zvážiť vhodnosť vedenia vozidiel.
4.8 Nežiaduce účinky
Najčastejším nežiaducim účinkom inzulínovej terapie u pacienta s diabetom je hypoglykémia. Závažná hypoglykémia môže viesť ku strate vedomia a v extrémnych prípadoch ku smrti. Frekvencia výskytu hypoglykémie nie je uvedená, pretože hypoglykémia je výsledkom pôsobenia nielen dávky inzulínu ale aj iných faktorov, napr. diéta pacienta a fyzická aktivita.
Často (1/100 až <1/10) sa u pacientov objavuje lokálna precitlivenosť. V mieste aplikácie inzulínu sa môže vyskytnúť začervenanie, opuch a svrbenie. Tento stav obvykle ustúpi počas niekoľkých dní alebo týždňov. V niektorých prípadoch môže byť tento stav zapríčinený inými faktormi ako inzulínom, napríklad iritáciou kože dezinfekčným prostriedkom alebo nesprávnou injekčnou technikou. Systémová alergia, ktorá je zriedkavá (1/10 000 až <1/1 000), ale potenciálne závažnejšia,
je generalizovanou alergiou na inzulín. Môže spôsobiť vyrážky po celom tele, dýchavičnosť, pískanie, pokles krvného tlaku, zrýchlený pulz alebo potenie. Ťažké stavy generalizovanej alergie môžu ohrozovať život.
Lipodystrofia v mieste aplikácie injekcie je menej častá (1/1 000 až <1/100).
Prípady edémov počas inzulínovej liečby boli hlásené najmä vtedy, keď v dôsledku intenzívnejšej inzulinoterapie došlo k zlepšeniu predchádzajúcej zlej metabolickej kompenzácie.
Hlásenie podozrení na nežiaduce reakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné
monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili

akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.4.9 PredávkovanieInzulín nemá špecifickú definíciu predávkovania, pretože koncentrácia glukózy v sére je výsledkom komplexných interakcií medzi hladinou inzulínu, dostupnosťou glukózy a ostatnými metabolickými procesmi. Hypoglykémia sa môže objaviť ako dôsledok nadbytku inzulínovej aktivity v pomere
k príjmu potravy a výdaju energie.
Hypoglykémia môže byť spojená s nevšímavosťou, zmätenosťou, palpitáciami, bolesťami hlavy,
potením a vracaním.
Mierne epizódy hypoglykémie reagujú na perorálne podanie glukózy, iného cukru, príp. produktu obsahujúceho sacharidy.
Korekcia stredne ťažkej hypoglykémie sa môže uskutočniť intramuskulárnou alebo subkutánnou aplikáciou glukagónu a následným perorálnym podaním sacharidov, pokiaľ sa pacient dostatočne zotaví. Pacienti, ktorí nereagujú na glukagón, musia dostať infúziu glukózy intravenózne.
Pokiaľ je pacient v kóme, glukagón sa má aplikovať intramuskulárne alebo subkutánne. Pokiaľ však glukagón nie je k dispozícii alebo pacient na jeho podanie nereaguje, musí sa podať roztok glukózy intravenózne. Akonáhle sa pacient preberie z bezvedomia, musí sa najesť.
Po zdanlivej úprave klinického stavu môže byť potrebný trvalý príjem sacharidov a sledovanie
pacienta, pretože hypoglykémia sa môže opakovať.
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Inzulíny a ich analógy, strednodobo pôsobiace v kombinácii s rýchlopôsobiacimi inzulínmi, ATC kód: A10A D04
Liprolog Mix25 je vopred namiešaná suspenzia obsahujúca inzulín lispro (rýchlopôsobiaci analóg
ľudského inzulínu) a inzulín lispro izofán (strednodobo pôsobiaci analóg ľudského inzulínu).
Primárnym účinkom inzulínu lispro je regulácia glukózového metabolizmu.
Inzulín má navyše ďalšie anabolické a anti-katabolické vlastnosti na mnoho rôznych tkanív.
V svalovom tkanive tieto účinky zahŕňajú zvýšenie syntézy glykogénu, mastných kyselín, glycerolu a proteínov a vychytávanie aminokyselín a zároveň zníženie glykogenolýzy, glukoneogenézy, ketogenézy, lipolýzy, proteínového katabolizmu a tvorby aminokyselín.
Rýchly nástup účinku inzulínu lispro (približne 15 minút) umožňuje jeho podanie v tesnej časovej
súvislosti s jedlom (v rozmedzí 0 až 15 minút pred jedlom) v porovnaní s regular inzulínom
(30 až 45 minút pred jedlom). Po subkutánnej aplikácii Liprologu Mix25 dochádza k rýchlemu nástupu účinku a skorému dosiahnutiu vrcholu aktivity inzulínu lispro. Profil účinku Liprologu Basal je veľmi podobný účinku bazálneho inzulínu (NPH) a pretrváva počas približne 15 hodín.
Klinické štúdie u pacientov s diabetom typu 1 alebo 2 preukázali nižší výskyt postprandiálnej hyperglykémie u Liprologu Mix25 v porovnaní so zmesou 30/70 ľudského inzulínu. V jednej klinickej štúdii bolo pozorované malé zvýšenie (0,38 mmol/l) hladín glukózy v noci (o 3. hodine ráno).
Na nasledujúcom obrázku je zobrazená farmakodynamika Liprologu Mix25 a Liprologu Basal.

Humalog Mix25
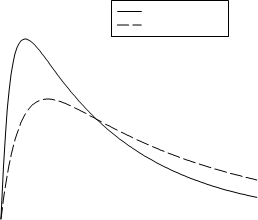
NPL
Hypoglykemická
aktivita

0 4 8 12 16 20 24
Čas, hodiny
Graf zobrazuje relatívne množstvo glukózy v závislosti na čase potrebné na udržanie celkovej plazmatickej glukózovej koncentrácie testovaného jedinca blízko hladinám nalačno a je indikátorom efektu týchto inzulínov na glukózový metabolizmus v závislosti na čase.
Glukodynamická odpoveď na inzulín lispro nie je ovplyvnená poškodením funkcie pečene alebo obličiek. Glukodynamické rozdiely medzi inzulínom lispro a rozpustným ľudským inzulínom merané v priebehu glukózového clampu boli udržané v širokom spektre renálnych funkcií.
Bolo preukázané, že inzulín lispro je molárne ekvipotentný s ľudským inzulínom, ale jeho účinok
nastupuje rýchlejšie a má kratšiu dobu trvania.
V dvoch 8-mesačných otvorených prekrížených štúdiách pacienti s diabetom 2. typu, ktorí doteraz neboli liečení inzulínom, alebo si už aplikovali inzulín jeden alebo dvakrát denne, boli v náhodnom poradí 4 mesiace liečení Liprologom Mix25 (užívaným dvakrát denne s metformínom) a inzulínom glargin (užívaným jedenkrát denne s metformínom). Detailné informácie môžete nájsť v nasledujúcej tabuľke.
| Pacienti doteraz neliečení
inzulínom n=78
| Pacienti už predtým liečení
inzulínom n=97
| Priemerná celková dávka
inzulínu pri ukončení liečby
| 0,63 U/kg
| 0,42 U/kg
| Redukcia hemoglobínu A1c1
| 1,30% (priemerná východisková hodnota = 8,7%)
| 1,00% (priemerná východisková hodnota = 8,5%)
| Redukcia priemernej
kombinovanej rannej /večernej
2 hodinovej postprandiálnej glykémie1
| 3,46 mM
| 2,48 mM
| Redukcia priemernej glykémie
nalačno1
| 0,55 mM
| 0,65 mM
| Výskyt hypoglykémií pri
ukončení liečby
| 25%
| 25%
| Hmotnostný prírastok2
| 2,33 kg
| 0,96 kg
|
|
|
1 od východiskového stavu po ukončenie liečby Liprologom Mix25
2 u pacientov randomizovaných na Liprolog Mix25 v priebehu prvej fázy prekríženej liečby
5.2 Farmakokinetické vlastnosti
Podľa farmakokinetických vlastností je inzulín lispro zlúčenina, ktorá sa rýchlo vstrebáva a dosahuje maximálne hladiny v krvi 30 až 70 minút po subkutánnom podaní. Farmakokinetika suspenzie inzulínu lispro izofán je zhodná so strednodobo pôsobiacimi inzulínmi ako je NPH. Farmakokinetika Liprologu Mix25 reprezentuje individuálne farmakokinetické vlastnosti jeho dvoch zložiek. Ak vezmeme do úvahy klinický význam týchto kinetík, je vhodnejšie vyšetriť krivky utilizácie glukózy. (pozri časť 5.1).
Inzulín lispro je u pacientov s renálnou insuficienciou absorbovaný rýchlejšie ako rozpustný ľudský inzulín. U pacientov s diabetom typu 2 v celom širokom spektre renálnych funkcií boli farmakokinetické diferencie medzi inzulínom lispro a rozpustným ľudským inzulínom všeobecne udržané a ukázali sa nezávislými na renálnych funkciách. Inzulín lispro je u pacientov s poškodenou funkciou pečene absorbovaný a eliminovaný rýchlejšie v porovnaní s rozpustným ľudským inzulínom.
5.3 Predklinické údaje o bezpečnosti
Pri testoch uskutočnených in vitro zahŕňajúcich väzbu na inzulínové receptory a účinky na rastúce bunky, sa inzulín lispro správal spôsobom, ktorý veľmi pripomínal ľudský inzulín. Štúdie tiež preukázali, že disociácia väzby inzulínu lispro na inzulínový receptor je totožná s ľudským inzulínom. Akútne, jeden mesiac a dvanásť mesiacov trvajúce toxikologické štúdie nepreukázali žiadne
významné toxikologické účinky.
V štúdiách na zvieratách inzulín lispro nespôsoboval poškodenie plodnosti, prejavy embryotoxicity alebo teratogenicity.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Protamíniumsulfát Metakrezol[1,76 mg/ml] Fenol [0,80 mg/ml] Glycerol
Heptahydrát hydrogénfosforečnanu sodného
Oxid zinočnatý
Voda na injekciu
Kyselina chlorovodíková a hydroxid sodný môžu byť použité na úpravu pH na 7,0 - 7,8.
6.2 Inkompatibility
Miešanie Liprologu Mix25 s inými inzulínmi sa neskúmalo. Pre nedostatok štúdií kompatibility
nesmie byť tento liek miešaný s inými liekmi.
6.3 Čas použiteľnosti
Nepoužitá náplň
3 roky
Po vložení náplne do pera
28 dní
6.4 Špeciálne upozornenia na uchovávanie a špeciálne zariadenie na použitie, podanie alebo implantáciu
Nepoužitá náplň
Uchovávajte v chladničke pri teplote (2°C – 8°C). Neuchovávajte v mrazničke. Nevystavujte
nadmernému teplu alebo priamemu slnečnému svetlu.
Po vložení náplne do pera
Uchovávajte pri teplote do 30°C. Neuchovávajte v chladničke. Pero obsahujúce náplň neuchovávajte
s nasadenou ihlou.
6.5 Druh obalu a obsah balenia
Suspenzia sa plní do náplní z kremičitého skla typu I, ktoré sú utesnené butylovým alebo halobutylovým diskovým uzáverom s piestom a zabezpečené alumíniovým tesnením. Na ošetrenie piestu a/alebo skla náplne sa môže použiť dimetikón alebo silikónová emulzia.
Nie všetky veľkosti balenia musia byť uvedené do obehu.
5 x 3 ml Liprolog Mix25 náplne pre 3 ml pero.
2 x (5 x 3 ml) Liprolog Mix25 náplne pre 3 ml pero.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s
národnýmipožiadavkami.
Návod na použitie
Liprolog Mix25 náplne používajte s perom označeným CE značkou podľa odporúčania v informácii poskytovanej výrobcom pomôcky.
a) Príprava dávky
Bezprostredne pred použitím sa náplne obsahujúce Liprolog Mix25 desaťkrát premiešajú prevaľovaním v dlaniach a desaťkrát prevrátia o 180° z dôvodu premiešania inzulínu, pokiaľ sa
nedocieli rovnomerný zákal alebo mliečne zafarbenie. Ak sa tak nestane, zopakujte vyššie uvedený postup, až sa obsah nepremieša. Náplne obsahujú malú sklenenú guľôčku uľahčujúcu miešanie. Netraste rázne, pretože to môže spôsobiť spenenie, ktoré by mohlo ovplyvniť správne odmeranie dávky.
Náplne sa majú často kontrolovať a nesmú sa použiť, pokiaľ inzulín tvorí zhluky alebo pokiaľ pevné biele častice ostávajú na dne alebo na stene náplne, ktorá tým získava matný vzhľad.
V náplni Liprologu Mix25 nie je možné miešať iný inzulín. Náplne sa nemôžu znovu plniť.
Nasleduje všeobecný popis použitia. U každého jednotlivého pera sa musia dodržiavať inštrukcie
výrobcu na založenie náplne, pripojenie ihly a aplikáciu injekcie inzulínu.
b) Aplikácia dávky
1. Umyte si ruky.
2. Vyberte miesto vpichu.
3. Očistite kožu podľa inštrukcie.
4. Odstráňte vonkajší ochranný kryt ihly.
5. Stabilizujte kožu tak, že ju buď napnete alebo vytvoríte väčšiu kožnú riasu. Ihlu vpichnite podľa
inštrukcie.
6. Stlačte dávkovacie tlačidlo.
7. Vytiahnite ihlu a miesto vpichu niekoľko sekúnd jemne tlačte. Miesto nemasírujte.
8. Pomocou vonkajšieho ochranného krytu ihlu odskrutkujte a bezpečne znehodnoťte.
9. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby rovnaké miesto nebolo použité
v priemere viackrát ako raz za mesiac.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Eli Lilly Nederland B.V., Grootslag 1-5, 3991 RA Houten, Holandsko.
8. REGISTRAČNÉ ČÍSLA
EU/1/01/195/003 5 x 3 ml Liprolog Mix25 náplne pre 3 ml pero
EU/1/01/195/011 2 x (5 x 3 ml) Liprolog Mix25 náplne pre 3 ml pero
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 1. augusta 2001
Dátum posledného predĺženia: 1. augusta 2006
10. DÁTUM REVÍZIE TEXTU
1. NÁZOV LIEKU
Liprolog Mix50 100 U/ml, injekčná suspenzia v náplni
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
2.1 Všeobecný opis
Liprolog Mix50 je biela sterilná suspenzia.
2.2 Kvalitatívne a kvantitatívne zloženie
1 ml obsahuje 100 U (zodpovedá 3,5 mg) inzulín lispro (pôvod z rekombinantnej DNA
produkovanej E.coli). Každé balenie obsahuje 3ml, čo zodpovedá 300 U inzulínu lispro. Liprolog Mix50 tvorí 50% roztok inzulínu lispro a 50% suspenzia inzulínu lispro izofán. Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčná suspenzia.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Liprolog Mix50 je určený na liečbu pacientov s diabetes mellitus, ktorí potrebujú inzulín na udržanie normálnej glukózovej homeostázy.
4.2 Dávkovanie a spôsob podávania
Dávkovanie určí lekár v súlade s potrebami pacienta.
Liprolog Mix50 sa môže podať krátko pred jedlom. V prípade potreby sa Liprolog Mix50 môže podať i bezprostredne po jedle. Liprolog Mix50 sa aplikuje len subkutánnou injekciou. Liprolog Mix50 sa nemá nikdy podať intravenózne.
Subkutánne sa má podať v hornej časti ramien, na stehnách, zadku alebo bruchu. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužilo viackrát ako približne raz za mesiac.
Pri subkutánnej aplikácii Liprologu Mix50 je potrebné sa starostlivo uistiť o tom, že nedošlo
k aplikácii do cievy. Po aplikácii sa miesto vpichu nemá masírovať. Pacient musí byť riadne poučený
o správnej aplikačnej technike.
Po subkutánnej aplikácii Liprologu Mix50 dochádza k rýchlemu nástupu účinku a skorému dosiahnutiu vrcholu aktivity Liprologu. To umožňuje podanie Liprologu Mix50 v tesnej časovej súvislosti s jedlom. Trvanie účinku zložky suspenzie inzulínu lispro izofán (Basal) Liprologu Mix50 je veľmi podobné účinku bazálneho inzulínu (NPH).
Časový priebeh aktivity akéhokoľvek inzulínu sa môže významne líšiť u rôznych osôb alebo u jednej
osoby v rôznych časových intervaloch. Rovnako ako u všetkých inzulínových prípravkov závisí trvanie účinku Liprologu Mix50 na dávke, mieste vpichu, krvnom zásobovaní, teplote a fyzickej aktivite.
4.3 Kontraindikácie
Precitlivenosť na inzulín lispro alebo na ktorúkoľvek z pomocných látok. Hypoglykémia.
4.4 Osobitné upozornenia a opatrenia pri používaní
Liprolog Mix50 sa nesmie za žiadnych okolností podať intravenózne.
Prechod pacienta na iný typ alebo značku inzulínu sa musí uskutočniť pod prísnym lekárskym dohľadom. Zmeny koncentrácie, značky (výrobcu), typu (regular, NPH, lente a i.), druhu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo spôsobu výroby (rekombinantná DNA oproti inzulínu zvieracieho pôvodu) môžu mať za následok potrebu zmeny dávkovania.
Dlhotrvajúci diabetes, intenzifikovaná inzulínová terapia, diabetická neuropatia alebo užívanie liekov, ako sú beta-blokátory, môžu zmeniť alebo zmierniť skoré varovné príznaky hypoglykémie.
Malý počet pacientov, ktorí mali hypoglykemické reakcie po prevode z inzulínu zvieracieho pôvodu na ľudský inzulín, uvádzalo, že skoré varovné príznaky hypoglykémie boli menej výrazné alebo odlišné od tých, ktoré zažili pri použití predchádzajúceho inzulínu. Nekontrolované hypoglykemické alebo hyperglykemické reakcie môžu spôsobiť stratu vedomia, kómu alebo smrť.
Použitie nedostatočných dávok alebo prerušenie liečby, najmä u inzulín-dependentných diabetikov,
môže viesť k hyperglykémii a diabetickej ketoacidóze; stavom, ktoré môžu byť letálne.
Potreba inzulínu môže byť znížená pri poškodení funkcie obličiek. Potreba inzulínu môže byť znížená u pacientov s poškodením funkcie pečene z dôvodov nižšej kapacity pre glukoneogenézu a zhoršeného odbúravania inzulínu; avšak u pacientov s chronickým poškodením funkcie pečene môže zvýšenie inzulínovej rezistencie viesť ku vyššej potrebe inzulínu.
Potreba inzulínu sa môže zvýšiť počas ochorenia alebo vplyvom emocionálnych stresov.
Úprava dávky môže byť rovnako potrebná, pokiaľ pacienti vykonávajú zvýšenú fyzickú aktivitu alebo
menia svoju zvyčajnú diétu. Cvičenie ihneď po požití potravy môže zvýšiť riziko hypoglykémie.
Podanie inzulínu lispro deťom mladším ako 12 rokov sa má zvážiť iba v prípade očakávaného prínosu
v porovnaní s regular inzulínom.
Kombinácia Liprologu Mix50 a pioglitazónu
V prípadoch, keď sa použil pioglitazón v kombinácii s inzulínom, boli zaznamenané prípady srdcového zlyhania, najmä u pacientov s rizikovými faktormi pre vznik srdcového zlyhania. Treba
mať na zreteli tieto fakty v prípade, že sa zvažuje liečba kombináciou pioglitazónu a Liprologu Mix50. Ak pacient používa danú kombináciu, je u neho potrebné sledovať znaky a symptómy srdcového zlyhania, priberanie na hmotnosti a edém. Ak sa zistí akékoľvek zhoršenie srdcových symptómov, pioglitazón sa musí prestať podávať.
4.5 Liekové a iné interakcie
Potreba inzulínu sa môže zvýšiť látkami s hyperglykemickým účinkom, ako je
perorálna antikoncepcia, kortikosteroidy alebo hormonálna substitúcia počas liečby porúch štítnej žľazy, danazol, beta2-mimetiká (ritodrín, salbutamol, terbutalín).
Potreba inzulínu sa môže znížiť pri podávaní liekov s hypoglykemickým účinkom ako sú perorálne antidiabetiká, salicyláty (napr. kyselina acetylosalicylová), sulfónamidy, niektoré antidepresíva (inhibítory monoaminooxidázy, selektívne inhibítory spätného vychytávania sérotonínu), niektoré
inhibítory angiotenzín konvertujúceho enzýmu (kaptopril, enalapril), blokátory receptorov angiotenzínu II, beta-blokátory, oktreotid alebo alkohol.
Miešanie Liprologu Mix50 s inými inzulínmi sa neskúmalo.
Užívanie iných liekov podávaných súčasne s Liprologom Mix50 sa má konzultovať s lekárom (pozri
časť 4.4).
4.6 Fertilita, gravidita a laktácia
Údaje o veľkom počte gravidných žien užívajúcich inzulín lispro nepreukázali žiadne nežiaduce
účinky na graviditu alebo na zdravie plodu/novorodenca.
Udržanie dobrej kontroly glykémie počas gravidity je základnou požiadavkou liečby diabetu
u pacientky liečenej inzulínom pri inzulín-dependentnom alebo gestačnom diabete. Potreba inzulínu sa
zvyčajne znižuje počas prvého trimestra a zvyšuje počas druhého a tretieho trimestra. Pacientky s diabetom majú byť poučené o tom, aby informovali svojho lekára v prípade gravidity alebo ak graviditu zvažujú. Starostlivé monitorovanie glykémie, rovnako ako aj celkového zdravotného stavu, je základnou požiadavkou u gravidných s diabetom.
U dojčiacich diabetičiek môže vzniknúť potreba úpravy dávky inzulínu, diéty alebo oboje.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta koncentrovať sa a reagovať môže byť porušená v dôsledku hypoglykémie. To môže byť riskantné v situáciách špeciálne vyžadujúcich vyššie uvedené schopnosti (napr. vedenie auta alebo obsluha strojov).
Pacient má byť poučený o potrebe zabrániť hypoglykémii počas vedenia vozidla, čo je obzvlášť dôležité u tých osôb, ktoré majú zníženú alebo chýbajúcu vnímavosť varovných príznakov hypoglykémie alebo majú časté hypoglykemické epizódy. Za týchto okolností sa musí starostlivo zvážiť vhodnosť vedenia vozidiel.
4.8 Nežiaduce účinky
Najčastejším nežiaducim účinkom inzulínovej terapie u pacienta s diabetom je hypoglykémia. Závažná hypoglykémia môže viesť ku strate vedomia a v extrémnych prípadoch ku smrti. Frekvencia výskytu hypoglykémie nie je uvedená, pretože hypoglykémia je výsledkom pôsobenia nielen dávky inzulínu ale aj iných faktorov, napr. diéta pacienta a fyzická aktivita.
Často (1/100 až <1/10) sa u pacientov objavuje lokálna precitlivenosť. V mieste aplikácie inzulínu sa môže vyskytnúť začervenanie, opuch a svrbenie. Tento stav obvykle ustúpi počas niekoľkých dní alebo týždňov. V niektorých prípadoch môže byť tento stav zapríčinený inými faktormi ako inzulínom, napríklad iritáciou kože dezinfekčným prostriedkom alebo nesprávnou injekčnou technikou. Systémová alergia, ktorá je zriedkavá (1/10 000 až <1/1 000), ale potenciálne závažnejšia,
je generalizovanou alergiou na inzulín. Môže spôsobiť vyrážky po celom tele, dýchavičnosť, pískanie, pokles krvného tlaku, zrýchlený pulz alebo potenie. Ťažké stavy generalizovanej alergie môžu ohrozovať život.
Lipodystrofia v mieste aplikácie injekcie je menej častá (1/1 000 až <1/100).
Prípady edémov počas inzulínovej liečby boli hlásené najmä vtedy, keď v dôsledku intenzívnejšej inzulinoterapie došlo k zlepšeniu predchádzajúcej zlej metabolickej kompenzácie.
Hlásenie podozrení na nežiaduce reakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné
monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili

akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.4.9 PredávkovanieInzulín nemá špecifickú definíciu predávkovania, pretože koncentrácia glukózy v sére je výsledkom komplexných interakcií medzi hladinou inzulínu, dostupnosťou glukózy a ostatnými metabolickými procesmi. Hypoglykémia sa môže objaviť ako dôsledok nadbytku inzulínovej aktivity v pomere
k príjmu potravy a výdaju energie.
Hypoglykémia môže byť spojená s nevšímavosťou, zmätenosťou, palpitáciami, bolesťami hlavy,
potením a vracaním.
Mierne epizódy hypoglykémie reagujú na perorálne podanie glukózy, iného cukru, príp. produktu obsahujúceho sacharidy.
Korekcia stredne ťažkej hypoglykémie sa môže uskutočniť intramuskulárnou alebo subkutánnou aplikáciou glukagónu a následným perorálnym podaním sacharidov, pokiaľ sa pacient dostatočne zotaví. Pacienti, ktorí nereagujú na glukagón, musia dostať infúziu glukózy intravenózne.
Pokiaľ je pacient v kóme, glukagón sa má aplikovať intramuskulárne alebo subkutánne. Pokiaľ však glukagón nie je k dispozícii alebo pacient na jeho podanie nereaguje, musí sa podať roztok glukózy intravenózne. Akonáhle sa pacient preberie z bezvedomia, musí sa najesť.
Po zdanlivej úprave klinického stavu môže byť potrebný trvalý príjem sacharidov a sledovanie
pacienta, pretože hypoglykémia sa môže opakovať.
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Inzulíny a ich analógy, strednodobo pôsobiace v kombinácii s rýchlopôsobiacimi inzulínmi, ATC kód: A10A D04
Liprolog Mix50 je vopred namiešaná suspenzia obsahujúca inzulín lispro (rýchlopôsobiaci analóg
ľudského inzulínu) a inzulín lispro izofán (strednodobo pôsobiaci analóg ľudského inzulínu). Primárnym účinkom inzulínu lispro je regulácia glukózového metabolizmu.
Inzulín má navyše ďalšie anabolické a anti-katabolické vlastnosti na mnoho rôznych tkanív.
V svalovom tkanive tieto účinky zahŕňajú zvýšenie syntézy glykogénu, mastných kyselín, glycerolu a proteínov a vychytávanie aminokyselín a zároveň zníženie glykogenolýzy, glukoneogenézy, ketogenézy, lipolýzy, proteínového katabolizmu a tvorby aminokyselín.
Rýchly nástup účinku inzulínu lispro (približne 15 minút) umožňuje jeho podanie v tesnej časovej
súvislosti s jedlom (v rozmedzí 0 až 15 minút pred jedlom) v porovnaní s regular inzulínom
(30 až 45 minút pred jedlom). Po subkutánnej aplikácii Liprologu Mix50 dochádza k rýchlemu nástupu účinku a skorému dosiahnutiu vrcholu aktivity inzulínu lispro. Profil účinku Liprologu Basal je veľmi podobný účinku bazálneho inzulínu (NPH) a pretrváva počas približne 15 hodín. Na nasledujúcom obrázku je zobrazená farmakodynamika Liprologu Mix50 a Liprologu Basal.
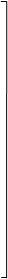
Humalog Mix50

NPL
Hypoglykemická
aktivita
0 4 8 12 16 20 24
Čas, hodiny
Graf zobrazuje relatívne množstvo glukózy v závislosti na čase potrebné na udržanie celkovej plazmatickej glukózovej koncentrácie testovaného jedinca blízko hladinám nalačno a je indikátorom efektu týchto inzulínov na glukózový metabolizmus v závislosti na čase.
Glukodynamická odpoveď na inzulín lispro nie je ovplyvnená poškodením funkcie pečene alebo obličiek. Glukodynamické rozdiely medzi inzulínom lispro a rozpustným ľudským inzulínom merané v priebehu glukózového clampu boli udržané v širokom spektre renálnych funkcií.
Bolo preukázané, že inzulín lispro je molárne ekvipotentný s ľudským inzulínom, ale jeho účinok
nastupuje rýchlejšie a má kratšiu dobu trvania.
5.2 Farmakokinetické vlastnostiPodľa farmakokinetických vlastností je inzulín lispro zlúčenina, ktorá sa rýchlo vstrebáva a dosahuje maximálne hladiny v krvi 30 až 70 minút po subkutánnom podaní. Farmakokinetika suspenzie inzulínu lispro izofán je zhodná so strednodobo pôsobiacimi inzulínmi ako je NPH. Farmakokinetika Liprologu Mix50 reprezentuje individuálne farmakokinetické vlastnosti jeho dvoch zložiek. Ak vezmeme do úvahy klinický význam týchto kinetík, je vhodnejšie vyšetriť krivky utilizácie glukózy. (pozri časť 5.1).
Inzulín lispro je u pacientov s renálnou insuficienciou absorbovaný rýchlejšie ako rozpustný ľudský inzulín. U pacientov s diabetom typu 2 v celom širokom spektre renálnych funkcií boli farmakokinetické diferencie medzi inzulínom lispro a rozpustným ľudským inzulínom všeobecne udržané a ukázali sa nezávislými na renálnych funkciách. Inzulín lispro je u pacientov s poškodenou funkciou pečene absorbovaný a eliminovaný rýchlejšie v porovnaní s rozpustným ľudským inzulínom.
5.3 Predklinické údaje o bezpečnostiPri testoch uskutočnených
in vitro zahŕňajúcich väzbu na inzulínové receptory a účinky na rastúce bunky, sa inzulín lispro správal spôsobom, ktorý veľmi pripomínal ľudský inzulín. Štúdie tiež preukázali, že disociácia väzby inzulínu lispro na inzulínový receptor je totožná s ľudským inzulínom. Akútne, jeden mesiac a dvanásť mesiacov trvajúce toxikologické štúdie nepreukázali žiadne
významné toxikologické účinky.
V štúdiách na zvieratách inzulín lispro nespôsoboval poškodenie plodnosti, prejavy embryotoxicity alebo teratogenicity.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Protamíniumsulfát Metakrezol[2,20 mg/ml] Fenol [1,00 mg/ml] Glycerol
Heptahydrát hydrogénfosforečnanu sodného
Oxid zinočnatý
Voda na injekciu
Kyselina chlorovodíková a hydroxid sodný môžu byť použité na úpravu pH na 7,0 - 7,8.
6.2 Inkompatibility
Miešanie Liprologu Mix50 s inými inzulínmi sa neskúmalo. Pre nedostatok štúdií kompatibility
nesmie byť tento liek miešaný s inými liekmi.
6.3 Čas použiteľnosti
Nepoužitá náplň
3 roky
Po vložení náplne do pera
28 dní
6.4 Špeciálne upozornenia na uchovávanie
Nepoužitá náplň
Uchovávajte v chladničke pri teplote (2°C – 8°C). Neuchovávajte v mrazničke. Nevystavujte
nadmernému teplu alebo priamemu slnečnému svetlu.
Po vložení náplne do pera
Uchovávajte pri teplote do 30°C. Neuchovávajte v chladničke. Pero obsahujúce náplň neuchovávajte
s nasadenou ihlou.
6.5 Druh obalu a obsah balenia a špeciálne zariadenie na použitie, podanie alebo implantáciu
Suspenzia sa plní do náplní z kremičitého skla typu I, ktoré sú utesnené butylovým alebo halobutylovým diskovým uzáverom s piestom a zabezpečené alumíniovým tesnením. Na ošetrenie piestu a/alebo skla náplne sa môže použiť dimetikón alebo silikónová emulzia.
Nie všetky veľkosti balenia musia byť uvedené do obehu.
5 x 3 ml Liprolog Mix50 náplne pre 3 ml pero.
2x (5 x 3 ml) Liprolog Mix50 náplne pre 3 ml pero.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými požiadavkami.
Návod na použitie
Liprolog Mix50 náplne používajte s perom označeným CE značkou podľa odporúčania v informácii poskytovanej výrobcom pomôcky.
a) Príprava dávky
Bezprostredne pred použitím sa náplne obsahujúce Liprolog Mix50 desaťkrát premiešajú prevaľovaním v dlaniach a desaťkrát prevrátia o 180° z dôvodu premiešania inzulínu, pokiaľ sa
nedocieli rovnomerný zákal alebo mliečne zafarbenie. Ak sa tak nestane, zopakujte vyššie uvedený postup, až sa obsah nepremieša. Náplne obsahujú malú sklenenú guľôčku uľahčujúcu miešanie. Netraste rázne, pretože to môže spôsobiť spenenie, ktoré by mohlo ovplyvniť správne odmeranie dávky.
Náplne sa majú často kontrolovať a nesmú sa použiť, pokiaľ inzulín tvorí zhluky alebo pokiaľ pevné biele častice ostávajú na dne alebo na stene náplne, ktorá tým získava matný vzhľad.
V náplni Liprologu Mix50 nie je možné miešať iný inzulín. Náplne sa nemôžu znovu plniť.
Nasleduje všeobecný popis použitia. U každého jednotlivého pera sa musia dodržiavať inštrukcie
výrobcu na založenie náplne, pripojenie ihly a aplikáciu injekcie inzulínu.
b) Aplikácia dávky
1. Umyte si ruky.
2. Vyberte miesto vpichu.
3. Očistite kožu podľa inštrukcie.
4. Odstráňte vonkajší ochranný kryt ihly.
5. Stabilizujte kožu tak, že ju buď napnete alebo vytvoríte väčšiu kožnú riasu. Ihlu vpichnite podľa
inštrukcie.
6. Stlačte dávkovacie tlačidlo.
7. Vytiahnite ihlu a miesto vpichu niekoľko sekúnd jemne tlačte. Miesto nemasírujte.
8. Pomocou vonkajšieho ochranného krytu ihlu odskrutkujte a bezpečne znehodnoťte.
9. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby rovnaké miesto nebolo použité
v priemere viackrát ako raz za mesiac.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Eli Lilly Nederland B.V., Grootslag 1-5, 3991 RA Houten, Holandsko.
8. REGISTRAČNÉ ČÍSLA
EU/1/01/195/004 5 x 3 ml Liprolog Mix50 náplne pre 3 ml pero
EU/1/01/195/012 2 x (5 x 3 ml) Liprolog Mix50 náplne pre 3 ml pero
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 1. augusta 2001
Dátum posledného predĺženia: 1. augusta 2006
10. DÁTUM REVÍZIE TEXTU
1. NÁZOV LIEKU
Liprolog Basal 100 U/ml injekčná suspenzia v náplni
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
2.1 Všeobecný opis
Liprolog Basal je biela sterilná suspenzia.
2.2 Kvalitatívne a kvantitatívne zloženie
1 ml obsahuje 100 U (zodpovedá 3,5 mg) inzulínu lispro (pôvod z rekombinantnej DNA
produkovanej E.coli). Každé balenie obsahuje 3 ml, čo zodpovedá 300 U inzulínu lispro. Liprolog Basal tvorí suspenzia inzulínu lispro izofán.
Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčná suspenzia.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Liprolog Basal je určený na liečbu pacientov s diabetes mellitus, ktorí potrebujú inzulín na udržanie normálnej glukózovej homeostázy.
4.2 Dávkovanie a spôsob podávania
Dávkovanie určí lekár v súlade s potrebami pacienta.
Liprolog Basal sa môže miešať alebo podávať spolu s Liprologom. Liprolog Basal sa má aplikovať iba
subkutánnou injekciou. Liprolog Basal sa nemá nikdy podať intravenózne.
Subkutánne sa má podať v hornej časti ramien, na stehnách, zadku alebo bruchu . Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužilo viackrát ako približne raz za mesiac.
Pri subkutánnej aplikácii Liprologu Basal je potrebné sa starostlivo uistiť o tom, že nedošlo k aplikácii do cievy. Po aplikácii sa miesto vpichu nemá masírovať. Pacient musí byť riadne poučený o správnej aplikačnej technike.
Profil účinku Liprologu Basal je veľmi podobný účinku bazálneho inzulínu (NPH) po dobu približne
15 hodín. Časový priebeh aktivity akéhokoľvek inzulínu sa môže významne líšiť u rôznych osôb alebo u jednej osoby v rôznych časových intervaloch. Rovnako ako u všetkých inzulínových prípravkov závisí trvanie účinku Liprolog u Basal na dávke, mieste vpichu, krvnom zásobovaní, teplote a fyzickej aktivite.
4.3 Kontraindikácie
Precitlivenosť na inzulín lispro alebo na ktorúkoľvek z pomocných látok. Hypoglykémia.
4.4 Osobitné upozornenia a opatrenia pri používaní
Liprolog Basal sa nesmie za žiadnych okolností podať intravenózne.
Prechod pacienta na iný typ alebo značku inzulínu sa musí uskutočniť pod prísnym lekárskym dohľadom. Zmeny koncentrácie, značky (výrobcu), typu (regular, NPH, lente ai.), druhu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo spôsobu výroby (rekombinantná DNA oproti inzulínu zvieracieho pôvodu) môžu mať za následok potrebu zmeny dávkovania.
Dlhotrvajúci diabetes, intenzifikovaná inzulínová terapia, diabetická neuropatia alebo užívanie liekov, ako sú beta-blokátory môžu zmeniť alebo zmierniť skoré varovné príznaky hypoglykémie.
Malý počet pacientov, ktorí mali hypoglykemické reakcie po prechode z inzulínu zvieracieho pôvodu na ľudský inzulín, uvádzalo, že skoré varovné príznaky hypoglykémie boli menej výrazné alebo odlišné od tých, ktoré zažili pri použití predchádzajúceho inzulínu. Nekontrolované hypoglykemické alebo hyperglykemické reakcie môžu spôsobiť stratu vedomia, kómu alebo smrť.
Použitie nedostatočných dávok alebo prerušenie liečby, najmä u inzulín-dependentných diabetikov,
môže viesť k hyperglykémii a diabetickej ketoacidóze; stavom, ktoré môžu byť letálne.
Potreba inzulínu môže byť znížená pri poškodení funkcie obličiek.
Potreba inzulínu môže byť znížená u pacientov s poškodením funkcie pečene z dôvodov nižšej kapacity pre glukoneogenézu a zhoršeného odbúravania inzulínu; avšak u pacientov s chronickým poškodením funkcie pečene môže zvýšenie inzulínovej rezistencie viesť ku vyššej potrebe inzulínu.
Potreba inzulínu sa môže zvýšiť počas ochorenia alebo vplyvom emocionálnych stresov.
Úprava dávky môže byť rovnako potrebná, pokiaľ pacienti vykonávajú zvýšenú fyzickú aktivitu alebo menia svoju zvyčajnú diétu. Cvičenie ihneď po požití potravy môže zvýšiť riziko hypoglykémie.
Podanie inzulínu lispro deťom mladším ako 12 rokov sa má zvážiť iba v prípade očakávaného prínosu
v porovnaní s regular inzulínom.
Kombinácia Liprologu Basal a pioglitazónu
V prípadoch, keď sa použil pioglitazón v kombinácii s inzulínom, boli zaznamenané prípady srdcového zlyhania, najmä u pacientov s rizikovými faktormi pre vznik srdcového zlyhania. Treba mať na zreteli tieto fakty v prípade, že sa zvažuje liečba kombináciou pioglitazónu a Liprologu Basal. Ak pacient používa danú kombináciu, je u neho potrebné sledovať znaky a symptómy srdcového zlyhania, priberanie na hmotnosti a edém. Ak sa zistí akékoľvek zhoršenie srdcových symptómov, pioglitazón sa musí prestať podávať.
4.5 Liekové a iné interakcie
Potreba inzulínu sa môže zvýšiť látkami s hyperglykemickým účinkom, ako je perorálna antikoncepcia, kortikosteroidy alebo hormonálna substitúcia počas liečby porúch štítnej žľazy, danazol, beta2-mimetiká (ritodrín, salbutamol, terbutalín).
Potreba inzulínu sa môže znížiť pri podávaní liekov s hypoglykemickým účinkom ako sú perorálne antidiabetiká, salicyláty (napr. kyselina acetylosalicylová), sulfónamidy, niektoré antidepresíva (inhibítory monoaminooxidázy, selektívne inhibítory spätného vychytávania sérotonínu), niektoré
inhibítory angiotenzín konvertujúceho enzýmu (kaptopril, enalapril), blokátory receptorov angiotenzínu II, beta-blokátory, oktreotid alebo alkohol.
Miešanie Liprologu Basal s inzulínmi inými ako je Liprolog sa neskúmalo.
Užívanie iných liekov podávaných súčasne s Liprologom Basal sa musí konzultovať s lekárom (pozri
časť 4.4).
4.6 Fertilita, gravidita a laktácia
Údaje o veľkom počte gravidných žien užívajúcich inzulín lispro nepreukázali žiadne nežiaduce
účinky na graviditu alebo na zdravie plodu/novorodenca.
Udržanie dobrej kontroly glykémie počas gravidity je základnou požiadavkou liečby diabetu
u pacientky liečenej inzulínom pri inzulín-dependentnom alebo gestačnom diabete. Potreba inzulínu sa zvyčajne znižuje počas prvého trimestra a zvyšuje počas druhého a tretieho trimestra. Pacientky
s diabetom majú byť poučené o tom, aby informovali svojho lekára v prípade gravidity alebo ak graviditu zvažujú. Starostlivé monitorovanie glykémie, rovnako ako aj celkového zdravotného stavu, je základnou požiadavkou u gravidných s diabetom.
U dojčiacich diabetičiek môže vzniknúť potreba úpravy dávky inzulínu, diéty alebo oboje.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta koncentrovať sa a reagovať môže byť porušená v dôsledku hypoglykémie. Môže to byť riskantné v situáciách špeciálne vyžadujúcich vyššie uvedené schopnosti (napr. vedenie auta alebo obsluha strojov).
Pacient má byť poučený o potrebe zabrániť hypoglykémii počas vedenia vozidla, čo je obzvlášť dôležité u tých osôb, ktoré majú zníženú alebo chýbajúcu vnímavosť varovných príznakov hypoglykémie alebo majú časté hypoglykemické epizódy. Za týchto okolností sa musí starostlivo zvážiť vhodnosť vedenia vozidiel.
4.8 Nežiaduce účinky
Najčastejším nežiaducim účinkom inzulínovej terapie u pacienta s diabetom je hypoglykémia. Závažná hypoglykémia môže viesť ku strate vedomia a v extrémnych prípadoch ku smrti. Frekvencia výskytu hypoglykémie nie je uvedená, pretože hypoglykémia je výsledkom pôsobenia nielen dávky inzulínu ale aj iných faktorov, napr. diéta pacienta a fyzická aktivita.
Často (1/100 až <1/10) sa u pacientov objavuje lokálna precitlivenosť. V mieste aplikácie inzulínu sa môže vyskytnúť začervenanie, opuch a svrbenie. Tento stav obvykle ustúpi počas niekoľkých dní alebo týždňov. V niektorých prípadoch môže byť tento stav zapríčinený inými faktormi ako inzulínom, napríklad iritáciou kože dezinfekčným prostriedkom alebo nesprávnou injekčnou technikou. Systémová alergia, ktorá je zriedkavá (1/10 000 až <1/1 000), ale potenciálne závažnejšia,
je generalizovanou alergiou na inzulín. Môže spôsobiť vyrážky po celom tele, dýchavičnosť, pískanie, pokles krvného tlaku, zrýchlený pulz alebo potenie. Ťažké stavy generalizovanej alergie môžu ohrozovať život.
Lipodystrofia v mieste aplikácie injekcie je menej častá (1/1 000 až <1/100).
Prípady edémov počas inzulínovej liečby boli hlásené najmä vtedy, keď v dôsledku intenzívnejšej inzulinoterapie došlo k zlepšeniu predchádzajúcej zlej metabolickej kompenzácie.
Hlásenie podozrení na nežiaduce reakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné
monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili

akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.4.9 PredávkovanieInzulín nemá špecifickú definíciu predávkovania, pretože sérová hladina krvného cukru je výsledkom komplexných interakcií medzi hladinou inzulínu, dostupnosťou glukózy a ostatnými metabolickými procesmi. Hypoglykémia sa môže objaviť ako dôsledok nadbytku inzulínovej aktivity v pomere
k príjmu potravy a výdaju energie.
Hypoglykémia môže byť spojená s nevšímavosťou, zmätenosťou, palpitáciami, bolesťami hlavy,
potením a vracaním.
Mierne epizódy hypoglykémie reagujú na perorálne podanie glukózy, iného cukru, príp. produktu obsahujúceho sacharidy.
Korekcia stredne ťažkej hypoglykémie sa môže uskutočniť intramuskulárnou alebo subkutánnou aplikáciou glukagónu a následným perorálnym podaním sacharidov, pokiaľ sa pacient dostatočne zotaví. Pacienti, ktorí nereagujú na glukagón, musia dostať infúziu glukózy intravenózne.
Pokiaľ je pacient v kóme, má sa aplikovať glukagón intramuskulárne alebo subkutánne. Pokiaľ však glukagón nie je k dispozícii alebo pacient na jeho podanie nereaguje, musí sa podať roztok glukózy intravenózne. Akonáhle sa pacient preberie z bezvedomia, musí sa najesť.
Po zdanlivej úprave klinického stavu môže byť potrebný trvalý príjem sacharidov a sledovanie
pacienta, pretože hypoglykémia sa môže opakovať.
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Inzulíny a ich analógy, strednodobo pôsobiace inzulíny, ATC kód: A10A C04.
Primárnym účinkom inzulínu lispro je regulácia glukózového metabolizmu.
Navyše má inzulín ďalšie anabolické a anti-katabolické vlastnosti na varietu rôznych tkanív.
V svalovom tkanive tieto účinky zahŕňajú zvýšenie syntézy glykogénu, mastných kyselín, glycerolu a proteínov a vychytávanie aminokyselín a zároveň zníženie glykogenolýzy, glukoneogenézy, ketogenézy, lipolýzy, proteínového katabolizmu a tvorby aminokyselín.
Profil účinku Liprologu Basal je veľmi podobný účinku bazálneho inzulínu (NPH) v časovom
intervale približne 15 hodín.
Glukodynamická odpoveď na inzulín lispro nie je ovplyvnená poškodením funkcie obličiek alebo pečene. Glukodynamické rozdiely medzi inzulínom lispro a rozpustným ľudským inzulínom merané v priebehu glukózového clampu boli udržané v širokom spektre renálnych funkcií.
Bolo preukázané, že inzulín lispro je molárne ekvipotentný s ľudským inzulínom, ale jeho účinok
nastupuje rýchlejšie a má kratšiu dobu trvania.
5.2 Farmakokinetické vlastnostiLiprolog Basal má predĺženú absorpciu a dosahuje maximálne koncentrácie inzulínu približne za
6 hodín po aplikácii dávky. Pri hodnotení klinickej významnosti takejto kinetiky je vhodnejšie vyšetriť
krivky utilizácie glukózy.
Inzulín lispro je u pacientov s poškodením funkcie obličiek absorbovaný rýchlejšie ako rozpustný ľudský inzulín. U pacientov s diabetom typu 2 v širokom spektre renálnych funkcií boli farmakokinetické diferencie medzi inzulínom lispro a rozpustným ľudským inzulínom dodržané
a ukázali sa nezávislými na renálnych funkciách. Inzulín lispro je u pacientov s poškodením funkcie
pečene absorbovaný a eliminovaný rýchlejšie v porovnaní s rozpustným ľudským inzulínom.
5.3 Predklinické údaje o bezpečnosti
Pri testoch uskutočnených in vitro zahŕňajúcich väzbu na inzulínové receptory a účinky na rastúce bunky, sa inzulín lispro správal spôsobom, ktorý veľmi pripomínal ľudský inzulín. Štúdie tiež preukázali, že disociácia väzby inzulínu lispro na inzulínový receptor je totožná s ľudským inzulínom. Akútne, jeden mesiac a dvanásť mesiacov trvajúce toxikologické štúdie nepreukázali žiadne
významné toxikologické účinky.
V štúdiách na zvieratách inzulín lispro nespôsoboval poškodenie plodnosti, prejavy embryotoxicity alebo teratogenicity.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Protamíniumsulfát Metakrezol[1,76 mg/ml] Fenol [0,80 mg/ml] Glycerol
Heptahydrát hydrogénfosforečnanu sodného
Oxid zinočnatý
Voda na injekciu
Kyselina chlorovodíková a hydroxid sodný môžu byť použité na úpravu pH na 7,0 - 7,8.
6.2 Inkompatibility
Miešanie Liprologu Basal s inzulínmi inými ako Liprolog sa neskúmalo. Tento liek sa nesmie miešať
s inými liekmi okrem Liprologu.
6.3 Čas použiteľnosti
Nepoužitá náplň
2 roky
Po založení náplne do pera
21 dní
6.4 Špeciálne upozornenia na uchovávanie
Nepoužitá náplň
Uchovávajte v chladničke pri teplote (2°C – 8°C). Neuchovávajte v mrazničke. Nevystavujte
nadmernému teplu alebo priamemu slnečnému svetlu.
Po vložení náplne do pera
Uchovávajte pri teplote do 30°C. Neuchovávajte v chladničke. Pero obsahujúce náplň neuchovávajte
s nasadenou ihlou.
6.5 Druh obalu a obsah balenia a špeciálne zariadenie na použitie, podanie alebo implantáciu
Suspenzia sa plní do náplní z kremičitého skla typu I, ktoré sú utesnené butylovým alebo halobutylovým diskovým uzáverom s piestom a zabezpečené alumíniovým tesnením. Na ošetrenie piestu a/alebo skla náplne sa môže použiť dimetikón alebo silikónová emulzia.
Nie všetky veľkosti balenia musia byť uvedené do obehu.
5 x 3 ml Liprolog Basal náplne pre 3 ml pero
2 x (5 x 3 ml) Liprolog Basal náplne pre 3 ml pero
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými požiadavkami.
Návod na použitie
Liprolog Basal náplne používajte s perom označeným CE značkou podľa odporúčania v informácii poskytovanej výrobcom pomôcky.
a) Príprava dávky
Bezprostredne pred použitím sa náplne obsahujúce Liprolog Basal desaťkrát premiešajú prevaľovaním
v dlaniach a desaťkrát prevrátia o 180° z dôvodu premiešania inzulínu, pokiaľ sa nedocieli
rovnomerný zákal alebo mliečne zafarbenie. Ak sa tak nestane, zopakujte vyššie zmienený postup, až
kým sa obsah premieša. Náplne obsahujú malú sklenenú guľôčku uľahčujúcu miešanie. Netraste rázne, pretože to môže spôsobiť spenenie, ktoré by mohlo ovplyvniť správne odmeranie dávky.
Náplne sa majú často kontrolovať a nesmú sa použiť, pokiaľ inzulín tvorí zhluky alebo pokiaľ pevné biele častice ostávajú na dne alebo na stene náplne, ktorá tým získava matný vzhľad.
V náplni Liprologu Basal nie je možné miešať iný inzulín. Náplne sa nemôžu znovu plniť. Nasleduje všeobecný popis použitia. U každého jednotlivého pera sa musia dodržiavať inštrukcie
výrobcu na založenie náplne, pripojenie ihly a aplikáciu injekcie inzulínu.
b) Aplikácia dávky
1. Umyte si ruky.
2. Vyberte miesto vpichu.
3. Očistite kožu podľa inštrukcie.
4. Odstráňte vonkajší ochranný kryt ihly.
5. Stabilizujte kožu tak, že ju buď napnete alebo vytvoríte väčšiu kožnú riasu. Ihlu vpichnite podľa
inštrukcie.
6. Stlačte dávkovacie tlačidlo.
7. Vytiahnite ihlu a miesto vpichu niekoľko sekúnd jemne tlačte. Miesto nemasírujte.
8. Pomocou vonkajšieho ochranného krytu ihlu odskrutkujte a bezpečne znehodnoťte.
9. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby rovnaké miesto nebolo použité
v priemere viackrát ako raz za mesiac. c) Miešanie inzulínov
Nemiešajte inzulín v injekčných liekovkách s inzulínom v náplniach. Pozri časť 6.2.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Eli Lilly Nederland B.V., Grootslag 1-5, 3991 RA Houten, Holandsko.
8. REGISTRAČNÉ ČÍSLA
EU/1/01/195/022 5 x 3 ml Liprolog Basal náplne pre 3 ml pero
EU/1/01/195/023 2 x (5 x 3 ml) Liprolog Basal náplne pre 3 ml pero
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 1. augusta 2001
Dátum posledného predĺženia: 1. augusta 2006
10. DÁTUM REVÍZIE TEXTU
1. NÁZOV LIEKU
Liprolog 100 U/ml KwikPen, injekčný roztok
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
2.1 Všeobecný opis
Liprolog KwikPen je sterilný, číry, bezfarebný vodný roztok.
2.2 Kvalitatívne a kvantitatívne zloženie
1 ml obsahuje 100 U (zodpovedá 3,5 mg) inzulínu lispro (pôvod z rekombinantnej DNA
produkovanej E.coli). Každá náplň obsahuje 3 ml, čo zodpovedá 300 U inzulínu lispro.
Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčný roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Na liečbu dospelých a detí s diabetes mellitus, ktorí potrebujú inzulín na udržanie normálnej glukózovej homeostázy. Rovnako sa Liprolog KwikPen indikuje na iniciálnu stabilizáciu diabetes mellitus.
4.2 Dávkovanie a spôsob podávania
Dávkovanie stanoví lekár v súlade s potrebami pacienta.
Liprolog sa môže aplikovať krátko pred jedlom. Ak je to potrebné, Liprolog možno podať krátko po jedle. Liprolog sa má aplikovať subkutánnou injekciou alebo kontinuálnou subkutánnou infúziou pomocou pumpy (pozri časť 4.2), avšak môže sa, aj keď sa to neodporúča, podať intramuskulárne.
V prípade potreby môže byť Liprolog podaný aj intravenózne, napr. ak je potrebné kontrolovať
glykémiu počas ketoacidózy, akútneho ochorenia alebo v priebehu operácie a pooperačného stavu.
Miesta subkutánneho podania majú byť horná časť ramien, stehno, zadok alebo brucho. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužilo viackrát ako približne raz za mesiac.
Pri subkutánnej aplikácii Liprologu KwikPen je potrebné sa dôkladne uistiť o tom, že nedošlo
k aplikácii do cievy. Po aplikácii sa miesto vpichu nemá masírovať. Pacient musí byť riadne poučený
o správnej aplikačnej technike.
Liprolog KwikPen účinkuje po subkutánnom podaní rýchlo a kratšiu dobu (2 -5 hodín) v porovnaní
s regular inzulínom. Tento rýchly nástup účinku dovoľuje podávanie injekcie Liprologu (alebo bolusu Liprologu v prípade kontinuálnej subkutánnej infúzie) veľmi krátko pred jedlom alebo po jedle. Časový priebeh aktivity akéhokoľvek inzulínu sa môže významne líšiť u rôznych osôb alebo u jednej osoby v rôznych časových intervaloch. Nástup účinku inzulínu lispro je v porovnaní s rozpustným ľudským inzulínom rýchlejší nezávisle na mieste vpichu. Rovnako ako u všetkých inzulínových
prípravkov závisí trvanie účinku Liprologu KwikPen na dávke, mieste vpichu, krvnom zásobovaní,
teplote a fyzickej aktivite.
Liprolog môže byť podľa rady lekára aplikovaný v kombinácii s dlhšie pôsobiacim inzulínom alebo s derivátmi sulfonylurey podanými perorálne.
Použitie Liprologu v inzulínových infúznych pumpách
Na infúzie inzulínu lispro sa môžu použiť inzulínové infúzne pumpy označené CE. Pred aplikáciou
infúzie inzulínu lispro si preštudujte inštrukcie výrobcu, aby sa zistila vhodnosť alebo iné parametre pre konkrétnu pumpu. Prečítajte si priložený návod na použitie infúznej pumpy a podľa neho postupujte. Spolu s pumpou používajte správny zásobník a katéter. Infúzny set (hadička a kanyla) sa má meniť podľa pokynov, ktoré sú súčasťou infúzneho setu. V prípade hypoglykémie sa musí infúzia prerušiť až do jej odoznenia. Ak si nameráte výrazne nízke alebo opakovane nízke hladiny glukózy
v krvi, upozornite svojho lekára a zvážte, či nie je potrebné infúziu spomaliť alebo zastaviť. Porucha
pumpy alebo upchatie infúzneho setu môže spôsobiť náhly vzostup hladiny glukózy. V prípade podozrenia na porušenie prietoku inzulínu sa riaďte pokynmi v návode na obsluhu, prípadne upovedomte svojho lekára. Pri používaní infúznej pumpy sa nemá Liprolog miešať s inými inzulínmi.
Intravenózna aplikácia inzulínu
Intravenózna aplikácia inzulínu lispro má byť vykonávaná podľa bežnej klinickej praxe pre
intravenózne podávanie, napr. intravenóznym bolusom alebo infúziou. Je nutná častá kontrola hladiny
glukózy v krvi.
Infúzny roztok s koncentráciou od 0,1 U/ml do 1,0 U/ml inzulínu lispro v 0,9% NaCl alebo
5% sacharóze je stabilný pri izbovej teplote po dobu 48 hodín. Pred zahájením infúzie sa odporúča infúznu súpravu prestrieknuť.
4.3 Kontraindikácie
Precitlivenosť na inzulín lispro alebo na ktorúkoľvek z pomocných látok. Hypoglykémia.
4.4 Osobitné upozornenia a opatrenia pri používaní
Prechod pacienta na iný typ alebo značku inzulínu sa musí uskutočniť pod prísnym lekárskym dohľadom. Zmeny koncentrácie, značky (výrobcu), typu (regular, NPH, lente a i.), druhu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo spôsobu výroby (rekombinantná DNA oproti inzulínu zvieracieho pôvodu) môžu mať za následok potrebu zmeny dávkovania. Každý pacient, ktorý užíva popri rýchlopôsobiacom aj bazálny inzulín, musí optimalizovať dávkovanie oboch inzulínov
k dosiahnutiu kontroly glykémie po celý deň, hlavne kontroly glykémie v noci/nalačno.
Dlhotrvajúci diabetes, intenzifikovaná inzulínová terapia, diabetická neuropatia alebo užívanie liekov, ako sú beta-blokátory, môžu zmeniť alebo zmierniť skoré varovné príznaky hypoglykémie.
Malý počet pacientov, ktorí mali hypoglykemické reakcie po prechode z inzulínu zvieracieho pôvodu na ľudský inzulín, uvádzalo, že skoré varovné príznaky hypoglykémie boli menej výrazné alebo odlišné od tých, ktoré zažili pri použití predchádzajúceho inzulínu. Nekontrolované hypoglykemické alebo hyperglykemické reakcie môžu spôsobiť stratu vedomia, kómu alebo smrť.
Použitie neadekvátnych dávok alebo prerušenie liečby, najmä u inzulín-dependentných diabetikov,
môže viesť k hyperglykémii a diabetickej ketoacidóze, ktoré sú potenciálne letálne.
Potreba inzulínu môže byť znížená pri poškodení funkcie obličiek. Potreba inzulínu môže byť znížená
u pacientov s poškodením funkcie pečene z dôvodu nižšej kapacity pre glukoneogenézu a zhoršeného
odbúravania inzulínu. Avšak u pacientov s chronickým poškodením funkcie pečene môže zvýšenie inzulínovej rezistencie viesť k vyššej potrebe inzulínu.
Potreba inzulínu sa môže zvýšiť počas choroby alebo pri emocionálnom rozrušení.
Úprava dávky môže byť tiež potrebná, pokiaľ pacienti vykonávajú zvýšenú fyzickú aktivitu alebo menia svoju zvyčajnú diétu. Cvičenie ihneď po požití potravy môže zvýšiť riziko hypoglykémie. Dôsledok farmakodynamiky rýchlopôsobiaceho analógu ľudského inzulínu je výskyt hypoglykémie, pri porovnaní s rozpustným ľudským inzulínom, sa po injekcii môže vyskytnúť skôr.
Podanie Liprologu deťom má byť zvážené iba v prípade očakávaného prínosu v porovnaní
s rozpustným inzulínom, napr. v súvislosti so zmeneným časovým odstupom aplikácie vzhľadom na
podanie jedla.
Kombinácia Liprologu Mix50 a pioglitazónu
V prípadoch, keď sa použil pioglitazón v kombinácii s inzulínom, boli zaznamenané prípady srdcového zlyhania, najmä u pacientov s rizikovými faktormi pre vznik srdcového zlyhania. Treba
mať na zreteli tieto fakty v prípade, že sa zvažuje liečba kombináciou pioglitazónu a Liprologu Mix50. Ak pacient používa danú kombináciu, je u neho potrebné sledovať znaky a symptómy srdcového zlyhania, priberanie na hmotnosti a edém. Ak sa zistí akékoľvek zhoršenie srdcových symptómov, pioglitazón sa musí prestať podávať.
4.5 Liekové a iné interakcie
Potreba inzulínu sa môže zvýšiť liekmi s hyperglykemickým účinkom, ako je perorálna antikoncepcia, kortikosteroidy alebo hormonálna substitučná terapia pri liečbe porúch štítnej žľazy, danazol, beta2-mimetiká (ritodrín, salbutamol, terbutalín).
Potreba inzulínu sa môže znížiť pri podávaní liekov s hypoglykemickým účinkom, ako sú perorálne antidiabetiká, salicyláty (napríklad kyselina acetylsalicylová), sulfónamidy, niektoré antidepresíva (inhibítory monoaminooxidázy, selektívne inhibítory spätného vychytávania sérotonínu), niektoré inhibítory angiotenzín konvertujúceho enzýmu (kaptopril, enalapril), blokátory receptorov angiotenzínu II, beta-blokátory, oktreotid alebo alkohol.
Používanie iných liekov podávaných súčasne s Liprologom KwikPen sa musí konzultovať s lekárom
(pozri časť 4.4).
4.6 Fertilita, gravidita a laktácia
Údaje o veľkom počte gravidných žien užívajúcich inzulín lispro nepreukázali žiadne nežiaduce
účinky na graviditu alebo na zdravie plodu/novorodenca.
Udržanie dobrej kontroly glykémie počas gravidity je základnou požiadavkou liečby diabetu
u pacientky liečenej inzulínom pri inzulín-dependentnom alebo gestačnom diabete. Potreba inzulínu sa obvykle znižuje počas prvého trimestra a zvyšuje počas druhého a tretieho trimestra. Pacientky
s diabetom majú byť poučené o tom, aby informovali svojho lekára v prípade gravidity alebo pokiaľ graviditu zvažujú. Starostlivé monitorovanie glykémie, rovnako ako aj celkového zdravotného stavu, je základnou požiadavkou u gravidných s diabetom.
Dojčiace diabetičky môžu potrebovať úpravu dávky inzulínu, diéty alebo oboje.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta koncentrovať sa a reagovať môže byť porušená v dôsledku hypoglykémie. To môže byť riskantné v situáciách špeciálne vyžadujúcich vyššie uvedené schopnosti (napr. vedenie auta alebo obsluha strojov).
Pacient má byť poučený o nutnosti zabrániť hypoglykémii počas vedenia vozidla, čo je obzvlášť dôležité u tých osôb, ktoré majú zníženú alebo chýbajúcu vnímavosť varovných príznakov hypoglykémie alebo majú časté hypoglykemické epizódy. Za týchto okolností sa má starostlivo zvážiť vhodnosť vedenia vozidiel.
4.8 Nežiaduce účinkyNajčastejším nežiaducim účinkom inzulínovej terapie u pacienta s diabetom je hypoglykémia. Závažná hypoglykémia môže viesť ku strate vedomia a v extrémnych prípadoch ku smrti. Frekvencia výskytu hypoglykémie nie je uvedená, pretože hypoglykémia je výsledkom pôsobenia nielen dávky inzulínu ale aj iných faktorov, napr. diéta pacienta a fyzická aktivita.
Často (1/100 až <1/10) sa u pacientov objavuje lokálna precitlivenosť. V mieste aplikácie inzulínu sa môže vyskytnúť začervenanie, opuch a svrbenie. Tento stav obvykle ustúpi počas niekoľkých dní alebo týždňov. V niektorých prípadoch môže byť tento stav zapríčinený inými faktormi ako inzulínom, napríklad iritáciou kože dezinfekčným prostriedkom alebo nesprávnou injekčnou technikou. Systémová alergia, ktorá je zriedkavá (1/10 000 až <1/1 000), ale potenciálne závažnejšia,
je generalizovanou alergiou na inzulín. Môže spôsobiť vyrážky po celom tele, dýchavičnosť, pískanie,
pokles krvného tlaku, zrýchlený pulz alebo potenie. Ťažké stavy generalizovanej alergie môžu ohrozovať život.
Lipodystrofia v mieste aplikácie injekcie je menej častá (1/1 000 až <1/100).
Prípady edémov počas inzulínovej liečby boli hlásené najmä vtedy, keď v dôsledku intenzívnejšej inzulinoterapie došlo k zlepšeniu predchádzajúcej zlej metabolickej kompenzácie.
Hlásenie podozrení na nežiaduce reakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.4.9 PredávkovanieInzulín nemá špecifickú definíciu predávkovania, pretože sérová hladina krvného cukru je výsledkom komplexných interakcií medzi hladinou inzulínu, dostupnosťou glukózy a ostatnými metabolickými procesmi. Hypoglykémia sa môže objaviť ako dôsledok nadbytku inzulínu v pomere k príjmu potravy a výdaju energie.
Hypoglykémia môže byť spojená s ľahostajnosťou, zmätenosťou, palpitáciami, bolesťami hlavy,
potením a vracaním.
Mierne epizódy hypoglykémie reagujú na perorálne podanie glukózy alebo iného cukru, prípadne produktu obsahujúceho sacharidy.
Korekcia stredne ťažkej hypoglykémie sa môže uskutočniť intramuskulárnou alebo subkutánnou aplikáciou glukagónu a následným perorálnym podaním uhľohydrátov, pokiaľ sa pacient dostatočne zotaví. Pacienti, ktorí nereagujú na glukagón, musia dostať infúziu glukózy intravenózne.
Pokiaľ je pacient v kóme, glukagón sa má aplikovať intramuskulárne alebo subkutánne. Pokiaľ však glukagón nie je k dispozícii alebo pacient na jeho podanie nereaguje, musí sa podať roztok glukózy intravenózne. Akonáhle sa pacient preberie z bezvedomia, musí sa najesť.
Po zdanlivej úprave klinického stavu môže byť potrebný trvalý príjem sacharidov a sledovanie
pacienta, pretože hypoglykémia sa môže opakovať.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Inzulíny a ich analógy, rýchlopôsobiace inzulíny, ATC kód: A10A B04.
Primárnym účinkom inzulínu lispro je regulácia glukózového metabolizmu.
Navyše má inzulín ďalšie anabolické a antikatabolické účinky na mnoho rôznych tkanív. V svalovom tkanive tieto účinky zahŕňajú zvýšenie syntézy glykogénu, mastných kyselín, glycerolu a proteínov
a vychytávanie aminokyselín a zároveň zníženie glykogenolýzy, glukoneogenézy, ketogenézy,
lipolýzy, proteínového katabolizmu a tvorby aminokyselín.
Inzulín lispro má rýchly nástup účinku (približne 15 minút), čo umožňuje jeho podanie krátko pred alebo po jedle (interval od 0 do 15 minút), v porovnaní s bežným rýchlopôsobiacim inzulínom (aplikácia 30 až 45 minút pred jedlom). Nástup účinku inzulínu lispro je rýchly a trvanie aktivity kratšie (2 až 5 hodín) v porovnaní s regular inzulínom.
Klinické štúdie u pacientov s diabetom typu 1 alebo 2 preukázali nižší výskyt postprandiálnej hyperglykémie u inzulínu lispro v porovnaní s rozpustným ľudským inzulínom.
Rovnako ako u všetkých inzulínových prípravkov môže byť časový priebeh účinku inzulínu lispro odlišný u rôznych jedincov alebo odlišný v rôznych časových intervaloch u rovnakého jedinca
v závislosti na dávke, mieste injekcie, krvnom zásobení, teplote a fyzickej aktivite. Typický priebeh aktivity v čase po subkutánnej injekcii ilustruje nasledujúci graf.
Hypoglykemická aktivita
___ inzulín lis pro

- - - Humulin R
0 1 2
3 4 5 6


Čas (hodiny)
Graf zobrazuje relatívne množstvo glukózy v závislosti na čase potrebné na udržanie celkovej
plazmatickej glukózovej koncentrácie testovaného jedinca blízko hladinám nalačno a je indikátorom efektu týchto inzulínov na glukózový metabolizmus v závislosti na čase.
Uskutočnili sa klinické štúdie u detí (61 pacientov vo veku 2 až 11 rokov) a u detí a mladistvých (481 pacientov vo veku 9 až 19 rokov) porovnávajúce inzulín lispro a ľudský rozpustný inzulín. Farmakodynamický profil inzulínu lispro u detí je podobný ako farmakodynamický profil pozorovaný u dospelých.
Liečba s inzulínom lispro preukázala nižšie hladiny glykovaného hemoglobínu pri porovnaní s rozpustným inzulínom, pri použití subkutánnou infúznou pumpou. V dvojito zaslepenej skríženej
štúdii došlo ku zníženiu hladiny glykovaného hemoglobínu po 12 týždňoch o 0,37 percentuálnych bodov u inzulínu lispro v porovnaní s 0,03 percentuálnymi bodmi u rozpustného inzulínu (p=0,004).
Štúdie ukázali, že pridanie inzulínu lispro signifikantne znižuje hladinu HbA1C v porovnaní
so samotnou sulfonylureou u pacientov s diabetom typu 2 na maximálnych dávkach derivátov
sulfonylurey. Zníženie hladiny HbA1C možno očakávať takisto pri kombinácii s inými prípravkami inzulínu, napr. regular alebo izofán inzulínom.
Klinické štúdie s pacientami s diabetom typu 1 a 2 preukázali nižší počet nočných hypoglykémií
s inzulínom lispro v porovnaní s rozpustným ľudským inzulínom. V niektorých štúdiách bol nižší
počet nočných hypoglykémií spojený so zvýšeným počtom denných hypoglykémií.
Glukodynamická odpoveď na inzulín lispro nie je ovplyvnená poškodením funkcie obličiek alebo pečene. Glukodynamické rozdiely medzi inzulínom lispro a rozpustným ľudským inzulínom merané v priebehu glukózového clampu boli udržané v širokom spektre renálnych funkcií.
Bolo preukázané, že inzulín lispro je molárne ekvipotentný s ľudským inzulínom, ale jeho účinok
nastupuje rýchlejšie a má kratšiu dobu trvania.
5.2 Farmakokinetické vlastnosti
Farmakokinetika inzulínu lispro zodpovedá látke, ktorá sa rýchlo absorbuje a dosahuje najvyššie plazmatické hladiny v čase od 30 do 70 minút po subkutánnej injekcii. Pri zvažovaní klinickej relevancie tejto kinetiky je vhodnejšie vyšetriť krivky utilizácie glukózy (pozri 5.1).
Inzulín lispro je u pacientov s poškodením funkcie obličiek absorbovaný rýchlejšie ako rozpustný ľudský inzulín. U pacientov s diabetom typu 2 v širokom spektre renálnych funkcií boli všeobecne dodržané farmakokinetické rozdiely medzi inzulínom lispro a rozpustným inzulínom a ukázali sa nezávislými na renálnych funkciách. Inzulín lispro je u pacientov s poškodením funkcie pečene absorbovaný a eliminovaný rýchlejšie v porovnaní s rozpustným ľudským inzulínom.
5.3 Predklinické údaje o bezpečnosti
Pri testoch uskutočnených in vitro, zahŕňajúcich väzbu na inzulínové receptory a účinky na
rastúce bunky, sa inzulín lispro správal spôsobom, ktorý veľmi pripomínal ľudský inzulín. Štúdie tiež preukázali, že disociácia väzby inzulínu lispro na inzulínový receptor je totožná s ľudským inzulínom. Akútne, jeden mesiac a dvanásť mesiacov trvajúce toxikologické štúdie nepreukázali žiadne
významné toxikologické účinky.
V štúdiách na zvieratách inzulín lispro nespôsoboval poškodenie plodnosti, prejavy embryotoxicity alebo teratogenicity.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Metakrezol [3,15 mg/ml] Glycerol
Heptahydrát hydrogénfosforečnanu sodného
Oxid zinočnatý
Voda na injekciu
Kyselina chlorovodíková a hydroxid sodný môžu byť použité na úpravu pH na 7,0 - 7,8.
6.2 Inkompatibility
Prípravky Liprologu sa nesmú miešať s inzulínmi iných výrobcov alebo so zvieracími inzulínmi.
6.3 Čas použiteľnosti
Nepoužité predplnené pero
3 roky
Po prvom použití
28 dní
6.4 Špeciálne upozornenia na uchovávanie
Nepoužité predplnené pero
Uchovávajte v chladničke pri teplote (2°C – 8°C). Neuchovávajte v mrazničke. Nevystavujte
nadmernému teplu alebo priamemu slnečnému svetlu.
Po prvom použití
Uchovávajte pri teplote do 30°C. Neuchovávajte v chladničke. Predplnené pero neuchovávajte
s nasadenou ihlou.
6.5 Druh obalu a obsah balenia a špeciálne zariadenie na použitie, podanie alebo implantáciu
Roztok sa plní do náplní z kremičitého skla typu I s butylovým alebo halobutylovým diskovým uzáverom s piestom, uzávery sú zabezpečené alumíniovým tesnením. Na ošetrenie piestu a/alebo skla náplne sa môže použiť dimetikón alebo silikónová emulzia. Náplne s objemom 3 ml sú uzatvorené
v dávkovači na jednorazové použitie, ktorý sa nazýva „KwikPen“. Ihly nie sú súčasťou balenia. Nie všetky veľkosti balenia musia byť uvedené do obehu.
5 x 3 ml Liprolog 100 U/ml KwikPen perá
2 x (5 x 3 ml) Liprolog 100 U/ml KwikPen perá
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými požiadavkami.
Návod na použitie
Skontrolujte injekčný roztok Liprolog KwikPen. Má byť číry a bezfarebný. Nepoužívajte Liprolog,
pokiaľ sa javí zakalený, zahustený alebo ľahko zafarbený alebo pokiaľ sú v ňom viditeľné pevné častice.
a) Zaobchádzanie s naplneným perom
Pred použitím pera KwikPen je potrebné si starostlivo prečítať príručku pre používateľa v písomnej
informácii pre používateľa. KwikPen sa musí používať podľa odporúčaní v príručke pre používateľa.
b) Miešanie inzulínov
Nemiešajte inzulín v injekčných liekovkách s inzulínom v náplniach. Pozri časť 6.2.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Eli Lilly Nederland B.V, Grootslag 1-5, 3991 RA Houten, Holandsko
8. REGISTRAČNÉ ČÍSLA
EU/1/01/195/016 5 x 3 ml Liprolog 100 U/ml KwikPen
EU/1/01/195/017 2 x (5 x 3 ml) Liprolog 100 U/ml KwikPen
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 1. augusta 2001
Dátum posledného predĺženia: 1. augusta 2006
10. DÁTUM REVÍZIE TEXTU
1. NÁZOV LIEKU
Liprolog Mix25 100 U/ml KwikPen, injekčná suspenzia
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
2.1 Všeobecný opis
Liprolog Mix25 je biela sterilná suspenzia.
2.2 Kvalitatívne a kvantitatívne zloženie
1 ml obsahuje 100 U (zodpovedá 3,5 mg) inzulín lispro (pôvod z rekombinantnej DNA
produkovanej E.coli). Každé balenie obsahuje 3ml, čo zodpovedá 300 U inzulínu lispro. Liprolog Mix25 tvorí 25% roztok inzulínu lispro a 75% suspenzia inzulínu lispro izofán. Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčná suspenzia.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Liprolog Mix25 je určený na liečbu pacientov s diabetes mellitus, ktorí potrebujú inzulín na udržanie normálnej glukózovej homeostázy.
4.2 Dávkovanie a spôsob podávania
Dávkovanie určí lekár v súlade s potrebami pacienta.
Liprolog Mix25 sa môže podať krátko pred jedlom. V prípade potreby sa Liprolog Mix25 môže podať i bezprostredne po jedle. Liprolog Mix25 sa aplikuje len subkutánnou injekciou. Liprolog Mix25 sa nemá nikdy podať intravenózne.
Subkutánne sa má podať v hornej časti ramien, na stehnách, zadku alebo bruchu. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužilo viackrát ako približne raz za mesiac.
Pri subkutánnej aplikácii Liprologu Mix25 je potrebné sa starostlivo uistiť o tom, že nedošlo
k aplikácii do cievy. Po aplikácii sa miesto vpichu nemá masírovať. Pacient musí byť riadne poučený
o správnej aplikačnej technike.
Po subkutánnej aplikácii Liprologu Mix25 dochádza k rýchlemu nástupu účinku a skorému dosiahnutiu vrcholu aktivity Liprologu. To umožňuje podanie Liprologu Mix25 v tesnej časovej súvislosti s jedlom. Trvanie účinku zložky suspenzie inzulínu lispro izofán (Basal) Liprologu Mix25 je veľmi podobné účinku bazálneho inzulínu (NPH).
Časový priebeh aktivity akéhokoľvek inzulínu sa môže významne líšiť u rôznych osôb alebo u jednej
osoby v rôznych časových intervaloch. Rovnako ako u všetkých inzulínových prípravkov závisí trvanie účinku Liprologu Mix25 na dávke, mieste vpichu, krvnom zásobovaní, teplote a fyzickej aktivite.
4.3 Kontraindikácie
Precitlivenosť na inzulín lispro alebo na ktorúkoľvek z pomocných látok. Hypoglykémia.
4.4 Osobitné upozornenia a opatrenia pri používaní
Liprolog Mix25 sa nesmie za žiadnych okolností podať intravenózne.
Prechod pacienta na iný typ alebo značku inzulínu sa musí uskutočniť pod prísnym lekárskym dohľadom. Zmeny koncentrácie, značky (výrobcu), typu (regular, NPH, lente a i.), druhu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo spôsobu výroby (rekombinantná DNA oproti inzulínu zvieracieho pôvodu) môžu mať za následok potrebu zmeny dávkovania.
Dlhotrvajúci diabetes, intenzifikovaná inzulínová terapia, diabetická neuropatia alebo užívanie liekov, ako sú beta-blokátory, môžu zmeniť alebo zmierniť skoré varovné príznaky hypoglykémie.
Malý počet pacientov, ktorí mali hypoglykemické reakcie po prevode z inzulínu zvieracieho pôvodu na ľudský inzulín, uvádzalo, že skoré varovné príznaky hypoglykémie boli menej výrazné alebo odlišné od tých, ktoré zažili pri použití predchádzajúceho inzulínu. Nekontrolované hypoglykemické alebo hyperglykemické reakcie môžu spôsobiť stratu vedomia, kómu alebo smrť.
Použitie nedostatočných dávok alebo prerušenie liečby, najmä u inzulín-dependentných diabetikov,
môže viesť k hyperglykémii a diabetickej ketoacidóze; stavom, ktoré môžu byť letálne.
Potreba inzulínu môže byť znížená pri poškodení funkcie obličiek. Potreba inzulínu môže byť znížená u pacientov s poškodením funkcie pečene z dôvodov nižšej kapacity pre glukoneogenézu a zhoršeného odbúravania inzulínu; avšak u pacientov s chronickým poškodením funkcie pečene môže zvýšenie inzulínovej rezistencie viesť ku vyššej potrebe inzulínu.
Potreba inzulínu sa môže zvýšiť počas ochorenia alebo vplyvom emocionálnych stresov.
Úprava dávky môže byť rovnako potrebná, pokiaľ pacienti vykonávajú zvýšenú fyzickú aktivitu alebo menia svoju zvyčajnú diétu. Cvičenie ihneď po požití potravy môže zvýšiť riziko hypoglykémie.
Podanie inzulínu lispro deťom mladším ako 12 rokov sa má zvážiť iba v prípade očakávaného prínosu
v porovnaní s regular inzulínom.
Kombinácia Liprologu Mix25 a pioglitazónu
V prípadoch, keď sa použil pioglitazón v kombinácii s inzulínom, boli zaznamenané prípady srdcového zlyhania, najmä u pacientov s rizikovými faktormi pre vznik srdcového zlyhania. Treba
mať na zreteli tieto fakty v prípade, že sa zvažuje liečba kombináciou pioglitazónu a Liprologu Mix25. Ak pacient používa danú kombináciu, je u neho potrebné sledovať znaky a symptómy srdcového zlyhania, priberanie na hmotnosti a edém. Ak sa zistí akékoľvek zhoršenie srdcových symptómov, pioglitazón sa musí prestať podávať.
4.5 Liekové a iné interakcie
Potreba inzulínu sa môže zvýšiť látkami s hyperglykemickým účinkom, ako je
perorálna antikoncepcia, kortikosteroidy alebo hormonálna substitúcia počas liečby porúch štítnej žľazy, danazol, beta2-mimetiká (ritodrín, salbutamol, terbutalín).
Potreba inzulínu sa môže znížiť pri podávaní liekov s hypoglykemickým účinkom ako sú perorálne antidiabetiká, salicyláty (napr. kyselina acetylosalicylová), sulfónamidy, niektoré antidepresíva (inhibítory monoaminooxidázy, selektívne inhibítory spätného vychytávania sérotonínu), niektoré
inhibítory angiotenzín konvertujúceho enzýmu (kaptopril, enalapril), blokátory receptorov angiotenzínu II, beta-blokátory, oktreotid alebo alkohol.
Miešanie Liprologu Mix25 s inými inzulínmi sa neskúmalo.
Užívanie iných liekov podávaných súčasne s Liprologom Mix25 KwikPen sa má konzultovať
s lekárom (pozri časť 4.4).
4.6 Fertilita, gravidita a laktácia
Údaje o veľkom počte gravidných žien užívajúcich inzulín lispro nepreukázali žiadne nežiaduce
účinky na graviditu alebo na zdravie plodu/novorodenca.
Udržanie dobrej kontroly glykémie počas gravidity je základnou požiadavkou liečby diabetu
u pacientky liečenej inzulínom pri inzulín-dependentnom alebo gestačnom diabete. Potreba inzulínu sa
zvyčajne znižuje počas prvého trimestra a zvyšuje počas druhého a tretieho trimestra. Pacientky s diabetom majú byť poučené o tom, aby informovali svojho lekára v prípade gravidity alebo ak graviditu zvažujú. Starostlivé monitorovanie glykémie, rovnako ako aj celkového zdravotného stavu, je základnou požiadavkou u gravidných s diabetom.
U dojčiacich diabetičiek môže vzniknúť potreba úpravy dávky inzulínu, diéty alebo oboje.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta koncentrovať sa a reagovať môže byť porušená v dôsledku hypoglykémie. To môže byť riskantné v situáciách špeciálne vyžadujúcich vyššie uvedené schopnosti (napr. vedenie auta alebo obsluha strojov).
Pacient má byť poučený o potrebe zabrániť hypoglykémii počas vedenia vozidla, čo je obzvlášť dôležité u tých osôb, ktoré majú zníženú alebo chýbajúcu vnímavosť varovných príznakov hypoglykémie alebo majú časté hypoglykemické epizódy. Za týchto okolností sa musí starostlivo zvážiť vhodnosť vedenia vozidiel.
4.8 Nežiaduce účinky
Najčastejším nežiaducim účinkom inzulínovej terapie u pacienta s diabetom je hypoglykémia. Závažná hypoglykémia môže viesť ku strate vedomia a v extrémnych prípadoch ku smrti. Frekvencia výskytu hypoglykémie nie je uvedená, pretože hypoglykémia je výsledkom pôsobenia nielen dávky inzulínu ale aj iných faktorov, napr. diéta pacienta a fyzická aktivita.
Často (1/100 až <1/10) sa u pacientov objavuje lokálna precitlivenosť. V mieste aplikácie inzulínu sa môže vyskytnúť začervenanie, opuch a svrbenie. Tento stav obvykle ustúpi počas niekoľkých dní alebo týždňov. V niektorých prípadoch môže byť tento stav zapríčinený inými faktormi ako inzulínom, napríklad iritáciou kože dezinfekčným prostriedkom alebo nesprávnou injekčnou technikou. Systémová alergia, ktorá je zriedkavá (1/10 000 až <1/1 000), ale potenciálne závažnejšia,
je generalizovanou alergiou na inzulín. Môže spôsobiť vyrážky po celom tele, dýchavičnosť, pískanie, pokles krvného tlaku, zrýchlený pulz alebo potenie. Ťažké stavy generalizovanej alergie môžu ohrozovať život.
Lipodystrofia v mieste aplikácie injekcie je menej častá (1/1 000 až <1/100).
Prípady edémov počas inzulínovej liečby boli hlásené najmä vtedy, keď v dôsledku intenzívnejšej inzulinoterapie došlo k zlepšeniu predchádzajúcej zlej metabolickej kompenzácie.
Hlásenie podozrení na nežiaduce reakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné
monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili

akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.4.9 PredávkovanieInzulín nemá špecifickú definíciu predávkovania, pretože koncentrácia glukózy v sére je výsledkom komplexných interakcií medzi hladinou inzulínu, dostupnosťou glukózy a ostatnými metabolickými procesmi. Hypoglykémia sa môže objaviť ako dôsledok nadbytku inzulínovej aktivity v pomere
k príjmu potravy a výdaju energie.
Hypoglykémia môže byť spojená s nevšímavosťou, zmätenosťou, palpitáciami, bolesťami hlavy,
potením a vracaním.
Mierne epizódy hypoglykémie reagujú na perorálne podanie glukózy, iného cukru, príp. produktu obsahujúceho sacharidy.
Korekcia stredne ťažkej hypoglykémie sa môže uskutočniť intramuskulárnou alebo subkutánnou aplikáciou glukagónu a následným perorálnym podaním sacharidov, pokiaľ sa pacient dostatočne zotaví. Pacienti, ktorí nereagujú na glukagón, musia dostať infúziu glukózy intravenózne.
Pokiaľ je pacient v kóme, glukagón sa má aplikovať intramuskulárne alebo subkutánne. Pokiaľ však glukagón nie je k dispozícii alebo pacient na jeho podanie nereaguje, musí sa podať roztok glukózy intravenózne. Akonáhle sa pacient preberie z bezvedomia, musí sa najesť.
Po zdanlivej úprave klinického stavu môže byť potrebný trvalý príjem sacharidov a sledovanie
pacienta, pretože hypoglykémia sa môže opakovať.
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Inzulíny a ich analógy, strednodobo pôsobiace v kombinácii s rýchlopôsobiacimi inzulínmi, ATC kód: A10A D04
Liprolog Mix25 je vopred namiešaná suspenzia obsahujúca inzulín lispro (rýchlopôsobiaci analóg
ľudského inzulínu) a inzulín lispro izofán (strednodobo pôsobiaci analóg ľudského inzulínu).
Primárnym účinkom inzulínu lispro je regulácia glukózového metabolizmu.
Inzulín má navyše ďalšie anabolické a anti-katabolické vlastnosti na mnoho rôznych tkanív.
V svalovom tkanive tieto účinky zahŕňajú zvýšenie syntézy glykogénu, mastných kyselín, glycerolu a proteínov a vychytávanie aminokyselín a zároveň zníženie glykogenolýzy, glukoneogenézy, ketogenézy, lipolýzy, proteínového katabolizmu a tvorby aminokyselín.
Rýchly nástup účinku inzulínu lispro (približne 15 minút) umožňuje jeho podanie v tesnej časovej
súvislosti s jedlom (v rozmedzí 0 až 15 minút pred jedlom) v porovnaní s regular inzulínom
(30 až 45 minút pred jedlom). Po subkutánnej aplikácii Liprologu Mix25 dochádza k rýchlemu nástupu účinku a skorému dosiahnutiu vrcholu aktivity inzulínu lispro. Profil účinku Liprologu Basal je veľmi podobný účinku bazálneho inzulínu (NPH) a pretrváva počas približne 15 hodín.
Klinické štúdie u pacientov s diabetom typu 1 alebo 2 preukázali nižší výskyt postprandiálnej hyperglykémie u Liprologu Mix25 v porovnaní so zmesou 30/70 ľudského inzulínu. V jednej klinickej štúdii bolo pozorované malé zvýšenie (0,38 mmol/l) hladín glukózy v noci (o 3. hodine ráno).
Na nasledujúcom obrázku je zobrazená farmakodynamika Liprologu Mix25 a Liprologu Basal.

Humalog Mix25

NPL
Hypoglykemická
aktivita

0 4 8 12 16 20 24
Čas, hodiny
Graf zobrazuje relatívne množstvo glukózy v závislosti na čase potrebné na udržanie celkovej plazmatickej glukózovej koncentrácie testovaného jedinca blízko hladinám nalačno a je indikátorom efektu týchto inzulínov na glukózový metabolizmus v závislosti na čase.
Glukodynamická odpoveď na inzulín lispro nie je ovplyvnená poškodením funkcie pečene alebo obličiek. Glukodynamické rozdiely medzi inzulínom lispro a rozpustným ľudským inzulínom merané v priebehu glukózového clampu boli udržané v širokom spektre renálnych funkcií.
Bolo preukázané, že inzulín lispro je molárne ekvipotentný s ľudským inzulínom, ale jeho účinok
nastupuje rýchlejšie a má kratšiu dobu trvania.
V dvoch 8-mesačných otvorených prekrížených štúdiách pacienti s diabetom 2. typu, ktorí doteraz neboli liečení inzulínom, alebo si už aplikovali inzulín jeden alebo dvakrát denne, boli v náhodnom poradí 4 mesiace liečení Liprologom Mix25 (užívaným dvakrát denne s metformínom) a inzulínom glargin (užívaným jedenkrát denne s metformínom). Detailné informácie môžete nájsť v nasledujúcej tabuľke.
| Pacienti doteraz neliečení
inzulínom n=78
| Pacienti už predtým liečení
inzulínom n=97
| Priemerná celková dávka
inzulínu pri ukončení liečby
| 0,63 U/kg
| 0,42 U/kg
| Redukcia hemoglobínu A1c1
| 1,30% (priemerná východisková hodnota = 8,7%)
| 1,00% (priemerná východisková hodnota = 8,5%)
| Redukcia priemernej
kombinovanej rannej /večernej
2 hodinovej postprandiálnej glykémie1
| 3,46 mM
| 2,48 mM
| Redukcia priemernej glykémie
nalačno1
| 0,55 mM
| 0,65 mM
| Výskyt hypoglykémií pri
ukončení liečby
| 25%
| 25%
| Hmotnostný prírastok2
| 2,33 kg
| 0,96 kg
|
|
|
1 od východiskového stavu po ukončenie liečby Liprologom Mix25
2 u pacientov randomizovaných na Liprolog Mix25 v priebehu prvej fázy prekríženej liečby
5.2 Farmakokinetické vlastnosti
Podľa farmakokinetických vlastností je inzulín lispro zlúčenina, ktorá sa rýchlo vstrebáva a dosahuje maximálne hladiny v krvi 30 až 70 minút po subkutánnom podaní. Farmakokinetika suspenzie inzulínu lispro izofán je zhodná so strednodobo pôsobiacimi inzulínmi ako je NPH. Farmakokinetika Liprologu Mix25 reprezentuje individuálne farmakokinetické vlastnosti jeho dvoch zložiek. Ak vezmeme do úvahy klinický význam týchto kinetík, je vhodnejšie vyšetriť krivky utilizácie glukózy. (pozri časť 5.1).
Inzulín lispro je u pacientov s renálnou insuficienciou absorbovaný rýchlejšie ako rozpustný ľudský inzulín. U pacientov s diabetom typu 2 v celom širokom spektre renálnych funkcií boli farmakokinetické diferencie medzi inzulínom lispro a rozpustným ľudským inzulínom všeobecne udržané a ukázali sa nezávislými na renálnych funkciách. Inzulín lispro je u pacientov s poškodenou funkciou pečene absorbovaný a eliminovaný rýchlejšie v porovnaní s rozpustným ľudským inzulínom.
5.3 Predklinické údaje o bezpečnosti
Pri testoch uskutočnených in vitro zahŕňajúcich väzbu na inzulínové receptory a účinky na rastúce bunky, sa inzulín lispro správal spôsobom, ktorý veľmi pripomínal ľudský inzulín. Štúdie tiež preukázali, že disociácia väzby inzulínu lispro na inzulínový receptor je totožná s ľudským inzulínom. Akútne, jeden mesiac a dvanásť mesiacov trvajúce toxikologické štúdie nepreukázali žiadne
významné toxikologické účinky.
V štúdiách na zvieratách inzulín lispro nespôsoboval poškodenie plodnosti, prejavy embryotoxicity alebo teratogenicity.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Protamíniumsulfát Metakrezol[1,76 mg/ml] Fenol [0,80 mg/ml] Glycerol
Heptahydrát hydrogénfosforečnanu sodného
Oxid zinočnatý
Voda na injekciu
Kyselina chlorovodíková a hydroxid sodný môžu byť použité na úpravu pH na 7,0 - 7,8.
6.2 Inkompatibility
Miešanie Liprologu Mix25 s inými inzulínmi sa neskúmalo. Pre nedostatok štúdií kompatibility
nesmie byť tento liek miešaný s inými liekmi.'
6.3 Čas použiteľnosti
Nepoužité predplnené pero
3 roky
Po prvom použití
28 dní
6.4 Špeciálne upozornenia na uchovávanie
Nepoužité predplnené pero
Uchovávajte v chladničke pri teplote (2°C – 8°C). Neuchovávajte v mrazničke. Nevystavujte
nadmernému teplu alebo priamemu slnečnému svetlu.
Po prvom použití
Uchovávajte pri teplote do 30°C. Neuchovávajte v mrazničke. Predplnené pero neuchovávajte
s nasadenou ihlou.
6.5 Druh obalu a obsah balenia a špeciálne zariadenie na použitie, podanie alebo implantáciu
Suspenzia sa plní do náplní z kremičitého skla typu I, ktoré sú utesnené halobutylovým diskovým uzáverom s piestom a zabezpečené alumíniovým tesnením. Na ošetrenie piestu a/alebo skla náplne sa môže použiť dimetikón alebo silikónová emulzia. Náplne s objemom 3 ml sú uzatvorené v naplnenom dávkovači na jednorazové použitie, nazývanom aj “KwikPen”. Ihly nie sú súčasťou balenia.
Nie všetky veľkosti balenia musia byť uvedené do obehu.
5 x 3 ml Liprolog Mix25 100U/ml KwikPen.
2 x (5 x 3 ml) Liprolog Mix25 100U/ml KwikPen.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými požiadavkami.
Návod na použitie
Bezprostredne pred použitím sa pero KwikPen desaťkrát premieša prevaľovaním v dlaniach
a desaťkrát prevráti o 180° z dôvodu premiešania inzulínu, pokiaľ sa nedocieli rovnomerný zákal
alebo mliečne zafarbenie. Pokiaľ sa tak nestane, je potrebné opakovať vyššie uvedený postup, až sa
obsah nepremieša. Náplne obsahujú malú sklenenú guľôčku uľahčujúcu miešanie. Netraste rázne, pretože to môže spôsobiť spenenie, ktoré by mohlo ovplyvniť správne dávkovanie.
Náplne sa majú často kontrolovať a nesmú sa použiť, pokiaľ inzulín tvorí zhluky alebo pokiaľ pevné biele častice ostávajú na dne alebo na stene náplne, ktorá tým získava matný vzhľad.
Zaobchádzanie s naplneným perom
Pred použitím pera KwikPen je potrebné si starostlivo prečítať príručku pre používateľa v písomnej
informácii pre používateľa. KwikPen sa musí používať podľa odporúčaní v príručke pre používateľa.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Eli Lilly Nederland B.V., Grootslag 1-5, 3991 RA Houten, Holandsko.
8. REGISTRAČNÉ ČÍSLA
EU/1/01/195/018 5 x 3 ml Liprolog Mix25 100 U/ml KwikPen
EU/1/01/195/019 2 x (5 x 3 ml) Liprolog Mix25 100 U/ml KwikPen
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 1. augusta 2001
Dátum posledného predĺženia: 1. augusta 2006
10. DÁTUM REVÍZIE TEXTU
1. NÁZOV LIEKU
Liprolog Mix50 100 U/ml KwikPen, injekčná suspenzia
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
2.1 Všeobecný opis
Liprolog Mix50 je biela sterilná suspenzia.
2.2 Kvalitatívne a kvantitatívne zloženie
1 ml obsahuje 100 U (zodpovedá 3,5 mg) inzulín lispro (pôvod z rekombinantnej DNA
produkovanej E.coli). Každé balenie obsahuje 3ml, čo zodpovedá 300 U inzulínu lispro. Liprolog Mix50 tvorí 50% roztok inzulínu lispro a 50% suspenzia inzulínu lispro izofán. Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčná suspenzia.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Liprolog Mix50 je určený na liečbu pacientov s diabetes mellitus, ktorí potrebujú inzulín na udržanie normálnej glukózovej homeostázy.
4.2 Dávkovanie a spôsob podávania
Dávkovanie určí lekár v súlade s potrebami pacienta.
Liprolog Mix50 sa môže podať krátko pred jedlom. V prípade potreby sa Liprolog Mix50 môže podať i bezprostredne po jedle. Liprolog Mix50 sa aplikuje len subkutánnou injekciou. Liprolog Mix50 sa nemá nikdy podať intravenózne.
Subkutánne sa má podať v hornej časti ramien, na stehnách, zadku alebo bruchu. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužilo viackrát ako približne raz za mesiac.
Pri subkutánnej aplikácii Liprologu Mix50 je potrebné sa starostlivo uistiť o tom, že nedošlo
k aplikácii do cievy. Po aplikácii sa miesto vpichu nemá masírovať. Pacient musí byť riadne poučený
o správnej aplikačnej technike.
Po subkutánnej aplikácii Liprologu Mix50 dochádza k rýchlemu nástupu účinku a skorému dosiahnutiu vrcholu aktivity Liprologu. To umožňuje podanie Liprologu Mix50 v tesnej časovej súvislosti s jedlom. Trvanie účinku zložky suspenzie inzulínu lispro izofán (Basal) Liprologu Mix50 je veľmi podobné účinku bazálneho inzulínu (NPH).
Časový priebeh aktivity akéhokoľvek inzulínu sa môže významne líšiť u rôznych osôb alebo u jednej
osoby v rôznych časových intervaloch. Rovnako ako u všetkých inzulínových prípravkov závisí trvanie účinku Liprologu Mix50 na dávke, mieste vpichu, krvnom zásobovaní, teplote a fyzickej aktivite.
4.3 Kontraindikácie
Precitlivenosť na inzulín lispro alebo na ktorúkoľvek z pomocných látok. Hypoglykémia.
4.4 Osobitné upozornenia a opatrenia pri používaní
Liprolog Mix50 sa nesmie za žiadnych okolností podať intravenózne.
Prechod pacienta na iný typ alebo značku inzulínu sa musí uskutočniť pod prísnym lekárskym dohľadom. Zmeny koncentrácie, značky (výrobcu), typu (regular, NPH, lente a i.), druhu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo spôsobu výroby (rekombinantná DNA oproti inzulínu zvieracieho pôvodu) môžu mať za následok potrebu zmeny dávkovania.
Dlhotrvajúci diabetes, intenzifikovaná inzulínová terapia, diabetická neuropatia alebo užívanie liekov, ako sú beta-blokátory, môžu zmeniť alebo zmierniť skoré varovné príznaky hypoglykémie.
Malý počet pacientov, ktorí mali hypoglykemické reakcie po prevode z inzulínu zvieracieho pôvodu na ľudský inzulín, uvádzalo, že skoré varovné príznaky hypoglykémie boli menej výrazné alebo odlišné od tých, ktoré zažili pri použití predchádzajúceho inzulínu. Nekontrolované hypoglykemické alebo hyperglykemické reakcie môžu spôsobiť stratu vedomia, kómu alebo smrť.
Použitie nedostatočných dávok alebo prerušenie liečby, najmä u inzulín-dependentných diabetikov,
môže viesť k hyperglykémii a diabetickej ketoacidóze; stavom, ktoré môžu byť letálne.
Potreba inzulínu môže byť znížená pri poškodení funkcie obličiek. Potreba inzulínu môže byť znížená u pacientov s poškodením funkcie pečene z dôvodov nižšej kapacity pre glukoneogenézu a zhoršeného odbúravania inzulínu; avšak u pacientov s chronickým poškodením funkcie pečene môže zvýšenie inzulínovej rezistencie viesť ku vyššej potrebe inzulínu.
Potreba inzulínu sa môže zvýšiť počas ochorenia alebo vplyvom emocionálnych stresov.
Úprava dávky môže byť rovnako potrebná, pokiaľ pacienti vykonávajú zvýšenú fyzickú aktivitu alebo menia svoju zvyčajnú diétu. Cvičenie ihneď po požití potravy môže zvýšiť riziko hypoglykémie.
Podanie inzulínu lispro deťom mladším ako 12 rokov sa má zvážiť iba v prípade očakávaného prínosu
v porovnaní s regular inzulínom.
Kombinácia Liprologu Mix50 a pioglitazónu
V prípadoch, keď sa použil pioglitazón v kombinácii s inzulínom, boli zaznamenané prípady srdcového zlyhania, najmä u pacientov s rizikovými faktormi pre vznik srdcového zlyhania. Treba
mať na zreteli tieto fakty v prípade, že sa zvažuje liečba kombináciou pioglitazónu a Liprologu Mix50. Ak pacient používa danú kombináciu, je u neho potrebné sledovať znaky a symptómy srdcového zlyhania, priberanie na hmotnosti a edém. Ak sa zistí akékoľvek zhoršenie srdcových symptómov, pioglitazón sa musí prestať podávať.
4.5 Liekové a iné interakcie
Potreba inzulínu sa môže zvýšiť látkami s hyperglykemickým účinkom, ako je
perorálna antikoncepcia, kortikosteroidy alebo hormonálna substitúcia počas liečby porúch štítnej žľazy, danazol, beta2-mimetiká (ritodrín, salbutamol, terbutalín).
Potreba inzulínu sa môže znížiť pri podávaní liekov s hypoglykemickým účinkom ako sú perorálne antidiabetiká, salicyláty (napr. kyselina acetylosalicylová), sulfónamidy, niektoré antidepresíva (inhibítory monoaminooxidázy, selektívne inhibítory spätného vychytávania sérotonínu), niektoré
inhibítory angiotenzín konvertujúceho enzýmu (kaptopril, enalapril), blokátory receptorov angiotenzínu II, beta-blokátory, oktreotid alebo alkohol.
Miešanie Liprologu Mix50 s inými inzulínmi sa neskúmalo.
Užívanie iných liekov podávaných súčasne s Liprologom Mix50 KwikPen sa má konzultovať
s lekárom (pozri časť 4.4).
4.6 Fertilita, gravidita a laktácia
Údaje o veľkom počte gravidných žien užívajúcich inzulín lispro nepreukázali žiadne nežiaduce
účinky na graviditu alebo na zdravie plodu/novorodenca.
Udržanie dobrej kontroly glykémie počas gravidity je základnou požiadavkou liečby diabetu
u pacientky liečenej inzulínom pri inzulín-dependentnom alebo gestačnom diabete. Potreba inzulínu sa
zvyčajne znižuje počas prvého trimestra a zvyšuje počas druhého a tretieho trimestra. Pacientky s diabetom majú byť poučené o tom, aby informovali svojho lekára v prípade gravidity alebo ak graviditu zvažujú. Starostlivé monitorovanie glykémie, rovnako ako aj celkového zdravotného stavu, je základnou požiadavkou u gravidných s diabetom.
U dojčiacich diabetičiek môže vzniknúť potreba úpravy dávky inzulínu, diéty alebo oboje.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta koncentrovať sa a reagovať môže byť porušená v dôsledku hypoglykémie. To môže byť riskantné v situáciách špeciálne vyžadujúcich vyššie uvedené schopnosti (napr. vedenie auta alebo obsluha strojov).
Pacient má byť poučený o potrebe zabrániť hypoglykémii počas vedenia vozidla, čo je obzvlášť dôležité u tých osôb, ktoré majú zníženú alebo chýbajúcu vnímavosť varovných príznakov hypoglykémie alebo majú časté hypoglykemické epizódy. Za týchto okolností sa musí starostlivo zvážiť vhodnosť vedenia vozidiel.
4.8 Nežiaduce účinky
Najčastejším nežiaducim účinkom inzulínovej terapie u pacienta s diabetom je hypoglykémia. Závažná hypoglykémia môže viesť ku strate vedomia a v extrémnych prípadoch ku smrti. Frekvencia výskytu hypoglykémie nie je uvedená, pretože hypoglykémia je výsledkom pôsobenia nielen dávky inzulínu ale aj iných faktorov, napr. diéta pacienta a fyzická aktivita.
Často (1/100 až <1/10) sa u pacientov objavuje lokálna precitlivenosť. V mieste aplikácie inzulínu sa môže vyskytnúť začervenanie, opuch a svrbenie. Tento stav obvykle ustúpi počas niekoľkých dní alebo týždňov. V niektorých prípadoch môže byť tento stav zapríčinený inými faktormi ako inzulínom, napríklad iritáciou kože dezinfekčným prostriedkom alebo nesprávnou injekčnou technikou. Systémová alergia, ktorá je zriedkavá (1/10 000 až <1/1 000), ale potenciálne závažnejšia,
je generalizovanou alergiou na inzulín. Môže spôsobiť vyrážky po celom tele, dýchavičnosť, pískanie, pokles krvného tlaku, zrýchlený pulz alebo potenie. Ťažké stavy generalizovanej alergie môžu ohrozovať život.
Lipodystrofia v mieste aplikácie injekcie je menej častá (1/1 000 až <1/100).
Prípady edémov počas inzulínovej liečby boli hlásené najmä vtedy, keď v dôsledku intenzívnejšej inzulinoterapie došlo k zlepšeniu predchádzajúcej zlej metabolickej kompenzácie.
Hlásenie podozrení na nežiaduce reakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné
monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili

akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.4.9 PredávkovanieInzulín nemá špecifickú definíciu predávkovania, pretože koncentrácia glukózy v sére je výsledkom komplexných interakcií medzi hladinou inzulínu, dostupnosťou glukózy a ostatnými metabolickými procesmi. Hypoglykémia sa môže objaviť ako dôsledok nadbytku inzulínovej aktivity v pomere
k príjmu potravy a výdaju energie.
Hypoglykémia môže byť spojená s nevšímavosťou, zmätenosťou, palpitáciami, bolesťami hlavy,
potením a vracaním.
Mierne epizódy hypoglykémie reagujú na perorálne podanie glukózy, iného cukru, príp. produktu obsahujúceho sacharidy.
Korekcia stredne ťažkej hypoglykémie sa môže uskutočniť intramuskulárnou alebo subkutánnou aplikáciou glukagónu a následným perorálnym podaním sacharidov, pokiaľ sa pacient dostatočne zotaví. Pacienti, ktorí nereagujú na glukagón, musia dostať infúziu glukózy intravenózne.
Pokiaľ je pacient v kóme, glukagón sa má aplikovať intramuskulárne alebo subkutánne. Pokiaľ však glukagón nie je k dispozícii alebo pacient na jeho podanie nereaguje, musí sa podať roztok glukózy intravenózne. Akonáhle sa pacient preberie z bezvedomia, musí sa najesť.
Po zdanlivej úprave klinického stavu môže byť potrebný trvalý príjem sacharidov a sledovanie
pacienta, pretože hypoglykémia sa môže opakovať.
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Inzulíny a ich analógy, strednodobo pôsobiace v kombinácii s rýchlopôsobiacimi inzulínmi, ATC kód: A10A D04
Liprolog Mix50 je vopred namiešaná suspenzia obsahujúca inzulín lispro (rýchlopôsobiaci analóg
ľudského inzulínu) a inzulín lispro izofán (strednodobo pôsobiaci analóg ľudského inzulínu). Primárnym účinkom inzulínu lispro je regulácia glukózového metabolizmu.
Inzulín má navyše ďalšie anabolické a anti-katabolické vlastnosti na mnoho rôznych tkanív.
V svalovom tkanive tieto účinky zahŕňajú zvýšenie syntézy glykogénu, mastných kyselín, glycerolu a proteínov a vychytávanie aminokyselín a zároveň zníženie glykogenolýzy, glukoneogenézy, ketogenézy, lipolýzy, proteínového katabolizmu a tvorby aminokyselín.
Rýchly nástup účinku inzulínu lispro (približne 15 minút) umožňuje jeho podanie v tesnej časovej
súvislosti s jedlom (v rozmedzí 0 až 15 minút pred jedlom) v porovnaní s regular inzulínom
(30 až 45 minút pred jedlom). Po subkutánnej aplikácii Liprologu Mix50 dochádza k rýchlemu nástupu účinku a skorému dosiahnutiu vrcholu aktivity inzulínu lispro. Profil účinku Liprologu Basal je veľmi podobný účinku bazálneho inzulínu (NPH) a pretrváva počas približne 15 hodín. Na nasledujúcom obrázku je zobrazená farmakodynamika Liprologu Mix50 a Liprologu Basal.
Humalog Mix50

NPL
Hypoglykemická
aktivita
0 4 8 12 16 20 24
Čas, hodiny
Graf zobrazuje relatívne množstvo glukózy v závislosti na čase potrebné na udržanie celkovej plazmatickej glukózovej koncentrácie testovaného jedinca blízko hladinám nalačno a je indikátorom efektu týchto inzulínov na glukózový metabolizmus v závislosti na čase.
Glukodynamická odpoveď na inzulín lispro nie je ovplyvnená poškodením funkcie pečene alebo obličiek. Glukodynamické rozdiely medzi inzulínom lispro a rozpustným ľudským inzulínom merané v priebehu glukózového clampu boli udržané v širokom spektre renálnych funkcií.
Bolo preukázané, že inzulín lispro je molárne ekvipotentný s ľudským inzulínom, ale jeho účinok
nastupuje rýchlejšie a má kratšiu dobu trvania.
5.2 Farmakokinetické vlastnostiPodľa farmakokinetických vlastností je inzulín lispro zlúčenina, ktorá sa rýchlo vstrebáva a dosahuje maximálne hladiny v krvi 30 až 70 minút po subkutánnom podaní. Farmakokinetika suspenzie inzulínu lispro izofán je zhodná so strednodobo pôsobiacimi inzulínmi ako je NPH. Farmakokinetika Liprologu Mix50 reprezentuje individuálne farmakokinetické vlastnosti jeho dvoch zložiek. Ak vezmeme do úvahy klinický význam týchto kinetík, je vhodnejšie vyšetriť krivky utilizácie glukózy. (pozri časť 5.1).
Inzulín lispro je u pacientov s renálnou insuficienciou absorbovaný rýchlejšie ako rozpustný ľudský inzulín. U pacientov s diabetom typu 2 v celom širokom spektre renálnych funkcií boli farmakokinetické diferencie medzi inzulínom lispro a rozpustným ľudským inzulínom všeobecne udržané a ukázali sa nezávislými na renálnych funkciách. Inzulín lispro je u pacientov s poškodenou funkciou pečene absorbovaný a eliminovaný rýchlejšie v porovnaní s rozpustným ľudským inzulínom.
5.3 Predklinické údaje o bezpečnostiPri testoch uskutočnených
in vitro zahŕňajúcich väzbu na inzulínové receptory a účinky na rastúce bunky, sa inzulín lispro správal spôsobom, ktorý veľmi pripomínal ľudský inzulín. Štúdie tiež preukázali, že disociácia väzby inzulínu lispro na inzulínový receptor je totožná s ľudským inzulínom. Akútne, jeden mesiac a dvanásť mesiacov trvajúce toxikologické štúdie nepreukázali žiadne
významné toxikologické účinky.
V štúdiách na zvieratách inzulín lispro nespôsoboval poškodenie plodnosti, prejavy embryotoxicity alebo teratogenicity.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Protamíniumsulfát Metakrezol[2,20 mg/ml] Fenol [1,00 mg/ml] Glycerol
Heptahydrát hydrogénfosforečnanu sodného
Oxid zinočnatý
Voda na injekciu
Kyselina chlorovodíková a hydroxid sodný môžu byť použité na úpravu pH na 7,0 - 7,8.
6.2 Inkompatibility
Miešanie Liprologu Mix50 s inými inzulínmi sa neskúmalo. Pre nedostatok štúdií kompatibility
nesmie byť tento liek miešaný s inými liekmi.
6.3 Čas použiteľnosti
Nepoužité predplnené pero
3 roky
Po prvom použití
28 dní
6.4 Špeciálne upozornenia na uchovávanie
Nepoužité predplnené pero
Uchovávajte v chladničke pri teplote (2°C – 8°C). Neuchovávajte v mrazničke. Nevystavujte
nadmernému teplu alebo priamemu slnečnému svetlu.
Po prvom použití
Uchovávajte pri teplote do 30°C. Neuchovávajte v mrazničke. Predplnené pero neuchovávajte
s nasadenou ihlou.
6.5 Druh obalu a obsah balenia a špeciálne zariadenie na použitie, podanie alebo implantáciu
Suspenzia sa plní do náplní z kremičitého skla typu I, ktoré sú utesnené halobutylovým diskovým uzáverom s piestom a zabezpečené alumíniovým tesnením. Na ošetrenie piestu a/alebo skla náplne sa môže použiť dimetikón alebo silikónová emulzia. Náplne s objemom 3 ml sú uzatvorené v naplnenom dávkovači na jednorazové použitie, nazývanom aj “KwikPen”. Ihly nie sú súčasťou balenia.
Nie všetky veľkosti balenia musia byť uvedené do obehu.
5 x 3 ml Liprolog Mix50 100U/ml KwikPen.
2 x (5 x 3 ml) Liprolog Mix50 100U/ml KwikPen.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými požiadavkami.
Návod na použitie
Bezprostredne pred použitím sa pero KwikPen desaťkrát premieša prevaľovaním v dlaniach
a desaťkrát prevráti o 180° z dôvodu premiešania inzulínu, pokiaľ sa nedocieli rovnomerný zákal
alebo mliečne zafarbenie. Pokiaľ sa tak nestane, je potrebné opakovať vyššie uvedený postup, až sa obsah nepremieša. Náplne obsahujú malú sklenenú guľôčku uľahčujúcu miešanie. Netraste rázne, pretože to môže spôsobiť spenenie, ktoré by mohlo ovplyvniť správne dávkovanie.
Náplne sa majú často kontrolovať a nesmú sa použiť, pokiaľ inzulín tvorí zhluky alebo pokiaľ pevné biele častice ostávajú na dne alebo na stene náplne, ktorá tým získava matný vzhľad.
Zaobchádzanie s naplneným perom
Pred použitím pera KwikPen je potrebné si starostlivo prečítať príručku pre používateľa v písomnej
informácii pre používateľa. KwikPen sa musí používať podľa odporúčaní v príručke pre používateľa.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Eli Lilly Nederland B.V., Grootslag 1-5, 3991 RA Houten, Holandsko.
8. REGISTRAČNÉ ČÍSLA
EU/1/01/195/020 5 x 3 ml Liprolog Mix50 100 U/ml KwikPen
EU/1/01/195/021 2 x (5 x 3 ml) Liprolog Mix50 100 U/ml KwikPen
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 1. augusta 2001
Dátum posledného predĺženia: 1. augusta 2006
10. DÁTUM REVÍZIE TEXTU
1. NÁZOV LIEKU
Liprolog Basal 100 U/ml KwikPen, injekčná suspenzia
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
2.1 Všeobecný opis
Liprolog Basal je biela sterilná suspenzia.
2.2 Kvalitatívne a kvantitatívne zloženie
1 ml obsahuje 100 U (zodpovedá 3,5 mg) inzulínu lispro (pôvod z rekombinantnej DNA
produkovanej E.coli). Každé balenie obsahuje 3 ml, čo zodpovedá 300 U inzulínu lispro. Liprolog Basal tvorí suspenzia inzulínu lispro izofán.
Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčná suspenzia.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Liprolog Basal je určený na liečbu pacientov s diabetes mellitus, ktorí potrebujú inzulín na udržanie normálnej glukózovej homeostázy.
4.2 Dávkovanie a spôsob podávania
Dávkovanie určí lekár v súlade s potrebami pacienta.
Liprolog Basal sa môže miešať alebo podávať spolu s Liprologom. Liprolog Basal sa má aplikovať iba subkutánnou injekciou. Liprolog Basal sa nemá nikdy podať intravenózne.
Subkutánne sa má podať v hornej časti ramien, na stehnách, zadku alebo bruchu . Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužilo viackrát ako približne raz za mesiac.
Pri subkutánnej aplikácii Liprologu Basal je potrebné sa starostlivo uistiť o tom, že nedošlo k aplikácii do cievy. Po aplikácii sa miesto vpichu nemá masírovať. Pacient musí byť riadne poučený o správnej aplikačnej technike.
Profil účinku Liprologu Basal je veľmi podobný účinku bazálneho inzulínu (NPH) po dobu približne
15 hodín. Časový priebeh aktivity akéhokoľvek inzulínu sa môže významne líšiť u rôznych osôb alebo u jednej osoby v rôznych časových intervaloch. Rovnako ako u všetkých inzulínových prípravkov závisí trvanie účinku Liprologu Basal na dávke, mieste vpichu, krvnom zásobovaní, teplote a fyzickej aktivite.
4.3 Kontraindikácie
Precitlivenosť na inzulín lispro alebo na ktorúkoľvek z pomocných látok. Hypoglykémia.
4.4 Osobitné upozornenia a opatrenia pri používaní
Liprolog Basal sa nesmie za žiadnych okolností podať intravenózne.
Prechod pacienta na iný typ alebo značku inzulínu sa musí uskutočniť pod prísnym lekárskym dohľadom. Zmeny koncentrácie, značky (výrobcu), typu (regular, NPH, lente ai.), druhu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo spôsobu výroby (rekombinantná DNA oproti inzulínu zvieracieho pôvodu) môžu mať za následok potrebu zmeny dávkovania.
Dlhotrvajúci diabetes, intenzifikovaná inzulínová terapia, diabetická neuropatia alebo užívanie liekov, ako sú beta-blokátory môžu zmeniť alebo zmierniť skoré varovné príznaky hypoglykémie.
Malý počet pacientov, ktorí mali hypoglykemické reakcie po prechode z inzulínu zvieracieho pôvodu na ľudský inzulín, uvádzalo, že skoré varovné príznaky hypoglykémie boli menej výrazné alebo odlišné od tých, ktoré zažili pri použití predchádzajúceho inzulínu. Nekontrolované hypoglykemické alebo hyperglykemické reakcie môžu spôsobiť stratu vedomia, kómu alebo smrť.
Použitie nedostatočných dávok alebo prerušenie liečby, najmä u inzulín-dependentných diabetikov,
môže viesť k hyperglykémii a diabetickej ketoacidóze; stavom, ktoré môžu byť letálne.
Potreba inzulínu môže byť znížená pri poškodení funkcie obličiek. Potreba inzulínu môže byť znížená u pacientov s poškodením funkcie pečene z dôvodov nižšej kapacity pre glukoneogenézu a zhoršeného odburávania inzulínu; avšak u pacientov s chronickým poškodením funkcie pečene môže zvýšenie inzulínovej rezistencie viesť ku vyššej potrebe inzulínu.
Potreba inzulínu sa môže zvýšiť počas ochorenia alebo vplyvom emocionálnych stresov.
Úprava dávky môže byť rovnako potrebná, pokiaľ pacienti vykonávajú zvýšenú fyzickú aktivitu alebo menia svoju zvyčajnú diétu. Cvičenie ihneď po požití potravy môže zvýšiť riziko hypoglykémie.
Podanie inzulínu lispro deťom mladším ako 12 rokov sa má zvážiť iba v prípade očakávaného prínosu
v porovnaní s regular inzulínom.
Kombinácia Liprologu Basal a pioglitazónu
V prípadoch, keď sa použil pioglitazón v kombinácii s inzulínom, boli zaznamenané prípady srdcového zlyhania, najmä u pacientov s rizikovými faktormi pre vznik srdcového zlyhania. T reba mať na zreteli tieto fakty v prípade, že sa zvažuje liečba kombináciou pioglitazónu a Liprologu Basal. Ak pacient používa danú kombináciu, je u neho potrebné sledovať znaky a symptómy srdcového zlyhania, priberanie na hmotnosti a edém. Ak sa zistí akékoľvek zhoršenie srdcových symptómov, pioglitazón sa musí prestať podávať.
4.5 Liekové a iné interakcie
Potreba inzulínu sa môže zvýšiť látkami s hyperglykemickým účinkom, ako je perorálna antikoncepcia, kortikosteroidy alebo hormonálna substitúcia počas liečby porúch štítnej žľazy, danazol, beta2-mimetiká (ritodrín, salbutamol, terbutalín).
Potreba inzulínu sa môže znížiť pri podávaní liekov s hypoglykemickým účinkom ako sú perorálne antidiabetiká, salicyláty (napr. kyselina acetylosalicylová), sulfónamidy, niektoré antidepresíva (inhibítory monoaminooxidázy, selektívne inhibítory spätného vychytávania sérotonínu), niektoré
inhibítory angiotenzín konvertujúceho enzýmu (kaptopril, enalapril), blokátory receptorov angiotenzínu II, beta-blokátory, oktreotid alebo alkohol.
Miešanie Liprologu Basal s inzulínmi inými ako je Liprolog sa neskúmalo.
Užívanie iných liekov podávaných súčasne s Liprologom Basal 100 U/ml KwikPen sa musí
konzultovať s lekárom (pozri časť 4.4).
4.6 Fertilita, gravidita a laktácia
Údaje o veľkom počte gravidných žien užívajúcich inzulín lispro nepreukázali žiadne nežiaduce
účinky na graviditu alebo na zdravie plodu/novorodenca.
Udržanie dobrej kontroly glykémie počas gravidity je základnou požiadavkou liečby diabetu
u pacientky liečenej inzulínom pri inzulín-dependentnom alebo gestačnom diabete. Potreba inzulínu sa zvyčajne znižuje počas prvého trimestra a zvyšuje počas druhého a tretieho trimestra. Pacientky
s diabetom majú byť poučené o tom, aby informovali svojho lekára v prípade gravidity alebo ak graviditu zvažujú. Starostlivé monitorovanie glykémie, rovnako ako aj celkového zdravotného stavu, je základnou požiadavkou u gravidných s diabetom.
U dojčiacich diabetičiek môže vzniknúť potreba úpravy dávky inzulínu, diéty alebo oboje.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta koncentrovať sa a reagovať môže byť porušená v dôsledku hypoglykémie. Môže to byť riskantné v situáciách špeciálne vyžadujúcich vyššie uvedené schopnosti (napr. vedenie auta alebo obsluha strojov).
Pacient má byť poučený o potrebe zabrániť hypoglykémii počas vedenia vozidla, čo je obzvlášť dôležité u tých osôb, ktoré majú zníženú alebo chýbajúcu vnímavosť varovných príznakov hypoglykémie alebo majú časté hypoglykemické epizódy. Za týchto okolností sa musí starostlivo zvážiť vhodnosť vedenia vozidiel.
4.8 Nežiaduce účinky
Najčastejším nežiaducim účinkom inzulínovej terapie u pacienta s diabetom je hypoglykémia. Závažná hypoglykémia môže viesť ku strate vedomia a v extrémnych prípadoch ku smrti. Frekvencia výskytu hypoglykémie nie je uvedená, pretože hypoglykémia je výsledkom pôsobenia nielen dávky inzulínu ale aj iných faktorov, napr. diéta pacienta a fyzická aktivita.
Často (1/100 až <1/10) sa u pacientov objavuje lokálna precitlivenosť. V mieste aplikácie inzulínu sa môže vyskytnúť začervenanie, opuch a svrbenie. Tento stav obvykle ustúpi počas niekoľkých dní alebo týždňov. V niektorých prípadoch môže byť tento stav zapríčinený inými faktormi ako inzulínom, napríklad iritáciou kože dezinfekčným prostriedkom alebo nesprávnou injekčnou technikou. Systémová alergia, ktorá je zriedkavá (1/10 000 až <1/1 000), ale potenciálne závažnejšia,
je generalizovanou alergiou na inzulín. Môže spôsobiť vyrážky po celom tele, dýchavičnosť, pískanie, pokles krvného tlaku, zrýchlený pulz alebo potenie. Ťažké stavy generalizovanej alergie môžu ohrozovať život.
Lipodystrofia v mieste aplikácie injekcie je menej častá (1/1 000 až <1/100).
Prípady edémov počas inzulínovej liečby boli hlásené najmä vtedy, keď v dôsledku intenzívnejšej inzulinoterapie došlo k zlepšeniu predchádzajúcej zlej metabolickej kompenzácie.
Hlásenie podozrení na nežiaduce reakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné
monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili

akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.4.9 PredávkovanieInzulín nemá špecifickú definíciu predávkovania, pretože sérová hladina krvného cukru je výsledkom komplexných interakcií medzi hladinou inzulínu, dostupnosťou glukózy a ostatnými metabolickými procesmi. Hypoglykémia sa môže objaviť ako dôsledok nadbytku inzulínovej aktivity v pomere
k príjmu potravy a výdaju energie.
Hypoglykémia môže byť spojená s nevšímavosťou, zmätenosťou, palpitáciami, bolesťami hlavy,
potením a vracaním.
Mierne epizódy hypoglykémie reagujú na perorálne podanie glukózy, iného cukru, príp. produktu obsahujúceho sacharidy.
Korekcia stredne ťažkej hypoglykémie sa môže uskutočniť intramuskulárnou alebo subkutánnou aplikáciou glukagónu a následným perorálnym podaním sacharidov, pokiaľ sa pacient dostatočne zotaví. Pacienti, ktorí nereagujú na glukagón, musia dostať infúziu glukózy intravenózne.
Pokiaľ je pacient v kóme, má sa aplikovať glukagón intramuskulárne alebo subkutánne. Pokiaľ však glukagón nie je k dispozícii alebo pacient na jeho podanie nereaguje, musí sa podať roztok glukózy intravenózne. Akonáhle sa pacient preberie z bezvedomia, musí sa najesť.
Po zdanlivej úprave klinického stavu môže byť potrebný trvalý príjem sacharidov a sledovanie
pacienta, pretože hypoglykémia sa môže opakovať.
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Inzulíny a ich analógy, strednodobo pôsobiace inzulíny, ATC kód: A10A C04.
Primárnym účinkom inzulínu lispro je regulácia glukózového metabolizmu.
Navyše má inzulín ďalšie anabolické a anti-katabolické vlastnosti na varietu rôznych tkanív.
V svalovom tkanive tieto účinky zahŕňajú zvýšenie syntézy glykogénu, mastných kyselín, glycerolu a proteínov a vychytávanie aminokyselín a zároveň zníženie glykogenolýzy, glukoneogenézy, ketogenézy, lipolýzy, proteínového katabolizmu a tvorby aminokyselín.
Profil účinku Liprologu Basal je veľmi podobný účinku bazálneho inzulínu (NPH) v časovom
intervale približne 15 hodín.
Glukodynamická odpoveď na inzulín lispro nie je ovplyvnená poškodením funkcie obličiek alebo pečene. Glukodynamické rozdiely medzi inzulínom lispro a rozpustným ľudským inzulínom merané v priebehu glukózového clampu boli udržané v širokom spektre renálnych funkcií.
Bolo preukázané, že inzulín lispro je molárne ekvipotentný s ľudským inzulínom, ale jeho účinok nastupuje rýchlejšie a má kratšiu dobu trvania.
5.2 Farmakokinetické vlastnostiLiprolog Basal má predĺženú absorpciu a dosahuje maximálne koncentrácie inzulínu približne za
6 hodín po aplikácii dávky. Pri hodnotení klinickej významnosti takejto kinetiky je vhodnejšie vyšetriť
krivky utilizácie glukózy.
Inzulín lispro je u pacientov s poškodením funkcie obličiek absorbovaný rýchlejšie ako rozpustný ľudský inzulín. U pacientov s diabetom typu 2 v širokom spektre renálnych funkcií boli farmakokinetické diferencie medzi inzulínom lispro a rozpustným ľudským inzulínom dodržané
a ukázali sa nezávislými na renálnych funkciách. Inzulín lispro je u pacientov s poškodením funkcie
pečene absorbovaný a eliminovaný rýchlejšie v porovnaní s rozpustným ľudským inzulínom.
5.3 Predklinické údaje o bezpečnosti
Pri testoch uskutočnených in vitro zahŕňajúcich väzbu na inzulínové receptory a účinky na rastúce bunky, sa inzulín lispro správal spôsobom, ktorý veľmi pripomínal ľudský inzulín. Štúdie tiež preukázali, že disociácia väzby inzulínu lispro na inzulínový receptor je totožná s ľudským inzulínom. Akútne, jeden mesiac a dvanásť mesiacov trvajúce toxikologické štúdie nepreukázali žiadne
významné toxikologické účinky.
V štúdiách na zvieratách inzulín lispro nespôsoboval poškodenie plodnosti, prejavy embryotoxicity alebo teratogenicity.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Protamíniumsulfát Metakrezol[1,76 mg/ml] Fenol [0,80 mg/ml] Glycerol
Heptahydrát hydrogénfosforečnanu sodného
Oxid zinočnatý
Voda na injekciu
Kyselina chlorovodíková a hydroxid sodný môžu byť použité na úpravu pH na 7,0 - 7,8.
6.2 Inkompatibility
Miešanie Liprologu Basal s inzulínmi inými ako Liprolog sa neskúmalo. Tento liek sa nesmie miešať
s inými liekmi okrem Liprologu.
6.3 Čas použiteľnosti
Nepoužité predplnené pero
2 roky
Po prvom použití
21 dní
6.4 Špeciálne upozornenia na uchovávanie
Nepoužité predplnené pero
Uchovávajte v chladničke pri teplote (2°C – 8°C). Neuchovávajte v mrazničke. Nevystavujte
nadmernému teplu alebo priamemu slnečnému svetlu.
Po prvom použití
Uchovávajte pri teplote do 30°C. Neuchovávajte v chladničke. Predplnené pero neuchovávajte
s nasadenou ihlou.
6.5 Druh obalu a obsah balenia a špeciálne zariadenie na použitie, podanie alebo implantáciu
Suspenzia sa plní do náplní z kremičitého skla typu I, ktoré sú utesnené halobutylovým diskovým uzáverom s piestom a zabezpečené alumíniovým tesnením. Na ošetrenie piestu a/alebo skla náplne sa môže použiť dimetikón alebo silikónová emulzia. Náplne s objemom 3 ml sú uzatvorené v dávkovači na jednorazové použitie, nazývanom „KwikPen“. Ihly nie sú súčasťou balenia.
Nie všetky veľkosti balenia musia byť uvedené do obehu.
5 x 3 ml Liprolog Basal 100 U/ml KwikPen
2 x (5 x 3 ml) Liprolog Basal 100 U/ml KwikPen
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými požiadavkami.
Návod na použitie
Bezprostredne pred použitím sa pero KwikPen desaťkrát premieša prevaľovaním v dlaniach
a desaťkrát prevráti o 180° z dôvodu premiešania inzulínu na docielenie rovnomerného zákalu alebo
mliečneho zafarbenia. Pokiaľ sa tak nestane, je potrebné opakovať vyššie uvedený postup, až kým sa
obsah nepremieša. Náplne obsahujú malú sklenenú guľôčku uľahčujúcu miešanie. Netraste rázne, pretože to môže spôsobiť spenenie, ktoré by mohlo ovplyvniť správne odmeranie dávky.
Náplne sa majú často kontrolovať a nesmú sa použiť, pokiaľ inzulín tvorí zhluky alebo pokiaľ pevné biele častice ostávajú na dne alebo na stene náplne, ktorá tým získava matný vzhľad.
Zaobchádzanie s naplneným perom
Pred použitím pera KwikPen je potrebné si starostlivo prečítať príručku pre používateľa v písomnej
informácii pre používateľa. KwikPen sa musí používať podľa odporúčaní v príručke pre používateľa.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Eli Lilly Nederland B.V., Grootslag 1-5, 3991 RA Houten, Holandsko.
8. REGISTRAČNÉ ČÍSLA
EU/1/01/195/026 5 x 3 ml Liprolog Basal 100 U/ml KwikPen
EU/1/01/195/027 2 x (5 x 3 ml) Liprolog Basal 100 U/ml KwikPen
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 1. augusta 2001
Dátum posledného predĺženia: 1. augusta 2006
10. DÁTUM REVÍZIE TEXTU
1. NÁZOV LIEKU
Liprolog 200 jednotiek/ml, injekčný roztok naplnený v injekčnom pere.
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Jeden ml roztoku obsahuje 200 jednotiek (zodpovedá 6,9 mg) inzulínu lispro*. Každé pero obsahuje 600 jednotiek inzulínu lispro v 3 ml roztoku.
*produkovaného v E. coli technológiou rekombinantnej DNA.
Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčný roztok. KwikPen. Číry, bezfarebný vodný roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Na liečbu dospelých s diabetom mellitus, ktorí potrebujú inzulín na udržanie normálnej glukózovej homeostázy. Rovnako sa Liprolog 200 jednotiek/ml KwikPen indikuje na iniciálnu stabilizáciu diabetes mellitus.
4.2 Dávkovanie a spôsob podávania
Dávkovanie
Dávkovanie stanoví lekár v súlade s potrebami pacienta.
Liprolog sa môže aplikovať krátko pred jedlom. Ak je to potrebné, Liprolog možno podať krátko po
jedle.
Liprolog účinkuje po subkutánnom podaní rýchlo a kratšiu dobu (2 -5 hodín) v porovnaní s regular inzulínom. Tento rýchly nástup účinku dovoľuje podávanie injekcie Liprologu veľmi krátko pred jedlom alebo po jedle. Časový priebeh aktivity akéhokoľvek inzulínu sa môže významne líšiť
u rôznych osôb alebo u jednej osoby v rôznych časových intervaloch. Nástup účinku inzulínu lispro je
v porovnaní s rozpustným ľudským inzulínom rýchlejší nezávisle na mieste vpichu. Rovnako ako u všetkých inzulínových liekov závisí trvanie účinku Liprologu na dávke, mieste vpichu, krvnom zásobovaní, teplote a fyzickej aktivite.
Liprolog môže byť podľa rady lekára aplikovaný v kombinácii s dlhšie pôsobiacim inzulínom alebo s derivátmi sulfonylurey podanými perorálne.
Liprolog 100 jednotiek/ml KwikPen a Liprolog 200 jednotiek/ml KwikPen
Liprolog KwikPen je dostupný v dvoch silách. Pri oboch silách sa potrebná dávka nastavuje po jednotkách. Obidvomi naplnenými perami, Liprolog 100 jednotiek/ml KwikPen aj Liprolog
200 jednotiek/ml KwikPen, si podáte 1 - 60 jednotiek postupne po jednej jednotke v každej injekcii. Počítadlo dávkovača ukazuje počet jednotiek, bez ohľadu na silu a nie je potrebné upravovať dávku, keď pacienta prestavujete na novú silu.
Liprolog 200 jednotiek/ml KwikPen je určený pre diabetických pacientov, ktorých denná dávka rýchlo
pôsobiaceho inzulínu je vyššia ako 20 jednotiek. Roztok inzulínu lispro obsahujúci 200 jednotiek/ml
sa nemá vyberať z naplneného pera (KwikPen) ani miešať s inými inzulínmi (pozri časť 4.4 a časť 6.2)
Špeciálne skupiny
Poškodenie funkcie obličiek
Potreba inzulínu môže byť znížená pri poškodení funkcie obličiek.
Poškodenie funkcie pečene
Potreba inzulínu môže byť znížená u pacientov s poškodením funkcie pečene z dôvodu nižšej kapacity pre glukoneogenézu a zhoršeného odbúravania inzulínu. Avšak u pacientov s chronickým
poškodením funkcie pečene môže zvýšenie inzulínovej rezistencie viesť k vyššej potrebe inzulínu.
Spôsob podania
Injekčný roztok Liprologu sa má podávať subkutánne.
Miesta subkutánneho podania majú byť horná časť ramien, stehno, zadok alebo brucho. Miesta vpichu sa majú meniť rotačným spôsobom tak, aby sa rovnaké miesto nepoužilo viackrát ako približne raz za mesiac.
Pri subkutánnej aplikácii Liprologu je potrebné sa dôkladne uistiť o tom, že nedošlo k aplikácii
do cievy. Po aplikácii sa miesto vpichu nemá masírovať. Pacient musí byť riadne poučený o správnej
aplikačnej technike.
Nepoužívajte Liprolog 200 jednotiek/ml KwikPen injekčný roztok v inzulínových pumpách. Nepoužívajte Liprolog 200 jednotiek/ml KwikPen injekčný roztok intravenózne.
4.3 Kontraindikácie
Precitlivenosť na liečivo alebo na ktorúkoľvek z pomocných látok uvedených v časti 6.1.
Hypoglykémia.
4.4 Osobitné upozornenia a opatrenia pri používaní
Prechod pacienta na iný typ alebo značku inzulínu
Prechod pacienta na iný typ alebo značku inzulínu sa musí uskutočniť pod prísnym lekárskym dohľadom. Zmeny koncentrácie, značky (výrobcu), typu (regular, NPH, lente a i.), druhu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo spôsobu výroby (rekombinantná DNA oproti inzulínu zvieracieho pôvodu) môžu mať za následok potrebu zmeny dávkovania. Každý pacient, ktorý užíva popri rýchlo pôsobiacom aj bazálny inzulín, musí optimalizovať dávkovanie oboch inzulínov, aby dosiahol kontrolu glykémie po celý deň, najmä kontrolu glykémie v noci/nalačno.
Hypoglykémia a hyperglykémia
Dlhotrvajúci diabetes, intenzifikovaná inzulínová terapia, diabetická neuropatia alebo užívanie liekov, ako sú beta-blokátory, môžu zmeniť alebo zmierniť skoré varovné príznaky hypoglykémie.
Malý počet pacientov, ktorí mali hypoglykemické reakcie po prechode z inzulínu zvieracieho pôvodu na ľudský inzulín, uvádzalo, že skoré varovné príznaky hypoglykémie boli menej výrazné alebo odlišné od tých, ktoré zažili pri použití predchádzajúceho inzulínu. Nekontrolované hypoglykemické alebo hyperglykemické reakcie môžu spôsobiť stratu vedomia, kómu alebo smrť.
Použitie neadekvátnych dávok alebo prerušenie liečby, najmä u inzulín-dependentných diabetikov,
môže viesť k hyperglykémii a diabetickej ketoacidóze, ktoré sú potenciálne letálne.
Potreba inzulínu a úprava dávky
Potreba inzulínu sa môže zvýšiť počas choroby alebo pri emocionálnom rozrušení.
Úprava dávky môže byť tiež potrebná, pokiaľ pacienti vykonávajú zvýšenú fyzickú aktivitu alebo menia svoju zvyčajnú diétu. Cvičenie ihneď po požití potravy môže zvýšiť riziko hypoglykémie. Dôsledok farmakodynamiky rýchlo pôsobiaceho analógu ľudského inzulínu je výskyt hypoglykémie, pri porovnaní s rozpustným ľudským inzulínom, sa po injekcii môže vyskytnúť skôr.
Kombinácia Liprologu s pioglitazónom:
V prípadoch, keď sa použil pioglitazón v kombinácii s inzulínom, boli zaznamenané prípady srdcového zlyhania, najmä u pacientov s rizikovými faktormi pre vznik srdcového zlyhania. Treba mať na zreteli tieto fakty v prípade, že sa zvažuje liečba kombináciou pioglitazónu a Liprologu. Ak
pacient používa danú kombináciu, je u neho potrebné sledovať prejavy a príznaky srdcového zlyhania, priberanie na hmotnosti a edém. Ak sa zistí akékoľvek zhoršenie srdcových príznakov, pioglitazón sa musí prestať podávať.
Ako savyvarovať chybámvliečbe pripoužití inzulínu lispro (200U/ml) naplnený vinjekčnom pere: Roztok inzulínu lispro obsahujúci 200 jednotiek/ml sa nesmie prenášať z naplneného pera KwikPen do injekčnej striekačky. Značky na inzulínovej striekačke neodmerajú dávku správne. Predávkovanie
môže spôsobiť závažnú hypoglykémiu. Injekčný roztok inzulínu lispro obsahujúci 200 jednotiek/ml sa nesmie prenášať z KwikPenu do žiadnej inej inzulínovej pomôcky vrátane inzulínových púmp.
Pomocné látky
Tento liek obsahuje menej ako 1 mmol sodíka (23 mg) v jednej dávke, takže je v podstate „bez sodíka“.
4.5 Liekové a iné interakcie
Potreba inzulínu sa môže zvýšiť liekmi s hyperglykemickým účinkom, ako je perorálna antikoncepcia, kortikosteroidy alebo hormonálna substitučná terapia pri liečbe porúch štítnej žľazy, danazol, beta2-mimetiká (ritodrín, salbutamol, terbutalín).
Potreba inzulínu sa môže znížiť pri podávaní liekov s hypoglykemickým účinkom, ako sú perorálne
antidiabetiká, salicyláty (napríklad kyselina acetylsalicylová), sulfónamidy, niektoré antidepresíva (inhibítory monoaminooxidázy, selektívne inhibítory spätného vychytávania sérotonínu), niektoré inhibítory angiotenzín konvertujúceho enzýmu (kaptopril, enalapril), blokátory receptorov angiotenzínu II, beta-blokátory, oktreotid alebo alkohol.
Používanie iných liekov podávaných súčasne s Liprologom 200 jednotiek/ml KwikPen sa musí
konzultovať s lekárom (pozri časť 4.4).
4.6 Fertilita, gravidita a laktácia
Gravidita
Údaje o veľkom počte gravidných žien užívajúcich inzulín lispro nepreukázali žiadne nežiaduce
účinky na graviditu alebo na zdravie plodu/novorodenca.
Udržanie dobrej kontroly glykémie počas gravidity je základnou požiadavkou liečby diabetu
u pacientky liečenej inzulínom pri inzulín-dependentnom alebo gestačnom diabete. Potreba inzulínu sa obvykle znižuje počas prvého trimestra a zvyšuje počas druhého a tretieho trimestra. Pacientky
s diabetom majú byť poučené o tom, aby informovali svojho lekára v prípade gravidity alebo pokiaľ graviditu zvažujú. Starostlivé monitorovanie glykémie, rovnako ako aj celkového zdravotného stavu, je základnou požiadavkou u gravidných s diabetom.
Laktácia
Dojčiace diabetičky môžu potrebovať úpravu dávky inzulínu, diéty alebo oboje.
Fertilita
V štúdiách so zvieratami inzulín lispro nespôsobil zhoršenie fertility (pozri časť 5.3).
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta koncentrovať sa a reagovať môže byť porušená v dôsledku hypoglykémie. To môže byť riskantné v situáciách špeciálne vyžadujúcich vyššie uvedené schopnosti (napr. vedenie auta alebo obsluha strojov).
Pacient má byť poučený o nutnosti zabrániť hypoglykémii počas vedenia vozidla, čo je obzvlášť dôležité u tých osôb, ktoré majú zníženú alebo chýbajúcu vnímavosť varovných príznakov hypoglykémie alebo majú časté hypoglykemické epizódy. Za týchto okolností sa má starostlivo zvážiť vhodnosť vedenia vozidiel.
4.8 Nežiaduce účinkyZhrnutie bezpečnostného profiluNajčastejším nežiaducim účinkom inzulínovej terapie u pacienta s diabetom je hypoglykémia.
Závažná hypoglykémia môže viesť ku strate vedomia a v extrémnych prípadoch ku smrti. Frekvencia výskytu hypoglykémie nie je uvedená, pretože hypoglykémia je výsledkom pôsobenia nielen dávky inzulínu ale aj iných faktorov, napr. diéta pacienta a fyzická aktivita.
Zoznam nežiaducich účinkov v tabuľkovom formáteZ klinických štúdií vyplynuli nasledujúce nežiaduce účinky, ktoré sú zoradené podľa tried orgánových
systémov a v poradí podľa klesajúceho výskytu (veľmi časté: ≥ 1/10; časté: ≥ 1/100 až < 1/10; menej časté: ≥ 1/1 000 až < 1/100; zriedkavé: ≥ 1/10 000 až < 1/1 000; veľmi zriedkavé: < 1/10 000).
V rámci jednotlivých skupín frekvencií sú nežiaduce reakcie usporiadané v poradí klesajúcej závažnosti.
MedDRA triedy orgánových systémov
| Veľmi časté
|
Časté
| Menej
časté
|
Zriedkavé
| Veľmi
zriedkavé
|
Poruchy imunitného systému
|
Lokálna alergická reakcia
|
| X
|
|
|
|
Systémová alergická reakcia
|
|
|
| X
|
|
Poruchy kože a podkožného tkaniva
|
Lipodystrofia
|
|
| X
|
|
|
Opis vybraných nežiaducich reakciíLokálna alergická reakciaČasto sa u pacientov objavuje lokálna precitlivenosť. V mieste aplikácie inzulínu sa môže vyskytnúť začervenanie, opuch a svrbenie. Tento stav obvykle ustúpi počas niekoľkých dní alebo týždňov.
V niektorých prípadoch môže byť tento stav zapríčinený inými faktormi ako inzulínom, napríklad iritáciou kože dezinfekčným prostriedkom alebo nesprávnou injekčnou technikou.
Systémová alergická reakciaSystémová alergia, ktorá je zriedkavá , ale potenciálne závažnejšia, je generalizovanou alergiou na inzulín. Môže spôsobiť vyrážky po celom tele, dýchavičnosť, pískanie, pokles krvného tlaku, zrýchlený pulz alebo potenie. Ťažké stavy generalizovanej alergie môžu ohrozovať život.
LipodystrofiaLipodystrofia v mieste aplikácie injekcie je menej častá (1/1 000 až <1/100).
EdémPrípady edémov počas inzulínovej liečby boli hlásené najmä vtedy, keď v dôsledku intenzívnejšej inzulínoterapie došlo k zlepšeniu predchádzajúcej zlej metabolickej kompenzácie.
Hlásenie podozrení na nežiaduce reakcie

Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.4.9 PredávkovanieInzulín nemá špecifickú definíciu predávkovania, pretože sérová hladina krvného cukru je výsledkom komplexných interakcií medzi hladinou inzulínu, dostupnosťou glukózy a ostatnými metabolickými procesmi. Hypoglykémia sa môže objaviť ako dôsledok nadbytku inzulínu v pomere k príjmu potravy a výdaju energie.
Hypoglykémia môže byť spojená s ľahostajnosťou, zmätenosťou, palpitáciami, bolesťami hlavy,
potením a vracaním.
Mierne epizódy hypoglykémie reagujú na perorálne podanie glukózy alebo iného cukru, prípadne produktu obsahujúceho sacharidy.
Korekcia stredne ťažkej hypoglykémie sa môže uskutočniť intramuskulárnou alebo subkutánnou aplikáciou glukagónu a následným perorálnym podaním uhľohydrátov, pokiaľ sa pacient dostatočne zotaví. Pacienti, ktorí nereagujú na glukagón, musia dostať infúziu glukózy intravenózne.
Pokiaľ je pacient v kóme, glukagón sa má aplikovať intramuskulárne alebo subkutánne. Pokiaľ však glukagón nie je k dispozícii alebo pacient na jeho podanie nereaguje, musí sa podať roztok glukózy intravenózne. Akonáhle sa pacient preberie z bezvedomia, musí sa najesť.
Po zdanlivej úprave klinického stavu môže byť potrebný trvalý príjem sacharidov a sledovanie
pacienta, pretože hypoglykémia sa môže opakovať.
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Lieky používané pri diabete, inzulíny a analógy na injekciu, rýchlo pôsobiace, ATC kód: A10AB04.
Primárnym účinkom inzulínu lispro je regulácia glukózového metabolizmu.
Navyše má inzulín ďalšie anabolické a antikatabolické účinky na mnoho rôznych tkanív. V svalovom
tkanive tieto účinky zahŕňajú zvýšenie syntézy glykogénu, mastných kyselín, glycerolu a proteínov a vychytávanie aminokyselín a zároveň zníženie glykogenolýzy, glukoneogenézy, ketogenézy, lipolýzy, proteínového katabolizmu a tvorby aminokyselín.
Inzulín lispro má rýchly nástup účinku (približne 15 minút), čo umožňuje jeho podanie krátko pred alebo po jedle (interval od 0 do 15 minút), v porovnaní s bežným rýchlo pôsobiacim inzulínom (aplikácia 30 až 45 minút pred jedlom). Nástup účinku inzulínu lispro je rýchly a trvanie aktivity kratšie (2 až 5 hodín) v porovnaní s regular inzulínom.
Klinické štúdie u pacientov s diabetom typu 1 alebo 2 preukázali nižší výskyt postprandiálnej hyperglykémie u inzulínu lispro v porovnaní s rozpustným ľudským inzulínom.
Časový priebeh účinku inzulínu lispro môže byť odlišný u rôznych jedincov alebo odlišný v rôznych časových intervaloch u rovnakého jedinca v závislosti na dávke, mieste injekcie, krvnom zásobení, teplote a fyzickej aktivite. Typický priebeh aktivity v čase po subkutánnej injekcii ilustruje nasledujúci graf.
Obrázok 1:

Hypoglykemická aktivita
Inzulín lispro
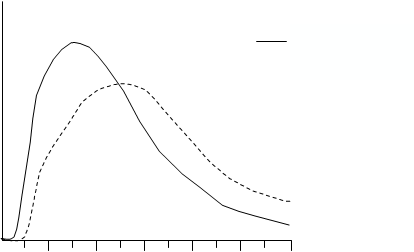
Humulin R
0 1 2
3 4 5 6

Čas (hodiny)
Graf (obrázku 1) zobrazuje relatívne množstvo glukózy v závislosti na čase potrebné na udržanie
celkovej plazmatickej glukózovej koncentrácie testovaného jedinca blízko hladinám nalačno a je indikátorom efektu týchto inzulínov (100 jednotiek/ml) na glukózový metabolizmus v závislosti od času.
Ako vidno z nasledujúceho grafu (obrázok 2), farmakodynamické odpovede injekčného roztoku
200 jednotiek/ml inzulínu lispro boli podobné ako farmakodynamické odpovede injekčného roztoku inzulínu lispro 100 jednotiek/ml podaného subkutánne v jedinej 20-jednotkovej dávke zdravým jedincom.
inzulín lispro 200 jednotiek/ml
inzulín lispro 100 jednotiek/ml

Čas (hod)
 Obrázok 2:
Obrázok 2:Aritmetický priemer rýchlosti glukózovej infúzie v závislosti od času po podaní 20 jednotiek
200-jednotkového (200 U/ml) inzulínu lispro alebo 100-jednotkového (100 U/ml) inzulínu lispro.
Štúdie ukázali, že pridanie inzulínu lispro signifikantne znižuje hladinu HbA1C v porovnaní
so samotnou sulfonylureou u pacientov s diabetom typu 2 na maximálnych dávkach derivátov
sulfonylurey. Zníženie hladiny HbA1C možno očakávať takisto pri kombinácii s inými prípravkami inzulínu, napr. regular alebo izofán inzulínom.
Klinické štúdie s pacientami s diabetom typu 1 a 2 preukázali nižší počet nočných hypoglykémií
s inzulínom lispro v porovnaní s rozpustným ľudským inzulínom. V niektorých štúdiách bol nižší
počet nočných hypoglykémií spojený so zvýšeným počtom denných hypoglykémií.
Glukodynamická odpoveď na inzulín lispro nie je ovplyvnená poškodením funkcie obličiek alebo pečene. Glukodynamické rozdiely medzi inzulínom lispro a rozpustným ľudským inzulínom merané v priebehu glukózového clampu boli udržané v širokom spektre renálnych funkcií.
Bolo preukázané, že inzulín lispro je molárne ekvipotentný s ľudským inzulínom, ale jeho účinok
nastupuje rýchlejšie a má kratšiu dobu trvania.
5.2 Farmakokinetické vlastnosti
Farmakokinetika inzulínu lispro zodpovedá látke, ktorá sa rýchlo absorbuje a dosahuje najvyššie plazmatické hladiny v čase od 30 do 70 minút po subkutánnej injekcii. Pri zvažovaní klinickej relevancie tejto kinetiky je vhodnejšie vyšetriť krivky utilizácie glukózy (pozri 5.1).
Inzulín lispro je u pacientov s poškodením funkcie obličiek absorbovaný rýchlejšie ako rozpustný ľudský inzulín. U pacientov s diabetom typu 2 v širokom spektre renálnych funkcií boli všeobecne dodržané farmakokinetické rozdiely medzi inzulínom lispro a rozpustným inzulínom a ukázali sa nezávislými na renálnych funkciách. Inzulín lispro je u pacientov s poškodením funkcie pečene absorbovaný a eliminovaný rýchlejšie v porovnaní s rozpustným ľudským inzulínom.
Injekčný roztok s obsahom 200 jednotiek/ml inzulínu lispro bol bioekvivalentný injekčnému roztoku s obsahom 100 jednotiek/ml inzulínu lispro po subkutánnom podaní jedinej 20-jednotkovej dávky zdravým jedincom. Čas do dosiahnutia maximálnej koncentrácie bol takisto podobný pre obidve formulácie.
5.3 Predklinické údaje o bezpečnosti
Pri testoch uskutočnených in vitro, zahŕňajúcich väzbu na inzulínové receptory a účinky na
rastúce bunky, sa inzulín lispro správal spôsobom, ktorý veľmi pripomínal ľudský inzulín. Štúdie tiež preukázali, že disociácia väzby inzulínu lispro na inzulínový receptor je totožná s ľudským inzulínom. Akútne, jeden mesiac a dvanásť mesiacov trvajúce toxikologické štúdie nepreukázali žiadne
významné toxikologické účinky.
V štúdiách na zvieratách inzulín lispro nespôsoboval poškodenie plodnosti, prejavy embryotoxicity alebo teratogenicity.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Metakrezol Glycerol Trometamol Oxid zinočnatý
Voda na injekciu
Kyselina chlorovodíková a hydroxid sodný môžu byť použité na úpravu pH.
6.2 Inkompatibility
Tento liek sa nesmie miešať so žiadnym iným inzulínom ani iným liekom Injekčný roztok sa nesmie riediť.
6.3 Čas použiteľnosti
Nepoužité naplnené perá
3 roky
Po prvom použití
28 dní
6.4 Špeciálne upozornenia na uchovávanie
Nepoužité naplnené perá
Uchovávajte v chladničke pri teplote (2°C – 8°C). Neuchovávajte v mrazničke. Nevystavujte
nadmernému teplu alebo priamemu slnečnému svetlu.
Po prvom použití
Uchovávajte pri teplote do 30 °C. Neuchovávajte v chladničke. Naplnené pero sa nemá uchovávať
s nasadenou ihlou.
6.5 Druh obalu a obsah balenia a špeciálne zariadenie na použitie, podanie alebo implantáciu
Roztok sa plní do sklenených náplní typu I uzavretých chlórbutylovým diskovým uzáverom s piestom, uzávery sú zabezpečené hliníkovým tesnením. Na ošetrenie piestu a/alebo skla náplne sa môže použiť dimetikón alebo silikónová emulzia. Náplne s objemom 3 ml obsahujúce 600 jednotiek inzulínu lispro (200 jednotiek/ml) sú vbudované do dávkovača na jednorazové použitie, ktorý sa nazýva „KwikPen“. Ihly nie sú súčasťou balenia.
1 naplnené 3 ml pero
2 naplnené 3 ml perá
5 naplnených 3 ml pier
multibalenie obsahujúce 10 (2 balenia po 5) naplnených 3 ml pier
Na trh nemusia byť uvedené všetky veľkosti balenia.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Návod na použitie
Roztok Liprologu má byť číry a bezfarebný. Pokiaľ sa Liprolog javí zakalený, zahustený alebo ľahko zafarbený alebo pokiaľ sú v ňom viditeľné pevné častice, nepoužívajte ho.
Zaobchádzanie s naplneným perom
Pred použitím pera KwikPen je potrebné si starostlivo prečítať príručku pre používateľa v písomnej
informácii pre používateľa. KwikPen sa musí používať podľa odporúčaní v príručke pre používateľa.
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými
požiadavkami.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Eli Lilly Nederland B.V, Grootslag 1-5, 3991 RA Houten, Holandsko
8. REGISTRAČNÉ ČÍSLA
EU/1/96/195/039
EU/1/96/195/040
EU/1/96/195/041
EU/1/96/195/042
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIEDátum prvej registrácie: 1. augusta 2001
Dátum posledného predĺženia: 1. augusta 2006
10. DÁTUM REVÍZIE TEXTUPodrobné informácie o tomto lieku sú dostupné na internetovej stránke Európskej agentúry pre lieky
http://www.ema.europa.eu