dávok. Pri monoterapii kyselinou valproovou môže byť celková denná dávka tiež podaná raz denne – večer (do maximálnej dávky 15 mg/kg telesnej hmotnosti/deň). Môže byť indikované monitorovanie krvných hladín (napr. pre sledovanie compliance, určovanie potenciálnej intoxikácie; pozri časť 5.2).
U pacientov predtým liečených inými liekmi sa má predchádzajúca antiepileptická terapia postupne redukovať.
Spôsob podania:Počas jedla alebo po jedle.
4. 3 Kontraindikácie Precitlivenosť na kyselinu valproovú, alebo na ktorúkoľvek z pomocných látok uvedených v časti 6.1, poruchy funkcie pečene (akútna hepatitída, chronická hepatitída, osobná alebo rodinná anamnéza ťažkej hepatitídy, hlavne spôsobenej liekmi, hepatálna porfýria) alebo funkcie pankreasu.
Špeciálna opatrnosť sa vyžaduje v nasledujúcich prípadoch:
- pri anamnéze hepatálnych alebo pankreatických ochorení, alebo abnormalitách kostnej drene
- pri hemoragickej diatéze
- pri renálnej dysfunkcii
- pri vrodených enzýmových poruchách
- pri ťažkých typoch epileptických záchvatov
- u mentálne retardovaných detí
- pri organických poškodeniach mozgu
- u detí mladších ako 2 roky (lebo sú zvlášť citlivé na poškodenie pečene; pozri časť 4.8 ).
4. 4 Osobitné upozornenia a opatrenia pri používaníTesty funkcie pečene, parametre koagulácie (čas krvácania, Quickov test, plazmatický fibrinogén, počet trombocytov, agregácia trombocytov, tromboelastogram) a určenie sérovej amylázy a lipázy má byť urobené pred začiatkom liečby, ako aj pri každom zvýšení dávky a v dvojmesačných intervaloch počas liečby.
Terapia sa musí ihneď prerušiť, aksa objaví jeden z nasledujúcich príznakov: hypofibrinogenémia, poruchy koagulácie, zvýšenie transamináz na ich trojnásobnú hodnotu, zvýšenie alkalickej fosfatázy alebo bilirubínu v sére, prvé príznaky toxickej hepatitídy (patologické laboratórne hodnoty spolu s klinickými príznakmi).
Ak sú ľahko zvýšené len transaminázy, treba znížiť dávku a monitorovať funkciu pečene a parametre koagulácie.
Funkcia pankreasu (amyláza, lipáza) má byť vyšetrená pred začiatkom terapie a opakovane počas liečby kyselinou valproovou a špeciálne, ak sa objaví nejasná bolesť brucha, príznaky organického poškodenia alebo hemoragických porúch. Pri prvých náznakoch pankreatitídy (abnormálne laboratórne hodnoty spojené s klinickými príznakmi) treba liečbu ihneď ukončiť.
Renálnu funkciu a hladiny sérového amoniaku treba monitorovať v pravidelných intervaloch.
Pre možné zvýšenie sklonu ku krvácaniu sa vyžaduje opatrnosť pri chirurgických alebo zubárskych zákrokoch.
Náhle vysadenie kyseliny valproovej môže viesť k zvýšeniu frekvencie záchvatov.
Pri liečbe antiepileptikami v niekoľkých indikáciách boli u pacientov hlásené suicidálne myšlienky a správanie. Metaanalýza randomizovaných placebom kontrolovaných štúdií s antiepileptikami ukázala malé zvýšenie rizika suicidálnych myšlienok a správania. Mechanizmus tohto rizika nie je známy a dostupné údaje nevylučujú možnosť zvýšeného rizika u nátriumvalproátu.
Pacientov je preto potrebné sledovať na príznaky a symptómy suicidálnych myšlienok a správania a je potrebné zvážiť vhodnú liečbu. Pacientom (a opatrovateľom pacientov) je potrebné odporučiť, aby vyhľadali lekársku pomoc, ak sa objavia príznaky suicidálnych myšlienok alebo správania.
Súčasné užívanie kyseliny valproovej/valproátu sodného a karbapenémov sa neodporúča (pozri časť 4.5).
Upozornenie pre diabetikov:Sirup Convulex obsahuje umelé sladidlá, preto ho môžu užívať aj diabetickí pacienti. Treba však počítať s obsahom karbohydrátov vo výške 0,05 sacharidových jednotiek v 1 ml sirupu.
Sirup Convulex obsahuje lykasín (roztok maltitolu). Pacienti so zriedkavými dedičnými problémami intolerancie fruktózy nesmú užívať tento liek.
4. 5 Liekové a iné interakcie Kyselina valproová vytláča fenytoín, fenobarbital a diazepam z väzby na plazmatickú bielkovinu, čo vedie k zvýšeniu neviazaných hladín týchto látok. Kyselina valproová inhibuje metabolizmus diazepamu. Sérové hladiny primidónu sú zvýšené. Účinok etosuximidu sa potencuje. Fenytoín, fenobarbital a primidón vedú k zvýšeniu klírensu a k zníženiu plazmatických hladín kyseliny valproovej. Súčasné podávanie kyseliny valproovej a karbapenémov spôsobilo zníženie hladiny kyseliny valproovej v krvi (60-100 % zníženie v priebehu dvoch dní). Z dôvodu rýchleho nástupu a rozsahu tohto poklesu sa súčasné podávanie karbapenémov u pacientov stabilizovaných na kyseline valproovej nepovažuje za zvládnuteľné, preto je nutné vyhnúť sa mu (pozri časť 4.4).
V zriedkavých prípadoch môže súčasné podávanie klonazepamu privodiť status absencií. V prípade kombinácie liečby s inými antiepileptikami je preto potrebné presne zistiť krvné hladiny (monitorovanie liekov). Súčasné užívanie felbamátu vedie k zvýšeniu plazmatických hladín kyseliny valproovej. Súčasné podávanie lamotrigínu zvyšuje polčas vylučovania tejto látky.
Kyselina valproová potencuje centrálne tlmivý účinok určitých liekov (napr. barbiturátov, primidónu, neuroleptík a antidepresív) a alkoholu.
Pôsobenie inhibítorov agregácie trombocytov (kyseliny acetylosalicilovej), antikoagulancií kumarínového typu a heparínu sa potencuje.
Podľa viacerých štúdií salicyláty vytláčajú kyselinu valproovú z jej väzby na sérový albumín a menia jej metabolizmus, čo môže vyústiť do toxických koncentrácií kyseliny valproovej (to je klinicky závažné hlavne u detí). Súčasné užívanie hepatotoxických liekov môže potencovať možné nežiaduce účinky kyseliny valproovej na pečeň.
Interakcie s perorálnymi kontraceptívami neboli hlásené.
Účinky kyseliny valproovej na laboratórne parametre:Kyselina valproová sa čiastočne vylučuje do moču ako ketometabolit, čo môže viesť k falošne pozitívnemu výsledku testu na ketolátky v moči u diabetických pacientov.
V závislosti od plazmatickej koncentrácie môže viesť kyselina valproová k vytláčaniu tyreoidálnych hormónov z ich väzby na bielkovinu a k ich rýchlejšej metabolizácii, takže tyreoidálne funkčné testy môžu nesprávne viesť k podozreniu na hypotyreoidizmus.
4. 6 Fertilita, gravidita a laktácia Gravidita
Riziko spojené s užívaním kyseliny valproovejŠtúdie na zvieratách dokázali, že kyselina valproová môže indukovať teratogenitu. U človeka boli pozorované defekty neurálnej trubice (spina bifida). Preto sa má počas gravidity používať najnižšie účinné dávkovanie kyseliny valproovej. Pokiaľ je to možné, treba sa vyhnúť kombinácii s inými antiepileptikami.
Počas prvých troch mesiacov gravidity sa nemá začínať liečba kyselinou valproovou. Ak gravidná žena už užíva ako antiepileptickú liečbu kyselinu valproovú, liek sa nemá náhle vysadiť, pretože vysadením sa riskuje zvýšenie frekvencie záchvatov alebo indukcia status epilepticus, čo môže byť životu nebezpečné pre matku aj plod. Hladiny kyseliny valproovej treba monitorovať (terapeutický rozsah).
Laktácia
Odporúča sa prerušiť dojčenie.
4. 7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje Convulex má vplyv na schopnosť viesť vozidlá a obsluhovať stroje. Reaktivita môže byť natoľko porušená, hlavne v kombinácii s alkoholom a na začiatku liečby,že je zmenená spôsobilosť pacienta viesť vozidlo alebo obsluhovať stroje. Konzumácii alkoholu sa treba vyhýbať.
4. 8 Nežiaduce účinky Vo všeobecnosti sa sirup Convulex dobre toleruje. Nežiaduce účinky sa vyskytujú len v zriedkavých prípadoch a sú častejšie pri plazmatických hladinách nad 100 mg/l a keď sa sirup Convulex užíva v kombinovanej liečbe.
Klasifikácia frekvencií nežiaducich účinkov je rozdelená nasledovne:
Veľmi časté (≥1/10), časté (≥1/100 až <1/10), menej časté (≥1/1 000 až <1/100), zriedkavé (≥1/10 000 až <1/1 000), veľmi zriedkavé (<1/10 000), neznáme (z dostupných údajov).
Vzhľadom na nekompletnosť údajov, nemôžu byť frekvencie určené pre všetky nežiaduce účinky.
Poruchy gastrointestinálneho traktu:Časté: nauzea, vracanie a anorexia sa vyskytujú prevažne na začiatku liečby a vymiznú pri prispôsobení dávky a pri užívaní počas jedla alebo po jedle. Bola hlásená zvýšená chuť do jedla, prírastok na hmotnosti, bolesti žalúdka, kŕče v žalúdku, hnačka a obstipácia.
Poruchy nervového systému:Zriedkavé: útlm, závrat, bolesť hlavy, depresívne stavy, agresia, mimovoľné pohyby, hyperaktivita, tonické kŕče, ataxia, poruchy koordinácie, tremor, asterixis, dysartria. V ojedinelých prípadoch boli niekoľko dní po dosiahnutí terapeutickej plazmatickej hladiny pozorované stavy zmätenosti, stupor a kóma; v týchto prípadoch je predpoklad, že ide o paradoxný účinok u pacientov s predchádzajúcimi psychickými poruchami.
Bol opísaný aj výskyt syndrómu podobného
Reyovmu.Poruchy oka: nystagmus a diplopia.
Poruchy krvi a lymfatického systému:Hlásené hematologické zmeny zahŕňajú trombocytopéniu, útlm agregácie trombocytov, neutropéniu, lymfocytózu, hypofibrinogenémiu a v extrémne zriedkavých prípadoch aj anémiu a útlm kostnej drene.
Poruchy metabolizmu a výživy:Bola hlásená hyperamonémia, vzostup hladín sérového glycínu a pokles hladín karnitínu.
Poruchy kože a podkožného tkaniva:Alergické kožné reakcie sa objavujú veľmi zriedkavo. Boli pozorované jednotlivé prípady petechiálneho krvácania, sklonu k tvoreniu hematómov a prechodnej straty vlasov.
Laboratórne a funkčné vyšetrenia:Zmeny v laboratórnych parametroch hepatálnych funkcií (zvýšenie ALT, AST, LAP, gammaGT, alkalickej fosfatázy, bilirubínu) sú počas liečby časté, ale normalizujú sa obyčajne po prispôsobení dávky. Pri výskyte klinických príznakov poškodenia pečene (recidivujúce ťažkosti v epigastriu, dávenie, anorexia, únava, asténia, ikterus, ascites, hepatická encefalopatia) treba liečbu ihneď prerušiť. Veľmi zriedka sa zaznamenalo ťažké hepatické poškodenie, ktoré sa môže objaviť počas prvých 6 mesiacov liečby nezávisle od úrovne dávkovania.
Poruchy pečene a žlčových ciest:Riziko rozvoja fatálnej hepatotoxicity bolo značne zvýšené u detí mladších ako 2 roky, ktoré dostali kombinovanú antiepileptickú terapiu alebo mali vrodené metabolické poruchy, ťažké záchvaty a boli mentálne retardované alebo u detí s organickými mozgovými léziami.
Veľmi zriedkavo boli zaznamenané i prípady ochorení pankreasu (akútna pankreatitída) s vysokými hladinami plazmatických amyláz a lipáz a podobnými ťažkosťami.
Poruchy ciev:Môžu sa objaviť edémy.
Poruchy reprodukčného systému a prsníkov:Zriedkavo poruchy menštruácie a galaktorea.
4. 9 Predávkovanie Akútne predávkovanie vedie ku kóme spojenej s hyporeflexiou a areflexiou a s centrálnym respiračným útlmom.
Ako liečbu možno skúsiť výplach žalúdka, podávanie aktívneho uhlia a zavedenie hemoperfúzie. Respirátor sa má použiť len v podmienkach intenzívnej starostlivosti. Úspešne bol použitý naloxon ako antidotum.
5. FARMAKOLOGICKÉ VLASTNOSTI 5. 1 Farmakodynamické vlastnosti '
Farmakoterapeutická skupina: antiepileptikumATC kód: N03AG01Kyselina valproová je nasýtená jednoducho rozvetvená mastná kyselina, čím sa odlišuje štruktúrou od ostatných cyklických antiepileptických liekov. Farmakologický účinok kyseliny valproovej je pravdepodobne spôsobený jej pôsobením na metabolizmus kyseliny gammaaminomaslovej (GABA). Aktivácia dekarboxylázy kyseliny glutámovej a inhibícia GABA transaminázy vedie k silnému zvýšeniu koncentrácie GABA v synaptozómoch a v intersynaptickej štrbine. Ako inhibičný neurotransmiter GABA tlmí pre- a postsynaptické výboje, a tým zabraňuje šíreniu záchvatovej aktivity. Psychotropná aktivita kyseliny valproovej vedie k lepšej vizuomotorickej koordinácii a zvýšenej koncentrácii.
5. 2 Farmakokinetické vlastnosti Distribúcia je obmedzená hlavne do krvi s rýchlou výmenou do extracelulárnej tekutiny.
Účinná dávka sa resorbuje v gastrointestinálnom trakte. Vrchol plazmatických hladín sa dosahuje 1 - 3 hodiny po podaní. Súčasný príjem potravy nemá vplyv na množstvo absorbovanej účinnej látky. Rovnovážny stav (steady state) plazmatických hladín sa dosahuje o 2 - 4 dni v závislosti od intervalov dávkovania. Terapeutický rozsah leží väčšinou medzi 50 - 100 mg/l (približne 300 - 600 µmol/l).
80 - 95 % kyseliny valproovej sa viaže na plazmatické proteíny.
Koncentrácie kyseliny valproovej v likvore dobre korelujú s voľným podielom účinnej látky v plazme.
Len 1 - 3 % podanej dávky sa vylúčia nezmenené obličkami. Prevažná časť podlieha glukuronizácii a oxidácii v pečeni. Metabolity sa vylučujú obličkami. Plazmatický polčas eliminácie kolíše individuálne medzi 9 - 16 hodinami a je zvýšený u pacientov s hepatálnym poškodením.
Pre svoju príjemnú chuť sa sirup Convulex používa hlavne na liečbu malých detí.
Sirup Convulex obsahuje lykasín, náhradu cukru, ktorý nie je odbúravaný na kyseliny cukru kyselinotvornými baktériami a preto nemôže podporne pôsobiť na zubný kaz.
5. 3 Predklinické údaje o bezpečnosti Štúdie na zvieratách dokázali, že kyselina valproová má teratogénny potenciál. Pri dávkach vysoko prevyšujúcich ľudskú terapeutickú dávku sa pozorovali abnormality skeletu u mláďat myší a potkanov. Primárne zasahujú rebrá a stavce, ale tiež sa vyskytli faciálne dysmorfie a defekty neurálnej trubice. Štúdie chronickej toxicity pri dávkach väčších ako 250 mg/kg u potkanov a väčších ako 90 mg/kg u psov demonštrujú testikulárnu atrofiu, degeneráciu ductus deferens a insuficientnú spermatogenézu ako aj patologické zmeny v pľúcach a v prostate.
Testy mutagenity u baktérií a u potkanov a myší boli negatívne. Dlhodobé štúdie kancerogenity sa robili u potkanov a myší. Potkaní samci, ktorí dostávali extrémne vysoké dávky, mali zvýšený výskyt subkutánnych fibrosarkómov.
6. FARMACEUTICKÉ INFORMÁCIE 6. 1 Zoznam pomocných látok natrii hydroxidum, lycasinum, methylis hydroxybenzoas (methylparabenum), propylis hydroxybenzoas (propylparabenum), saccharinum natricum, natrii cyclamas, natrii chloridum, raspberry flavour, peach flavour, aqua purificata
6. 2 Inkompatibility Neaplikovateľné.
6. 3 Čas použiteľnosti 60 mesiacov.
Čas použiteľnosti po prvom otvorení: 6 mesiacov
6. 4 Špeciálne upozornenia na uchovávanie Uchovávajte v suchu pri teplote do 25 °C, v pôvodnom obale na ochranu pred svetlom.
6. 5 Druh obalu a obsah balenia Fľaša z hnedého skla, kalibrovaný dávkovač, písomná informácia pre používateľov, papierová škatuľka.
Veľkosť balenia: 100 ml alebo 300 ml
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekomMiesto na odčítanie dávky

õpiest
| 
| 
| 
|
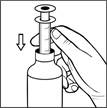
1. Zatlačte piest na doraz do
striekačky a vložte striekačku do fľaše.
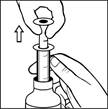
| 2. Vytiahnite piest smerom hore, kým
nedosiahnete značku predpísaného množstva lieku (dávkovanie je vyznačené v ml aj v mg). Zopakujte procedúru ak je nutné, kým dosiahnete celkové požadované množstvo sirupu.
| 3. Stlačením piestu dole aplikujte
predpísané množstvo priamo do úst dieťaťa alebo použite lyžicu alebo pohár. Uistite sa, že celá predpísaná dávka bola podaná.
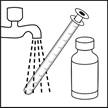
| 4. Po každom použití uzavrite fľašu a
dôkladne očistite striekačku vodou. Skladujte fľašu aj striekačku v originálnom vonkajšom obale lieku.
|
Nepoužitý liek alebo odpad vzniknutý z lieku treba vrátiť do lekárne.
7. Držiteľ rozhodnutia o registrácii G.L. Pharma GmbH
Schlossplatz 1
8502 Lannach
Rakúsko
8. Registračné číslo 21/0037/82 - S
9. DÁTUM PRVEJ REGISTRÁCIE / predĺženia registrácie 1.7.1982 / bez časového obmedzenia
10. Dátum revízie textuMarec 2012