ková dávka Lunaldinu by mala byť 100 mikrogramov a postupne sa zvyšovať v dostupnom rozsahu účinnosti tabliet.
Kým sa nedosiahne optimálna dávka, pacientov treba starostlivo sledovať.
Prechod od iných preparátov, obsahujúcich fentanyl, na Lunaldin sa nesmie urobiť v pomere 1:1, pretože preparáty majú iný absorpčný profil. Ak pacient prejde z iného fentanyl obsahujúceho preparátu, treba proces hľadania optimálnej dávky opakovať.
Odporúčame použiť nasledujúci postup hľadania optimálne dávky, pričom ošetrujúci lekár musí v každom prípade zohľadniť klinické potreby pacienta, jeho vek a sprievodné ochorenia.
Terapia sa u všetkých pacientov začína na jednej 100 mikrogramovej sublingválnej tablete. Ak sa do 15-30 minút od podania jednotlivej sublingválnej tablety nedosiahne primerané potlačenie bolesti, možno podať doplnkovú (druhú) 100 mikrogramovú sublingválnu tabletu. Ak sa dostatočná úľava bolesti nedosiahne v priebehu 15-30 minút od prvej dávky, treba pri ďalšej epizóde akútnej bolesti uvažovať o možnom zvýšení na ďalšiu vyššiu tabletu. (Pozri obrázok nižšie.)
Dávku treba zvyšovať postupne, až kým sa nedosiahne požadované potlačenie bolesti so znesiteľnými vedľajšími účinkami. Pri celkovej dávke 400 mikrogramov a viac, dávku v doplnkovej (druhej) tablete zvyšujte po 100 až 200 mikrogramoch. Ilustruje to rozpis uvedený nižšie. Pri jednej epizóde akútnej bolesti počas optimalizácie dávky nepodávajte viac ako dve (2) dávky.
Titračný proces Lunaldinu Veľkosť dávky (mikrogramy) prvej sublingválnej tablety na epizódu akútnej bolesti
| Veľkosť dávky (mikrogramy) dodatkovej (druhej) sublingválnej tablety podanej po 15-30 minútach po prvej tablete, ak je to potrebné
|
100
| 100
|
200
| 100
|
300
| 100
|
400
| 200
|
600
| 200
|
800
| -
|
Ak sa ani pri vyššej dávke nedosiahne potrebné potlačenie bolesti, ale vedľajšie účinky sú už neprijateľné, možno podať stredne veľkú dávku (podľa potreby 100 mikrogramovú sublingválnu tabletu).
Počas titrácie môžu byť pacienti poučení, aby užívali násobky 100 mikrogramových tabliet a/alebo 200 mikrogramových tabliet pri jednorazovej dávke. Naraz sa nemá užiť viac ako štyri (4) tablety.
V klinických štúdiách u pacientov nebola hodnotená účinnosť a bezpečnosť dávok vyšších ako 800 mikrogramov.
S cieľom minimalizovať riziko výskytu vedľajších reakcií typických pre opiáty a zistiť primeranú dávku, musia byť pacienti počas optimalizácie dávky dôsledne sledovaní profesionálnymi zdravotníckymi pracovníkmi.
Počas titrácie majú pacienti počkať najmenej 2 hodiny, kým užijú Lunaldin na potlačenie ďalšej epizódy akútnej bolesti.
Udržiavacia terapia:Akonáhle bola zistená vhodná jednotlivá dávka, čo môže byť viac ako jedna tableta, pacienta treba na tejto dávke udržovať a celkovú dennú dávku Lunaldinu obmedziť na štyri jednotlivé dávky.
Počas udržiavacieho obdobia majú pacienti počkať najmenej 2 hodiny, kým užijú Lunaldin na potlačenie ďalšej epizódy akútnej bolesti.
Upravenie dávkovania:Ak sa odozva na Lunaldin (analgetický účinok alebo vedľajšie reakcie) významne zmení, dávku bude treba upraviť tak, aby sa opäť dosiahla optimálna dávka.
Ak dochádza počas dňa k viac ako štyrom epizódam akútnej bolesti počas viac ako štyroch za sebou idúcich dní, treba prehodnotiť dávku opiátu s dlhotrvajúcim účinkom pre chronickú bolesť. Ak sa zmení opiát s dlhotrvajúci účinkom, alebo jeho dávkovanie, treba prehodnotiť dávku Lunaldinu, a opäť ju optimalizovať.
Opätovnú optimalizáciu dávky akéhokoľvek analgetika musí sledovať profesionálny zdravotnícky pracovník.
Ukončenie terapie:U pacientov, ktorí už nevyžadujú terapiu opiátmi, sa dávka Lunaldinu musí zohľadniť predtým, ako sa začne postupne znižovať dávka opiátov, aby sa minimalizovali účinky odvykania.
U pacientov, ktorí potrebujú opiátovú terapiu pre chronickú bolesť, ale už nepotrebujú tlmiť akútnu bolesť, je možné liečbu Lunaldinom ukončiť okamžite.
Použitie u detí a mladistvých:Lunaldin sa nesmie používať pre osoby mladšie ako 18 rokov, kvôli chýbajúcim údajom o bezpečnosti a účinnosti.
Použitie u seniorov:Stanovenie optimálnej dávky treba robiť mimoriadne starostlivo a pozorne sledovať pacientov na prejavy otravy fentanylom (pozri časť 4.4).
Používanie u pacientov s poškodenou funkciou pečene a obličiek:Pacientov s obmedzenou funkciou pečene či obličiek treba starostlivo sledovať, či vo fáze optimalizácie dávky neprejavujú príznaky otravy fentanylom (pozri časť 4.4).
4.3 Kontraindikácie
Precitlivenosť na liečivo alebo na niektorú z pomocných látok uvedených v časti 6.1.
Použitie Lunaldinu je kontraindikované u pacientov, ktorí nedostávali opiáty, pretože je tu riziko život ohrozujúcej respiračnej depresie.
Vážne potlačenie dýchacích funkcií alebo vážne blokovanie pľúc.
4.4 Osobitné upozornenia a opatrenia pri používaní
Pacientov, aj ich ošetrujúci personál treba informovať, že obsah aktívnej látky v Lunaldine môže byť smrteľný pre dieťa a tablety preto treba uchovávať mimo dosah a dohľad detí.
Pretože opiátová terapia, napr. Lunaldinom, môže mať potenciálne vážne vedľajšie účinky, pacienti aj ošetrujúci personál si musia byť vedomí dôležitosti správneho používania Lunaldinu a čo treba robiť v prípade, že sa objavia známky predávkovania.
Skôr, ako liečbu Lunaldinom spustíte, musí byť u pacientov stabilizovaná liečba chronickej bolesti pomocou opiátov.
Pri opakovanom podávaní opiátov ako fentanyl sa môže vyvinúť tolerancia alebo fyzická/psychická závislosť. Iatrogénna závislosť po terapeutickom použití opiátov je zriedkavá.
Tak ako u všetkých opiátov, je tu pri používaní Lunaldinu riziko klinicky významnej respiračnej depresie. Mimoriadna opatrnosť sa vyžaduje počas hľadania optimálnej dávky pre pacientov s chronickým blokovaním pľúcnych kanálov alebo trpiacich iným ochorením zvyšujúcim riziko potlačenia respirácie (napr. myastenia gravis), pretože hrozí zhoršenie respiračnej depresie, čo môže viesť až k jej zlyhaniu.
Pri podávaní Lunaldinu buďte mimoriadne opatrní u pacientov, ktorí sú obzvlášť citliví na intrakraniálne efekty hyperkapnie, napríklad u tých, ktorí vykazujú známky zvýšeného intrakraniálneho tlaku, potlačeného vedomia, kómy alebo mozgových nádorov. U pacientov so zraneniami hlavy môžu opiáty maskovať klinický priebeh. V takom prípade použite opiáty, iba ak je to absolútne nevyhnutné.
Bolo preukázané, že intravenózne podanie fentanylu spôsobuje bradykardiu. Lunaldin používajte opatrne u pacientov s bradyarytmiami.
Údaje zo štúdií s intravenóznym fentanylom poukazujú na to, že u starších pacientov je spomalené jeho vylučovanie a tým predĺžený polčas zotrvania v tele a že môžu byť citlivejší na liečivo ako mladí pacienti. Starší, telesne schátraní a chorobou oslabení pacienti musia byť sledovaní na prejavenie sa príznakov toxicity fentanylu a príslušné zníženie dávky.
Lunaldin treba podávať opatrne pacientom s obmedzenou funkciou pečene či obličiek, predovšetkým vo fáze hľadania optimálnej dávky. Ak sa Lunaldin použije u pacientov so zhoršenou funkciou pečene či obličiek, zvýši sa biologická dostupnosť fentanylu a zhorší sa jeho vylúčenie zo systému, čo môže viesť k jeho akumulácii a k výraznejším a predĺženým opiátovým účinkom.
Buďte opatrní pri nasadení Lunaldinu u pacientov s hypervolémiou a hypotenziou.
Lunaldin nebol študovaný u pacientov s ranami v ústach alebo zápalom ústnych slizníc. U takýchto pacientov hrozí riziko zvýšenej systémovej expozície aktívnej látky a preto sa pri hľadaní optimálnej dávky vyžaduje mimoriadna opatrnosť.
Pri ukončení terapie Lunaldinom sa nesmú vyskytnúť pozorovateľné efekty, iba možné symptómy ukončenia podávania, ako úzkosť, triaška, potenie, bledosť, žalúdočné ťažkosti a zvracanie.
4.5 Liekové a iné interakcie
Fentanyl je metabolizovaný CYP3A4. Liečivá, ktoré inhibujú aktivitu CYP3A4, ako napríklad makrolidové antibiotiká (napr. erytromycín), azolové antifungálne preparáty (napr. ketokonazol, itrakonazol) alebo určité inhibítory proteáz (napr. ritonavir) môžu zvýšiť biologickú dostupnosť fentanylu potlačením jeho systémového odbúravania a tým potenciálne predĺžiť, alebo potencovať opiátové účinky. Je známe, že aj grapefruitová šťava inhibuje CYP3A4. Ak sa fentanyl podáva spolu s inhibítormi CYP3A4, treba postupovať opatrne.
Súbežné podávanie iných látok potlačujúcich CNS, ako sú deriváty morfínu (analgetiká a antitusiká), všeobecné anestetiká, relaxanty kostrového svalstva, sedatívne antidepresívne látky, sedatívne H1 antihistaminiká, barbituráty, anxiolytiká (napr. benzdiazepíny), hypnotiká, antipsychotiká, klonidín a príbuzné látky môžu spôsobiť výraznejšie potlačenie CNS. Môže sa vyskytnúť respiračná depresia, hypotenzia a výrazný sedatívny účinok.
Alkohol potenciuje sedatívne účinky morfínových analgetík, preto pri terapii Lunaldinom neodporúčame požívať alkoholické nápoje ani medicínske prípravky obsahujúce alkohol.
Používanie Lunaldinu sa neodporúča u pacientov, ktorým boli v priebehu 14 dní podané inhibítory na báze monoamíno oxidázy (MAO), pretože u MAO inhibítorov je známe, že spôsobujú silné a nepredvídateľné potencovanie ópiových analgetík.
Neodporúča sa súbežné nasadenie čiastočných ópiových agonistov/antagonistov (napr. buprenorfínu, nalbufínu, pentazocínu). Tieto vykazujú vysokú afinitu k opiátovým receptorom s relatívne nízkou vlastnou aktivitou a preto čiastočne antagonizujú analgetický účinok fentanylu a môžu u pacientov závislých od opiátov vyvolať abstinenčné symptómy.
4.6 Fertilita, gravidita a laktácia
Bezpečnosť fentanylu počas tehotenstva nebola zistená. Štúdie na zvieratách preukázali reprodukčnú toxicitu s narušenou fertilitou u potkanov (pozri 5.3). Nie je známe potenciálne riziko u ľudí. Fentanyl sa má nasadzovať počas tehotenstva, iba ak je to nevyhnutné.
Dlhodobá liečba počas tehotenstva môže u novorodenca vyvolať abstinenčné príznaky.
Fentanyl sa nemá používať pred pôrodom a v štádiu pôrodu (vrátane pôrodu cisárskym rezom), pretože fentanyl prechádza placentou a môže u plodu alebo u novorodenca spôsobiť potlačenie dýchania.
Fentanyl je vylučovaný do materského mlieka a môže spôsobiť respiračnú depresiu u dojčeného dieťaťa. Použitie fentanylu u dojčiacich žien je prípustné iba v prípadoch, keď výhody vysoko prevažujú nad potenciálnymi rizikami pre matku a dieťa.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Neuskutočnili sa žiadne štúdie o účinkoch Lunaldinu na schopnosť viesť vozidlá a obsluhovať stroje.
Opiátové analgetiká však môžu negatívne ovplyvniť mentálne aj fyzické schopnosti vykonávať potenciálne nebezpečné činnosti, akými sú vedenie vozidiel a obsluha strojov. Pacienti by nemali viesť vozidlo, ani obsluhovať stroje, ak pociťujú závrat alebo ospalosť, rozmazané alebo dvojité videnie ako dôsledok terapie Lunaldinom.
4.8 Nežiaduce účinky
U Lunaldinu možno očakávať nežiaduce účinky typické pre opiáty; pri dlhšom používaní má ich intenzita klesajúcu tendenciu. K najzávážnejším typicky opiátovým vedľajším účinkom patrí respiračná depresia (ktorá môže viesť až k zastaveniu dýchania), hypotenzia a šok.
Klinické štúdie Lunaldinu boli navrhnuté na hodnotenie bezpečnosti a účinnosti liečby pacientov s akútnou bolesťou pri rakovine; všetci pacienti užívali pre svoje pretrvávajúce bolesti súčasne opiáty, ako morfín s pozvoľným uvoľňovaním, oxykodón s pozvoľným uvoľňovaním alebo transdermálny fentanyl. Preto nie je možné definitívne oddeliť účinky Lunaldinu samotného.
Medzi najčastejšie pozorované nežiaduce reakcie pri Lunaldine patria nežiaduce reakcie typické pre opiáty, ako je nauzea, zápcha, somnolencia a bolesť hlavy.
Prehľadný súhrn nežiaducich reakcií pri Lunaldine:
Nežiaduce reakcie zaznamenané u pacientov v štúdiách bezpečnosti a účinnosti Lunaldinu, s predpokladaným príčinným vzťahom k liečbe a tiež zaznamenané po uvedení lieku na trh, sú uvedené nižšie podľa tried systémových orgánov a frekvencie výskytu (veľmi časté ³ 1/10; časté ³ 1/100 až < 1/10; menej časté ≥1/1000 až <1/100; neznáme (nemožno stanoviť z dostupných dát)). V rámci jednotlivých skupín frekvencií sú nežiaduce účinky usporiadané v poradí klesajúcej závažnosti.
Možnosť priradiť Lunaldinu nežiaduce reakcie v závislosti od dávky je v klinických štúdiách limitovaná použitými titračnými schémami.
Trieda orgánových systémov
| Nežiaduce reakcie podľa frekvencie
|
| veľmi časté ³ 1/10
| časté ³ 1/100 až < 1/10
| menej časté ≥1/1000 až <1/100
| neznáme (nemožno stanoviť z dostupných dát)
|
Poruchy imunitného systému
|
|
| Precitlivenosť
|
|
Poruchy metabolizmu a výživy
|
|
| Anorexia
Znížená chuť do jedla
|
|
Psychiatrické poruchy
|
|
| Depresia
Paranoja
Stav zmätenosti
Dezorientácia
Zmeny duševného stavu
Úzkosť
Euforická nálada
Dysfória
Emocionálna labilita
Porucha koncentrácie
|
|
Poruchy nervového systému
|
| Závrat
Bolesť hlavy
Somnolencia
| Amnézia
Parosmia
Dysgeúzia
Tremor
Letargia
Hypoestézia
Insomnia
Poruchy spánku
|
|
Poruchy oka
|
|
| Zahmlené videnie
|
|
Poruchy srdca a srdcovej činnosti
|
|
| Tachykardia
Bradykardia
|
|
Poruchy ciev
|
|
| Hypotenzia
|
|
Poruchy dýchacej sústavy, hrudníka a mediastína
|
| Dyspnoe
| Orofaryngeálna bolesť
Pocit stiahnutého hrdla
|
|
Trieda orgánových systémov
| Nežiaduce reakcie podľa frekvencie
|
| veľmi časté ³ 1/10
| časté ³ 1/100 až < 1/10
| menej časté ≥1/1000 až <1/100
| neznáme (nemožno stanoviť z dostupných dát)
|
Poruchy gastrointestinálneho traktu
| Nauzea
| Stomatitída
Vracanie
Zápcha
Sucho v ústach
| Vredy v ústach
Gingiválna ulcerácia
Vredy na perách
Porucha vyprázdňovania žalúdka
Bolesť v bruchu
Dyspepsia
Žalúdočný dyskomfort
Poruchy jazyka
Aftózna stomatitída
| 1Opuch jazyka
|
Poruchy kože a podkožného tkaniva
|
| Hyperhidróza
| Lézie na koži
Vyrážka
Alergický pruritus
Pruritus
Nočné potenie
Náchylnosť na tvorbu modrín
|
|
Poruchy kostrovej a svalovej sústavy
a spojivového tkaniva
|
|
| Artralgia
Muskuloskeletálna stuhnutosť
Stuhnutosť kĺbov
| '
|
Poruchy reprodukčného systému a prsníkov
|
|
| Erektilná dysfunkcia
|
|
Celkové poruchy a reakcie v mieste podania
|
| Únava
| Syndróm z vysadenia lieku
Asténia
Nevoľnosť
|
|
Poranenia, otravy a komplikácie liečebného postupu
|
|
| Náhodné predávkovanie
|
|
1 Pozorované iba po uvedení lieku na trh
4.9 Predávkovanie
Symptómy predávkovania fentanylom sú zvýraznením jeho farmakologických účinkov, pričom najzávážnejší z nich je respiračná depresia, ktorá môže viesť až k zastaveniu dýchania.
Okamžité riešenie predávkovania opiátmi zahrňuje vybratie zvyšku sublingválnej tablety z úst, fyzikálnu a verbálnu stimuláciu pacienta a zhodnotenie úrovne vedomia. U pacienta treba udržiavať priechodnosť dýchacích ciest. V prípade potreby treba zasunúť orofaryngálnu alebo endotracheálnu dýchaciu trubicu, podávať kyslík a spustiť mechanickú podporu dýchania. Okrem toho treba udržiavať telesnú teplotu a prívod parenterálnej tekutiny.
Pre riešenie náhodného predávkovania u osôb predtým nevystavených opiátom použite naloxón alebo iného antagonistu opiátov podľa klinickej indikácie a v súlade s ich Súhrnom charakteristických vlastností lieku. Opakované podanie antagonistu opiátov môže byť potrebné, ak sa respiračná depresia predĺži.
Pri riešení predávkovania naloxónom alebo iným antagonistom opiátov u pacientov na opiátoch treba postupovať opatrne, aby sa nespustil akútny abstinenčný syndróm.
Ak dôjde k významnej alebo pretrvávajúcej hypotenzii, treba uvažovať o hypovolémii a situáciu treba riešiť prívodom vhodnej parenterálnej tekutiny.
Svalová stuhnutosť brániaca respirácii bola pozorovaná pri fentanyle a iných opiátoch. V takejto situácii môže byť potrebná endotracheálna intubácia, podpora dýchania a podávanie antagonistov opiátov ako aj svalových relaxantov.
5. farmakologické vlastnosti
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Analgetiká; Opiáty; Deriváty fenylpiperidínu. ATC kód: N02AB03.
Fentanyl je výkonné analgetikum typu µ-opiátu s rýchlym nástupom účinku a krátkym pretrvaním účinku. Fentanyl je asi 100-krát výkonnejšie analgetikum ako morfín. Sekundárne účinky fentanylu na CNS, respiračné a gastrointestinálne funkcie sú typické pre ópiové analgetiká a sú považované za reprezentatívne pre danú triedu preparátov.
Analgetické účinky fentanylu závisia od hladiny aktívnej látky v krvi; u pacientov predtým neliečených opiátmi sa minimálne účinné koncentrácie analgetika v sére pohybujú v rozsahu 0,3-1,2 ng/ml, pričom hladina 10-20 ng/ml v krvi spôsobuje chirurgickú anestéziu a výraznú respiračnú depresiu.
U pacientov trpiacich chronickou rakovinovou bolesťou a udržiavaných na stabilných dávkach opiátov Lunaldin spôsobuje oproti placebu výraznú úľavu od akútnej bolesti po 10 minútach od podania (pozri obrázok1 nižšie) a významne nižšiu potrebu pre záchrannú analgetickú terapiu.
Obrázok 1Stredná odchýlka intenzity bolesti od základnej línie (± SE) pre Lunaldin v porovnaní s placebom (merané 0-10 Lickertovou škálou)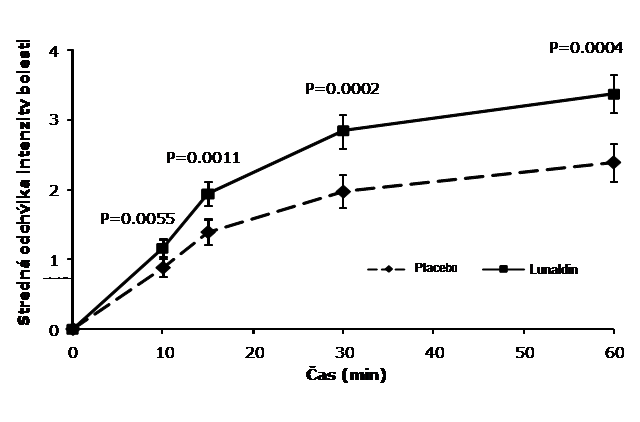
Bezpečnosť a účinnosť Lunaldinu bola hodnotená u pacientov, ktorí ho užívali pri nábehu epizódy akútnej bolesti. Preventívne použitie Lunaldinu pre predvídateľné epizódy akútnej bolesti nebolo v klinických skúškach skúmané.
Fentanyl, podobne ako iní antagonisti µ-ópiového receptora spôsobujú od dávky závislú respiračnú depresiu. Toto riziko je vyššie u pacientov neliečených opiátmi ako u pacientov so silnými bolesťami, alebo pacientov na chronickej terapii opiátmi. Dlhodobá liečba opiátmi vedie k vzniku tolerancie ich sekundárnych účinkov.
Aj keď opiáty obecne zvyšujú tonus hladkých svalov močových ciest, čistý výsledný efekt je variabilný, spôsobujúci v niektorých prípadoch nutkanie na močenie, v iných ťažkosti s močením.
Opiáty zvyšujú tonus a znižujú hnacie kontrakcie hladkého svalstva gastrointestinálneho traktu, čo zvyšuje čas prechodu zažívacím traktom a môže byť príčinou zápchy spôsobenej fentanylom.
5.2 Farmakokinetické vlastnosti
Fentanyl je výrazne lipofilný preparát, rýchlo sa absorbujúci cez sliznicu úst a pomalšie cez gastrointestinálny trakt. Orálne podaný fentanyl podstupuje pri prvom priechode výrazné zmeny pri priechode pečeňou a črevným systémom.
Lunaldin predstavuje rýchlorozpustnú formuláciu sublingválnej tablety. Rýchla absorpcia fentanylu prebehne počas približne 30 minút od podania Lunaldinu. Celková biologická dostupnosť Lunaldinu bola vypočítaná na 54 %. Maximálna stredná koncentrácia fentanylu v plazme sa pohybuje v rozsahu od 0,2 do 1,3 ng/m
l (po podaní 100 až 800 µg Lunaldinu) a dosiahne sa v priebehu 22,5 až 240 minút.
Asi 80-85% fentanylu sa viaže na plazmové proteíny, predovšetkým na a1-glykoproteín a do menšej miery na albumín a lipoproteín. Objemová distribúcia fentanylu v stabilizovanom stave je približne 3-6 l/kg.
Fentanyl sa metabolizuje hlavne účinkom CYP3A4 na niekoľko farmakologicky inaktívnych metabolitov, ku ktorým patrí aj norfentanyl. V priebehu 72 hodín od intravenózneho podania fentanylu je približne 75% dávky vylúčenej do moču, hlavne vo forme metabolitov, pričom nezmenenej aktívnej látky je menej ako 10%. Asi 9% dávky sa vylúči stolicou, hlavne vo forme metabolitov. Celková rýchlosť odbúravania fentanylu z plazmy je asi 0,5 l/h/kg.
Po podaní Lunaldinu je hlavný polčas metabolizovania fentanylu asi 7 hodín (rozpätie hodnôt je 3-12,5 hodín) a konečný polčas metabolizácie je asi 20 hodín (11,5-25 hodín).
Ukázalo sa, že farmakokinetika Lunaldinu je lineárne závislá od dávky v rozsahu dávok 100 až 800 µg. Z farmakokinetických štúdií vyplýva, že pri rovnocennej dávke je podanie viacerých tabliet biologicky rovnocenné s podávaním jednotlivých tabliet.
Poškodenie obličiek/pečeneK zvýšeným koncentráciám v sére môže dôjsť v prípade funkčnej poruchy pečene či obličiek. Starší, zoslabnutí a obecne pacienti v zhoršenom stave vylučujú fentanyl pomalšie, čo spôsobuje dlhší konečný polčas premeny (pozri časti 4.2 a 4.4).
5.3 Predklinické údaje o bezpečnosti
Bezpečnostná farmakológia a údaje toxicity pri opakovaných dávkach nesignalizujú žiadne riziká, ktoré by už neboli pokryté inými časťami tohto Súhrnu charakteristických vlastností lieku. Štúdie na zvieratách ukázali zníženie plodnosti a zvýšenú úmrtnosť potkaních plodov. Teratogénne účinky však objavené neboli.
Testovanie mutagenity na baktériách a hlodavcoch poskytli negatívne výsledky. Podobne ako iné opiáty, fentanyl spôsobuje
in vitro mutagenitu cicavčích buniek. Riziko mutagenity však v klinickom použití vyzerá nepravdepodobne, pretože účinky sa prejavujú až pri veľmi vysokých koncentráciách.
Dlhodobé štúdie karcinogenity neboli robené.
6. Farmaceutické informácie
6.1 Zoznam pomocných látok
Manitol (E421)
Oxidom kremičitým impregnovaná mikrokryštalická celulóza
Sodná soľ kroskarmelózy
Magnézium-stearát
6.2 Inkompatibility
Neaplikovateľné.
6.3 Čas použiteľnosti
3 roky.
6.4 Špeciálne upozornenia na uchovávanie
Uchovávajte pri teplote neprevyšujúcej 25°C.
Uchovávajte v pôvodnom obale blistra, na ochranu pred vlhkosťou.
6.5 Druh obalu a obsah balenia
Sublingválne tablety Lunaldin sú balené v detských bezpečnostných blistroch OPA/alumínium/PVC s fóliou papier/polyester/aluminium uložených v kartónovej škatuľke. Každé balenie má farebne kódovanú účinnosť sublingválnych tabliet.
Veľkosť balenia: Balenie 10 a 30 sublingválnych tabliet. Nie všetky veľkosti balenia musia byť uvedené do obehu.
6.6 Špeciálne opatrenia na likvidáciu
Odpad je potrebné bezpečne zlikvidovať. Pacientov/ošetrujúce osoby treba viesť k tomu, aby nepoužité lieky vrátili do lekárne, kde budú zlikvidované v súlade s národnými a miestnymi predpismi.
7. Držiteľ rozhodnutia o registrácii
Gedeon Richter Plc.
1103 Budapešť
Gyömrői út 19-21
Maďarsko
8. REGISTRAČNÉ ČÍSLA
Lunaldin 100 mikrogramov sublingválne tablety: 65/0130/09-S
Lunaldin 200 mikrogramov sublingválne tablety: 65/0131/09-S
Lunaldin 300 mikrogramov sublingválne tablety: 65/0132/09-S
Lunaldin 400 mikrogramov sublingválne tablety: 65/0133/09-S
Lunaldin 600 mikrogramov sublingválne tablety: 65/0134/09-S
Lunaldin 800 mikrogramov sublingválne tablety: 65/0135/09-S
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE
28.5.2009
10. dátum revízie textu 10/2012