
stredné alergické reakcie na inzulín sú zriedkavé. Takéto reakcie na inzulín (vrátane inzulínu
glargín) alebo na pomocné látky môžu byť spojené napríklad s generalizovanými kožnými reakciami, angioedémom, bronchospazmom, hypotenziou a šokom a môžu ohroziť život.
Podávanie inzulínu môže spôsobiť tvorbu protilátok. V klinických štúdiách sa pozorovali protilátky vykazujúce skrížené reakcie s ľudským inzulínom a inzulínom glargín rovnako v skupine pacientov liečených NPH inzulínom, ako aj v skupine pacientov liečených inzulínom glargín. V zriedkavých prípadoch si môže prítomnosť týchto inzulínových protilátok vyžiadať úpravu dávok inzulínu, aby sa upravil sklon ku hyper- alebo hypoglykémii.
Poruchy oka
Výrazné zmeny glykemickej kontroly môžu dočasne zhoršiť zrak tým, že sa prechodne zmení
zdurenie a refrakčný index šošovky.
Dlhodobo zlepšená glykemická kontrola zmenšuje riziko progresie diabetickej retinopatie. Avšak zintenzívnenie inzulínovej liečby s náhlym zlepšením glykemickej kontroly môže sprevádzať dočasné zhoršenie diabetickej retinopatie. U pacientov s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou, môžu ťažké hypoglykemické príhody vyústiť do prechodnej amaurózy.
Poruchy kože a podkožného tkaniva
Rovnako ako pri každej inzulínovej liečbe sa môže v mieste injekcie vyskytnúť lipodystrofia, ktorá
vedie k oneskorenej lokálnej absorpcii inzulínu. Priebežné striedanie miesta injekcie v rámci určitej injekčnej oblasti môže pomôcť znížiť alebo zabrániť takýmto reakciám.
Celkové poruchy a reakcie v mieste podania
K reakciám v mieste podania injekcie patrí sčervenanie kože, bolesť, svrbenie, žihľavka, opuch alebo
zápal. Väčšina miernych reakcií na inzulín v mieste injekcie obvykle vymizne za niekoľko dní až týždňov.
Inzulín môže zriedkavo spôsobiť retenciu sodíka a opuch, najmä ak sa pôvodne slabá metabolická kontrola zlepšila intenzifikovanou inzulínovou liečbou.
Pediatrickí pacienti
Vo všeobecnosti bezpečnostný profil u detí a dospievajúcich vo veku ≤ 18 rokov je podobný
bezpečnostnému profilu u dospelých.
Správy o nežiaducich reakciách z postmarketingového sledovania zahŕňali u detí a dospievajúcich vo veku ≤ 18 rokov) pomerne častejšie reakcie v mieste vpichu (bolesť v mieste vpichu, reakcie v mieste vpichu) a kožné reakcie (vyrážka, urtikária) ako u dospelých (vek > 18 rokov).
Nie sú dostupné žiadne klinické štúdie s údajmi o bezpečnosti u detí mladších ako 6 rokov.
4.9 Predávkovanie
Príznaky
Predávkovanie inzulínom môže viesť k ťažkej a niekedy dlhotrvajúcej a život ohrozujúcej
hypoglykémii.
Liečba
Mierne hypoglykemické príhody sa obvykle liečia perorálnymi sacharidmi. Môže byť potrebná úprava
dávky lieku, jedálneho lístka alebo telesnej aktivity.
Závažnejšie príhody spojené s kómou, kŕčmi alebo neurologickým poškodením možno liečiť intramuskulárnym alebo subkutánnym podaním glukagónu alebo intravenóznym podaním koncentrovanej glukózy. Keďže hypoglykémia sa po zdanlivom klinickom zotavení môže vrátiť, pacient musí udržiavať príjem sacharidov a je nutné pacienta pozorovať.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Lieky používané na liečbu diabetu. Inzulíny a injekčné analógy, dlhopôsobiace.
ATC kód: A10A E04.
Inzulín glargín je ľudský inzulínový analóg vyvinutý tak, aby mal nízku rozpustnosť v neutrálnom pH. Je úplne rozpustný v injekčnom roztoku Lantusu s kyslým pH (pH 4). Po injekcii do podkožného tkaniva sa kyslý roztok neutralizuje, následkom čoho sa tvoria mikroprecipitáty, z ktorých sa priebežne uvoľňuje v malých množstvách inzulín glargín, čím sa zaisťuje hladký a predvídateľný profil priebehu koncentrácie v závislosti od času bez vrcholov s predĺženým trvaním účinku.
Väzba inzulínu na receptory: Vzhľadom na väzbovú kinetiku receptorov inzulínu sa inzulín glargín veľmi podobá ľudskému inzulínu. Preto možno hovoriť o tom istom spôsobe účinku cez receptory inzulínu ako u ľudského inzulínu.
Primárny účinok inzulínov, vrátane inzulínu glargín, je regulácia glukózového metabolizmu. Inzulín a jeho analógy znižujú hladinu krvnej glukózy stimuláciou periférneho vychytávania glukózy, najmä kostrovým svalstvom a tukom a inhibíciou tvorby glukózy v pečeni. Inzulín inhibuje lipolýzu
v adipocytoch, inhibuje proteolýzu a zvyšuje syntézu proteínov.
V klinických farmakologických štúdiách sa ukázalo, že intravenózny inzulín glargín a ľudský inzulín sú pri rovnakých dávkach rovnocenné. Telesná aktivita a iné premenné môžu ovplyvňovať časový priebeh účinku inzulínu glargín rovnako ako pri všetkých inzulínoch.
V euglykemických uzatvorených štúdiách so zdravými dobrovoľníkmi alebo pacientmi s diabetes
1. typu, bol nástup účinku subkutánneho inzulínu glargín pomalší ako u ľudského NPH inzulínu, jeho profil účinku bol hladký, bez vrcholov a s predĺženým trvaním účinku.
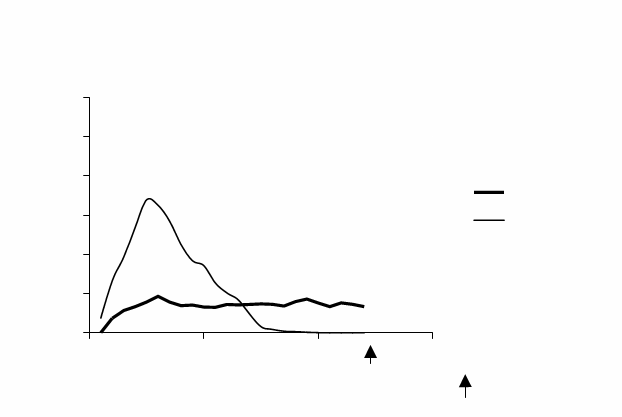
Nasledujúci graf zobrazuje výsledky štúdie u pacientov:
Profil účinku u pacientov s diabetes typu I
6
5
4
inzulín glargín
3 NPH inzulín
2
1
0
0 10 20 30
čas (h) po s.c. injekcii
ukončenie pozorovania





∗ udáva sa ako množstvo infundovanej glukózy na udržanie konštantných plazmatických hladín glukózy (priemerné hodinové hodnoty).
Dlhšie trvanie účinku podkožne podaného inzulínu glargín priamo súvisí s jeho nižšou absorpčnou rýchlosťou a umožňuje podávanie raz denne. Časový priebeh účinku inzulínu a inzulínových analógov, ako je inzulín glargín, sa môže značne líšiť u rôznych jedincov alebo u toho istého jedinca.
Príznaky hypoglykémie alebo hormonálnych odpovedí kontraregulácie boli v klinickej štúdii podobné po intravenóznom podaní inzulínu glargín a ľudského inzulínu u zdravých dobrovoľníkov aj u pacientov s diabetes 1. typu.
Účinky inzulínu glargín (podávaný jedenkrát denne) na diabetickú retinopatiu sa vyhodnocovali v otvorenej 5 -ročnej štúdii kontrolovanej NPH (NPH podávaný dvakrát denne) u 1024 pacientov s diabetom 2. typu, u ktorých bola zistená progresia retinopatie o 3 stupne a viac na základe
vyhodnocovania snímky očného pozadia podľa škály Early Treatment Diabetic Retinopathy Study (ETDRS). Pri porovnaní inzulínu glargín s NPH inzulínom sa nepozoroval žiadny významný rozdiel v progresii diabetickej retinopatie.
Pediatrická populáciaV randomizovanej, kontrolovanej klinickej štúdii boli pediatrickí pacienti (vo veku od 6 do 15 rokov) s diabetom 1. typu (n = 349) liečení po dobu 28 týždňov v inzulínovom režime bazál-bolus, kde bol použitý bežný ľudský inzulín pred každým jedlom. Inzulín glargín sa podával jedenkrát denne pred spaním a NPH ľudský inzulín sa podával jedenkrát alebo dvakrát denne. V obidvoch liečených
skupinách sa pozorovali podobné účinky na glykohemoglobín a výskyt symptomatickej
hypoglykémie, avšak hladina plazmatickej glukózy nalačno klesla z východiskovej hodnoty viac v skupine s inzulínom glargin ako v skupine s NPH. V skupine s inzulínom glargín bola taktiež menej častý výskyt ťažkej hypoglykémie. 143 pacientov liečených inzulínom glargín v tejto štúdii pokračovalo v liečbe inzulínom glargín v nekontrolovanom predĺžení štúdie pričom sledovanie trvalo priemerne 2 roky. Počas tejto predĺženej liečby inzulínom glargín sa nezaznamenali žiadne nové signály týkajúce sa bezpečnosti.
Taktiež sa uskutočnila „crossover“ štúdia (so skríženým dizajnom) porovnávajúca liečbu inzulínom glargín plus inzulín lispro s liečbou inzulínom NPH plus bežný ľudský inzulín (každá liečba sa podávala 16 týždňov v náhodnom poradí) u 26 dospievajúcich vo veku 12 až 18 rokov s diabetom
1. typu. Rovnako ako vo vyššie uvedenej pediatrickej štúdii pokles hladiny plazmatickej glukózy nalačno z východiskovej hodnoty bol väčší v skupine s inzulínom glargín ako v skupine s NPH.
Zmeny HbA1c z východiskovej hodnoty boli v obidvoch liečených skupinách podobné; hodnoty hladiny glukózy v krvi zaznamenané počas noci boli významne vyššie v skupine inzulín glargín / lispro ako v skupine NPH/bežný ľudský inzulín, s priemernou najnižšou hodnotou (nadir) 5,4 mmol/l oproti 4,1 mmol/l. Tomu zodpovedal výskyt nočnej hypoglykémie, ktorý bol 32 % v skupine inzulín glargín / lispro oproti 52 % v skupine NPH / bežný ľudský inzulín.
5.2 Farmakokinetické vlastnosti
U zdravých jedincov a diabetikov ukázali sérové koncentrácie inzulínu pomalšiu a dlhšiu absorpciu a po subkutánnej injekcii inzulínu glargín v porovnaní s ľudským NPH inzulínom chýba vrchol. Koncentrácie teda zodpovedali časovému profilu farmakodynamického účinku inzulínu glargín. Vyššie uvedený graf ukazuje profily farmakodynamického účinku inzulínu glargín a NPH inzulínu.
Inzulín glargín podaný raz denne dosiahne hladiny rovnovážneho stavu za 2-4 dni po prvej dávke. Pri intravenóznom podaní je polčas eliminácie inzulínu glargín a ľudského inzulínu porovnateľný.
U ľudí sa inzulín glargín čiastočne degraduje v podkožnom tkanive v uhlíkovom zakončení beta reťazca a tvoria sa účinné metabolity 21A-gly-inzulín a 21A-gly-des-30B-Thr-inzulín.
V plazme je taktiež prítomný nezmenený inzulín glargín a produkty degradácie.
V klinických štúdiách sa v jednotlivých podskupinách rozdelených podľa veku a rodu nezistili žiadne rozdiely v bezpečnosti a účinnosti pri liečbe inzulínom glargín v porovnaní s celkovou študovanou populáciou.
Paediatrická populácia
Špecifická farmakokinetická štúdia na deťoch alebo dospievajúcich sa nerobila.
5.3 Predklinické údaje o bezpečnosti
Predklinické údaje získané na základe obvyklých farmakologických štúdií bezpečnosti, toxicity po opakovanom podaní, genotoxicity, karcinogénneho potenciálu a reprodukčnej toxicity neodhalili žiadne osobitné riziko pre ľudí.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
5 ml injekčná liekovka chlorid zinočnatý, metakrezol,
glycerol,
kyselina chlorovodíková, hydroxid sodný,
voda na injekciu.
10 ml injekčná liekovka chlorid zinočnatý, metakrezol,
glycerol,
kyselina chlorovodíková, polysorbát 20,
hydroxid sodný, voda na injekciu.
6.2 Inkompatibility
Tento liek sa nesmie miešať so žiadnymi inými liekmi. Je dôležité zabezpečiť, aby injekčné striekačky neobsahovali stopy žiadnych iných látok.
6.3 Čas použiteľnosti
2 roky.
Čas použiteľnosti po prvom použití injekčnej liekovky
Liek sa môže uchovávať maximálne 4 týždne pri teplote neprevyšujúcej 25°C tak, aby nebol vystavený priamemu teplu ani priamemu svetlu. Uchovávajte injekčnú liekovku vo vonkajšom obale na ochranu pred svetlom.
Dátum prvého použitia injekčnej liekovky sa odporúča zaznamenať na štítku.
6.4 Špeciálne upozornenia na uchovávanie
Neotvorené injekčné liekovky Uchovávajte v chladničke (2 °C–8 °C). Neuchovávajte v mrazničke.
Nedávajte Lantus blízko mraziacej časti ani zmrazeného balenia.
Uchovávajte injekčnú liekovku vo vonkajšom obale na ochranu pred svetlom.
Otvorené injekčné liekovky:
Upozornenia na uchovávanie, pozri časť 6.3.
6.5 Druh obalu a obsah balenia
5 ml roztoku v injekčnej liekovke (bezfarebné sklo typu I) s tesniacim krytom (hliník), zátkou
(chlorobutylová guma typu I) a odlamovacím krytom (polypropylén). Dostupné sú balenia 1, 2, 5 a 10 injekčných liekoviek.
10 ml roztoku v injekčnej liekovke (bezfarebné sklo typu I) s tesniacim krytom (hliník), zátkou (guma typu I z polyizoprénového laminátu a bromobutylu) a odlamovacím krytom (polypropylén). Dostupné sú balenia po 1 injekčnej liekovke.
Nie všetky veľkosti balenia musia byť uvedené na trh.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Pred použitím skontrolujte injekčnú liekovku. Môže sa použiť len ak je roztok číry, bezfarebný, bez viditeľných tuhých častíc a len ak má konzistenciu podobnú vode. Keďže Lantus je roztok, nevyžaduje pred použitím resuspenzáciu.
Lantus sa nesmie miešať so žiadnym iným inzulínom a nesmie sa ani riediť. Miešanie alebo riedenie môže zmeniť jeho čas/profil účinku a miešanie môže spôsobiť precipitáciu.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Sanofi-Aventis Deutschland GmbH, D-65926 Frankfurt am Main, Nemecko.
8. REGISTRAČNÉ ČÍSLA
EU/1/00/134/001-004
EU/1/00/134/012
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIEDátum prvej registrácie: 9. jún 2000
Dátum posledného predĺženia: 9. jún 2010
10. DÁTUM REVÍZIE TEXTUPodrobné informácie o tomto lieku sú dostupné na internetovej stránke Európskej liekovej agentúry
http://www.ema.europa.eu/.
1. NÁZOV LIEKU
Lantus 100 jednotiek/ml injekčný roztok v náplni
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Každý ml obsahuje 100 jednotiek inzulínu glargín (zodpovedá 3,64 mg). Každá náplň obsahuje 3 ml injekčného roztoku, čo zodpovedá 300 jednotkám. Inzulín glargín sa vyrába rekombinantnou DNA technológiou v Escherichia coli. Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčný roztok.
Číry, bezfarebný roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Liečba dospelých, adolescentov a detí vo veku 6 rokov a starších s diabetom mellitus, kde sa vyžaduje liečba inzulínom.
4.2 Dávkovanie a spôsob podávania
Dávkovanie
Lantus obsahuje inzulín glargín, analóg inzulínu a mápredĺžené trvanie účinku.
Lantus sa má podávať raz denne, kedykoľvek počas dňa, ale každý deň v tom istom čase.
Dávkovacia schéma Lantusu (dávka a čas podania) sa musí prispôsobiť individuálne. Pacientom s diabetes mellitus 2. typu sa môže podávať Lantus spolu s perorálnymi antidiabetikami. Účinnosť tohto lieku je daná v jednotkách. Tieto jednotky sú špecifické len pre Lantus a nie sú rovnaké ako IU alebo jednotky, ktoré sa používajú na vyjadrenie účinnosti iných inzulínových analógov. Pozri časť 5.1.
Populácia starších pacientov (≥ 65 rokov)
U starších pacientov môže progresívne zhoršovanie renálnej funkcie viesť k stálemu poklesu nárokov na inzulín.
Zhoršená renálna funkcia
U pacientov so zhoršenou renálnou funkciou môžu byť nároky na inzulín znížené z dôvodu zníženého inzulínového metabolizmu.
Zhoršená funkcia pečene
U pacientov so zhoršenou funkciou pečene môžu byť nároky na inzulín znížené z dôvodu zníženej kapacity pre glukoneogenézu a zníženého inzulínového metabolizmu.
Pediatrická populácia
Bezpečnosť a účinnosť Lantusu bola stanovená u dospievajúcich a detí vo veku 6 rokov a starších.
U detí sa účinnosť a bezpečnosť Lantusu preukázala iba pri podávaní večer. Vzhľadom
k obmedzeným skúsenostiam s účinnosťou a bezpečnosťou Lantusu u detí mladších ako 6 rokov sa má Lantus podávať v tejto vekovej skupine pod dôsledným lekárskym dohľadom.
Prechod z iných inzulínov na Lantus
Zmena liečebného režimu zo strednodobo alebo dlhodobo pôsobiaceho inzulínu na režim s Lantusom
si môže vyžiadať zmenu dávky bazálneho inzulínu a úpravu sprievodnej antidiabetickej liečby (dávok a časovania prídavných bežných inzulínov alebo rýchlo pôsobiacich analógov inzulínu alebo dávok perorálnych antidiabetík).
Pacienti, ktorí menia režim bazálneho inzulínu z NPH dvakrát denne na režim Lantus jedenkrát denne, musia v prvých týždňoch liečby znížiť dennú dávku bazálneho inzulínu o 20-30 %, aby sa zmenšilo riziko nočnej alebo skorej rannej hypoglykémie. Toto zníženie dávky počas prvých týždňov sa má aspoň čiastočne kompenzovať zvýšením prandiálneho inzulínu, po uplynutí tohto času sa režim má individuálne upraviť.
Pacienti, ktorí užívajú veľké dávky inzulínu, môžu pocítiť pri Lantuse zlepšenú inzulínovú odpoveď, rovnako ako pri iných analógoch inzulínu. Príčinou sú protilátky proti ľudskému inzulínu.
Pri prechode a v prvých týždňoch po ňom sa odporúča starostlivé sledovanie metabolizmu.
So zlepšením metabolickej kontroly a následným zvýšením citlivosti na inzulín môže byť potrebná ďalšia úprava dávky. Úpravu dávky si môže vyžiadať napríklad aj zmena pacientovej hmotnosti a/alebo životného štýlu, zmena času podania dávky inzulínu alebo iné okolnosti, ktoré zvyšujú náchylnosť na hypoglykémiu alebo na hyperglykémiu (pozri časť 4.4).
Spôsob podávania
Lantus sa podáva subkutánne.
Lantus sa nemá podávať intravenózne. Predĺžený účinok Lantusu závisí od jeho aplikácie do subkutánneho tkaniva. Intravenózne podanie dávky, ktorá sa obvykle podáva subkutánne, by mohlo spôsobiť ťažkú hypoglykémiu.
Po podaní Lantusu do brušnej steny, deltového svalu alebo do stehna nie sú klinicky významné rozdiely v hladinách glukózy alebo inzulínu v sére. Miesta podania injekcie sa musia v rámci danej oblasti meniť po každom podaní.
Lantus sa nesmie miešať so žiadnym iným inzulínom ani riediť. Miešanie alebo riedenie môže zmeniť
jeho časový profil účinku a miešanie môže spôsobiť precipitáciu. Podrobnejšie o zaobchádzaní s liekom, pozri časť 6.6.
4.3 Kontraindikácie
Precitlivenosť na liečivo alebo na ktorúkoľvek z pomocných látok.
4.4 Osobitné upozornenia a opatrenia pri používaní
Lantus nie je inzulín voľby na liečbu diabetickej ketoacidózy. Namiesto toho, sa v takýchto prípadoch odporúča intravenózne podať bežný inzulín.
V prípade nedostatočnej glukózovej kontroly alebo náchylnosti na hyper- alebo hypoglykemické príhody sa musí ešte pred zvážením úpravy dávok prehodnotiť ako pacient dodržiava predpísaný liečebný režim, injekčné miesta, správnu techniku aplikácie injekcií a iné významné faktory.
Prestavenie pacienta na iný typ alebo druh inzulínu sa musí robiť pod prísnym lekárskym dohľadom. Zmena sily, druhu (iný výrobca), typu (bežný, NPH, lente, s dlhotrvajúcim účinkom, atď.), pôvodu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo výrobného postupu môže mať za následok to, že je potrebné zmeniť dávku.
Podávanie inzulínu môže spôsobiť tvorbu protilátok. V zriedkavých prípadoch si môže prítomnosť týchto inzulínových protilátok vyžiadať úpravu dávok inzulínu, aby sa upravil sklon ku hyper- alebo hypoglykémii. (pozri časť 4.8.)
Hypoglykémia
Čas výskytu hypoglykémie závisí od profilu účinku použitých inzulínov a preto sa môže zmeniť pri
zmene liečebného režimu. V dôsledku dlhšie pretrvávajúcej suplementácie bazálneho inzulínu pri liečbe Lantusom možno očakávať menej nočnej hypoglykémie, ale viac skorej rannej hypoglykémie.
Vyžaduje sa mimoriadna opatrnosť a intenzívne monitorovanie krvnej glukózy sa odporúča
u pacientov, pre ktorých môžu byť hypoglykemické príhody obzvlášť klinicky významné, ako sú napríklad pacienti so signifikantnou stenózou koronárnych artérií alebo krvných ciev zásobujúcich mozog (riziko srdcových alebo mozgových hypoglykemických komplikácií), ako aj pacienti
s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou (riziko prechodnej amaurózy po hypoglykémii).
Pacienti majú byť upozornení na okolnosti, kedy sa varovné príznaky hypoglykémie zmenšujú. Varovné príznaky hypoglykémie sa môžu meniť, môžu byť menej výrazné alebo u určitých rizikových skupín môžu chýbať. Patria sem pacienti:
- s nápadne zlepšenou glykemickou kontrolou,
- s pozvoľným nástupom hypoglykémie,
- staršieho veku,
- po prechode zo zvieracieho na ľudský inzulín,
- s autonómnou neuropatiou v súčasnosti,
- s dlhodobou anamnézou cukrovky,
- s psychiatrickým ochorením,
- dostávajúci sprievodnú liečbu niektorými inými liekmi (pozri časť 4.5).
Tieto okolnosti môžu spôsobiť ťažkú hypoglykémiu (a možnú stratu vedomia) skôr, ako si pacient hypoglykémiu uvedomí.
Predĺžený účinok subkutánne podaného inzulínu glargín môže oneskoriť zotavenie sa po hypoglykémii.
Ak sa zistia normálne alebo znížené hodnoty glykovaného hemoglobínu, musí sa vziať do úvahy možnosť rekurentných nerozpoznaných (najmä nočných) príhod hypoglykémie.
Nevyhnutným predpokladom pre zníženie rizika hypoglykémie je to, aby pacient dodržiaval režim dávok a diétny režim, správne podávanie inzulínu a znalosť príznakov hypoglykémie.
Faktory, ktoré zvyšujú náchylnosť na hypoglykémiu, si vyžadujú obzvlášť podrobné sledovanie a môžu si vyžiadať aj úpravu dávok. K nim patria:
- zmena injekčného miesta,
- zlepšená vnímavosť na inzulín (napr. odstránením stresových faktorov),
- neobvyklá, zvýšená alebo predĺžená fyzická aktivita,
- interkurentné ochorenie (napr. vracanie, hnačka),
- neprimeraný príjem potravy,
- vynechanie jedla,
- konzumácia alkoholu,
- určité nekompenzované poruchy endokrinného systému (napr. pri hypotyreóze a pri nedostatočnej činnosti adenohypofýzy alebo kôry nadobličiek),
- súbežná liečba niektorými inými liekmi.
Interkurentné ochorenie
Interkurentné ochorenie si vyžaduje intenzívnejšie sledovanie metabolizmu. V mnohých prípadoch sa
indikujú močové testy na ketóny a často sa musí upraviť dávku inzulínu. Nároky na inzulín sú často zvýšené. Pacienti s diabetes mellitus 1. typu musia udržiavať pravidelný prísun aspoň malého
množstva sacharidov, aj keď sú schopní jesť len málo alebo vôbec nie, prípadne vracajú a pod. a nikdy nesmú inzulín úplne vynechať.
4.5 Liekové a iné interakcie
Celý rad látok ovplyvňuje glukózový metabolizmus a môže si vyžiadať úpravu dávky inzulínu glargín.
Medzi látky, ktoré môžu zosilňovať účinok znižujúci hladinu cukru v krvi a zvyšujú náchylnosť na hypoglykémiu, patria: perorálne antidiabetiká, inhibítory enzýmu konvertujúceho angiotenzín (ACE), disopyramid, fibráty, fluoxetín, inhibítory monoaminooxidázy (MAO), pentoxifylín, propoxyfén, salicyláty a sulfónamidové antibiotiká.
Medzi látky, ktoré môžu zoslabovať účinok znižujúci hladinu cukru v krvi, patria: kortikosteroidy, danazol, diazoxid, diuretiká, glukagón, izoniazid, estrogény a progestagény, fenotiazínové deriváty, somatotropín, sympatomimetiká (napr. epinefrín [adrenalín], salbutamol, terbutalín), tyroidné hormóny, atypické antipsychotické lieky (napr. klozapín a olanzapín) a inhibítory proteázy.
Betablokátory, klonidín, soli lítia alebo alkohol môžu buď zosilňovať alebo zoslabovať účinok inzulínu znižujúci hladinu cukru v krvi.
Pentamidín môže spôsobiť hypoglykémiu, po ktorej môže niekedy nasledovať hyperglykémia.
Pod vplyvom sympatolytík, ako sú betablokátory, klonidín, guanetidín a rezerpín, sa naviac môžu oslabiť alebo chýbať príznaky adrenergnej kontraregulácie.
4.6 Fertilita, gravidita a laktácia
Gravidita
Z kontrolovaných klinických štúdii nie sú k dispozícii žiadne klinické údaje o gravidných ženách vystavených účinku inzulínu glargín. Údaje o stredne veľkom počte gravidných žien (závery z počtu
300-1000 gravidít) vystavených účinku inzulínu glargín uvádzaného na trh nepreukázali nežiaduce účinky inzulínu glargín na graviditu a nepreukázali malformácie ani toxicitu inzulínu glargín pre plod/novorodenca.
Údaje o zvieratách nepreukázali reprodukčnú toxicitu.
Použitie Lantusu počas gravidity sa môže zvážiť, ak je to nevyhnutné.
Pre pacientky s predtým existujúcou alebo gestačnou cukrovkou je dôležité udržiavanie dobrej metabolickej kontroly počas gravidity. Nároky na inzulín môžu počas prvého trimestra poklesnúť a
v druhom a treťom trimestri všeobecne stúpajú. Okamžite po pôrode nároky na inzulín rapídne klesnú
(zvýšené riziko hypoglykémie). Nevyhnutné je starostlivé sledovanie glykémie.
Dojčenie
Nie je známe, či sa inzulín glargín vylučuje do materského mlieka. Nepredpokladajú sa žiadne metabolické účinky požitého inzulínu glargín na dojčeného novorodenca/dieťa, keďže inzulín glargín ako peptid sa spracováva na aminokyseliny v ľudskom tráviacom trakte. Dojčiacim matkám možno bude treba upraviť dávky inzulínu a diétu.
Fertilita
Štúdie na zvieratách nepreukázali priame škodlivé účinky na fertilitu.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Následkom hypoglykémie alebo hyperglykémie, alebo napríklad ako dôsledok zhoršenia zraku, sa môže zhoršiť pacientova schopnosť sústrediť sa a reagovať. To môže predstavovať riziko
v situáciách, kedy sú tieto schopnosti zvlášť dôležité (napr. vedenie vozidla alebo obsluha strojov).
Pacientom majú byť odporučené také opatrenia, aby sa počas vedenia vozidla vyhli hypoglykémii. To je obzvlášť dôležité pre tých, ktorí majú oslabené alebo chýbajúce varovné príznaky hypoglykémie, alebo majú časté hypoglykemické príhody. Za týchto okolností sa musí zvážiť, či je vhodné viesť vozidlo alebo obsluhovať stroje.
4.8 Nežiaduce účinkyHypoglykémia je vo všeobecnosti najčastejšou nežiaducou reakciou inzulínovej liečby, ktorá sa môže vyskytnúť, ak je dávka inzulínu privysoká vzhľadom na potrebu inzulínu.
Z klinických štúdií vyplynuli nasledujúce nežiaduce účinky, ktoré sú zoradené podľa tried orgánových systémov a v poradí podľa klesajúceho výskytu (veľmi časté: ≥ 1/10; časté: ≥ 1/100 až < 1/10; menej časté: ≥ 1/1000 až < 1/100; zriedkavé: ≥ 1/10 000 až < 1/1000; veľmi zriedkavé: < 1/10 000).
MedDRA triedy orgánových systémov
| Veľmi časté
| Časté
| Menej časté
| Zriedkavé
| Veľmi zriedkavé
| Poruchy
imunitného systému
|
|
|
| Alergické
reakcie
|
| Poruchy metabolizmu a
výživy
| Hypoglykémia
|
|
|
|
| Poruchy
nervového systému
|
|
|
|
| Dysgeúzia
| Poruchy zraku
|
|
|
| Zhoršené
videnie
Retinopatia
|
| Poruchy kože
a podkožného tkaniva
|
| Lipohypertrofia
| Lipoatrofia
|
|
| Poruchy kostrovej
a svalovej sústavy
a spojivového tkaniva
|
|
|
|
| Myalgia
| Celkové poruchy
a reakcie
v mieste podania
|
| Reakcie v mieste
podania injekcie
|
| Edém
|
|
|
|
V rámci jednotlivých skupín frekvencií sú nežiaduce účinky usporiadané v poradí klesajúcej závažnosti.
Poruchy metabolizmu a výživyŤažké ataky hypoglykémie, najmä ak sú rekurentné, môžu spôsobiť neurologické poškodenie.
Dlhotrvajúce alebo ťažké hypoglykemické príhody môžu ohroziť život.
Znakom a príznakom neuroglykopénie predchádzajú u mnohých pacientov znaky adrenergnej kontraregulácie. Všeobecne čím väčší a rýchlejší je pokles krvnej glukózy, tým výraznejší je fenomén kontraregulácie a jej príznakov.
Poruchy imunitného systému
Bezprostredné alergické reakcie na inzulín sú zriedkavé. Takéto reakcie na inzulín (vrátane inzulínu
glargín) alebo na pomocné látky môžu byť spojené napríklad s generalizovanými kožnými reakciami, angioedémom, bronchospazmom, hypotenziou a šokom a môžu ohroziť život.
Podávanie inzulínu môže spôsobiť tvorbu protilátok. V klinických štúdiách sa pozorovali protilátky vykazujúce skrížené reakcie s ľudským inzulínom a inzulínom glargín rovnako v skupine pacientov liečených NPH inzulínom, ako aj v skupine pacientov liečených inzulínom glargín. V zriedkavých prípadoch si môže prítomnosť týchto inzulínových protilátok vyžiadať úpravu dávok inzulínu, aby sa upravil sklon ku hyper- alebo hypoglykémii.
Poruchy oka
Výrazné zmeny glykemickej kontroly môžu dočasne zhoršiť zrak tým, že sa prechodne zmení
zdurenie a refrakčný index šošovky.
Dlhodobo zlepšená glykemická kontrola zmenšuje riziko progresie diabetickej retinopatie. Avšak zintenzívnenie inzulínovej liečby s náhlym zlepšením glykemickej kontroly môže sprevádzať dočasné zhoršenie diabetickej retinopatie. U pacientov s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou, môžu ťažké hypoglykemické príhody vyústiť do prechodnej amaurózy.
Poruchy kože a podkožného tkaniva
Rovnako ako pri každej inzulínovej liečbe sa môže v mieste injekcie vyskytnúť lipodystrofia, ktorá
vedie k oneskorenej lokálnej absorpcii inzulínu. Priebežné striedanie miesta injekcie v rámci určitej injekčnej oblasti môže pomôcť znížiť alebo zabrániť takýmto reakciám.
Celkové poruchy a reakcie v mieste podania
K reakciám v mieste podania injekcie patrí sčervenanie kože, bolesť, svrbenie, žihľavka, opuch alebo
zápal. Väčšina miernych reakcií na inzulín v mieste injekcie obvykle vymizne za niekoľko dní až týždňov.
Inzulín môže zriedkavo spôsobiť retenciu sodíka a opuch, najmä ak sa pôvodne slabá metabolická kontrola zlepšila intenzifikovanou inzulínovou liečbou.
Pediatrickí pacienti
Vo všeobecnosti bezpečnostný profil u detí a dospievajúcich vo veku ≤ 18 rokov je podobný
bezpečnostnému profilu u dospelých.
Správy o nežiaducich reakciách z postmarketingového sledovania zahŕňali u detí a dospievajúcich vo veku ≤ 18 rokov pomerne častejšie reakcie v mieste vpichu (bolesť v mieste vpichu, reakcie v mieste vpichu) a kožné reakcie (vyrážka, urtikária) ako u dospelých (vek > 18 rokov).
Nie sú dostupné žiadne klinické štúdie s údajmi o bezpečnosti u detí mladších ako 6 rokov.
4.9 Predávkovanie
Príznaky
Predávkovanie inzulínom môže viesť k ťažkej a niekedy dlhotrvajúcej a život ohrozujúcej
hypoglykémii.
Liečba
Mierne hypoglykemické príhody sa obvykle liečia perorálnymi sacharidmi. Môže byť potrebná úprava
dávky lieku, jedálneho lístka alebo telesnej aktivity.
Závažnejšie príhody spojené s kómou, kŕčmi alebo neurologickým poškodením možno liečiť intramuskulárnym alebo subkutánnym podaním glukagónu alebo intravenóznym podaním koncentrovanej glukózy. Keďže hypoglykémia sa po zdanlivom klinickom zotavení môže vrátiť, pacient musí udržiavať príjem sacharidov a je nutné pacienta pozorovať.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Lieky používané na liečbu diabetu. Inzulíny a injekčné analógy, dlhopôsobiace.
ATC kód: A10A E04.
Inzulín glargín je ľudský inzulínový analóg vyvinutý tak, aby mal nízku rozpustnosť v neutrálnom pH. Je úplne rozpustný v injekčnom roztoku Lantusu s kyslým pH (pH 4). Po injekcii do podkožného tkaniva sa kyslý roztok neutralizuje, následkom čoho sa tvoria mikroprecipitáty, z ktorých sa priebežne uvoľňuje v malých množstvách inzulín glargín, čím sa zaisťuje hladký a predvídateľný profil priebehu koncentrácie v závislosti od času bez vrcholov s predĺženým trvaním účinku.
Väzba inzulínu na receptory: Vzhľadom na väzbovú kinetiku receptorov inzulínu sa inzulín glargín veľmi podobá ľudskému inzulínu. Preto možno hovoriť o tom istom spôsobe účinku cez receptory inzulínu ako u ľudského inzulínu.
Primárny účinok inzulínov, vrátane inzulínu glargín, je regulácia glukózového metabolizmu. Inzulín a jeho analógy znižujú hladinu krvnej glukózy stimuláciou periférneho vychytávania glukózy, najmä kostrovým svalstvom a tukom a inhibíciou tvorby glukózy v pečeni. Inzulín inhibuje lipolýzu
v adipocytoch, inhibuje proteolýzu a zvyšuje syntézu proteínov.
V klinických farmakologických štúdiách sa ukázalo, že intravenózny inzulín glargín a ľudský inzulín sú pri rovnakých dávkach rovnocenné. Telesná aktivita a iné premenné môžu ovplyvňovať časový priebeh účinku inzulínu glargín rovnako ako pri všetkých inzulínoch.
V euglykemických uzatvorených štúdiách so zdravými dobrovoľníkmi alebo pacientmi s diabetes
1. typu, bol nástup účinku subkutánneho inzulínu glargín pomalší ako u ľudského NPH inzulínu, jeho profil účinku bol hladký, bez vrcholov a s predĺženým trvaním účinku.
Nasledujúci graf zobrazuje výsledky štúdie u pacientov:
Profil účinku u pacientov s diabetes typu I
6
5
4
inzulín glargín

3 NPH inzulín
2
1
0
0 10 20 30
čas (h) po s.c. injekcii
ukončenie pozorovania




∗ udáva sa ako množstvo infundovanej glukózy na udržanie konštantných plazmatických hladín glukózy (priemerné hodinové hodnoty).
Dlhšie trvanie účinku podkožne podaného inzulínu glargín priamo súvisí s jeho nižšou absorpčnou rýchlosťou a umožňuje podávanie raz denne. Časový priebeh účinku inzulínu a inzulínových analógov, ako je inzulín glargín, sa môže značne líšiť u rôznych jedincov alebo u toho istého jedinca.
Príznaky hypoglykémie alebo hormonálnych odpovedí kontraregulácie boli v klinickej štúdii podobné po intravenóznom podaní inzulínu glargín a ľudského inzulínu u zdravých dobrovoľníkov aj u pacientov s diabetes 1. typu.
Účinky inzulínu glargín (podávaný jedenkrát denne) na diabetickú retinopatiu sa vyhodnocovali v otvorenej 5-ročnej štúdii kontrolovanej NPH (NPH podávaný dvakrát denne) u 1024 pacientov s diabetom 2. typu, u ktorých bola zistená progresia retinopatie o 3 stupne a viac na základe
vyhodnocovania snímky očného pozadia podľa škály Early Treatment Diabetic Retinopathy Study (ETDRS). Pri porovnaní inzulínu glargín s NPH inzulínom sa nepozoroval žiadny významný rozdiel v progresii diabetickej retinopatie.
Pediatrická populáciaV randomizovanej, kontrolovanej klinickej štúdii boli pediatrickí pacienti (vo veku od 6 do 15 rokov) s diabetom 1. typu (n = 349) liečení po dobu 28 týždňov v inzulínovom režime bazál-bolus, kde bol použitý bežný ľudský inzulín pred každým jedlom. Inzulín glargín sa podával jedenkrát denne pred
spaním a NPH ľudský inzulín sa podával jedenkrát alebo dvakrát denne. V obidvoch liečených
skupinách sa pozorovali podobné účinky na glykohemoglobín a výskyt symptomatickej hypoglykémie, avšak hladina plazmatickej glukózy nalačno klesla z východiskovej hodnoty viac v skupine s inzulínom glargin ako v skupine s NPH. V skupine s inzulínom glargín bola taktiež menej častý výskyt ťažkej hypoglykémie. 143 pacientov liečených inzulínom glargín v tejto štúdii pokračovalo v liečbe inzulínom glargín v nekontrolovanom predĺžení štúdie pričom sledovanie trvalo priemerne 2 roky. Počas tejto predĺženej liečby inzulínom glargín sa nezaznamenali žiadne nové signály týkajúce sa bezpečnosti.
Taktiež sa uskutočnila „crossover“ štúdia (so skríženým dizajnom) porovnávajúca liečbu inzulínom glargín plus inzulín lispro s liečbou inzulínom NPH plus bežný ľudský inzulín (každá liečba sa podávala 16 týždňov v náhodnom poradí) u 26 dospievajúcich vo veku 12 až 18 rokov s diabetom
1. typu. Rovnako ako vo vyššie uvedenej pediatrickej štúdii pokles hladiny plazmatickej glukózy
nalačno z východiskovej hodnoty bol väčší v skupine s inzulínom glargín ako v skupine s NPH. Zmeny HbA1c z východiskovej hodnoty boli v obidvoch liečených skupinách podobné; hodnoty hladiny glukózy v krvi zaznamenané počas noci boli významne vyššie v skupine inzulín glargín / lispro ako v skupine NPH/bežný ľudský inzulín, s priemernou najnižšou hodnotou (nadir) 5,4 mmol/l oproti 4,1 mmol/l. Tomu zodpovedal výskyt nočnej hypoglykémie, ktorý bol 32 % v skupine inzulín glargín / lispro oproti 52 % v skupine NPH / bežný ľudský inzulín.
5.2 Farmakokinetické vlastnosti
U zdravých jedincov a diabetikov ukázali sérové koncentrácie inzulínu pomalšiu a dlhšiu absorpciu a po subkutánnej injekcii inzulínu glargín v porovnaní s ľudským NPH inzulínom chýba vrchol. Koncentrácie teda zodpovedali časovému profilu farmakodynamického účinku inzulínu glargín. Vyššie uvedený graf ukazuje profily farmakodynamického účinku inzulínu glargín a NPH inzulínu.
Inzulín glargín podaný raz denne dosiahne hladiny rovnovážneho stavu za 2-4 dni po prvej dávke. Pri intravenóznom podaní je polčas eliminácie inzulínu glargín a ľudského inzulínu porovnateľný. U ľudí sa inzulín glargín čiastočne degraduje v podkožnom tkanive v uhlíkovom zakončení beta
reťazca a tvoria sa účinné metabolity 21A-gly-inzulín a 21A-gly-des-30B-Thr-inzulín.
V plazme je taktiež prítomný nezmenený inzulín glargín a produkty degradácie.
V klinických štúdiách sa v jednotlivých podskupinách rozdelených podľa veku a rodu nezistili žiadne rozdiely v bezpečnosti a účinnosti pri liečbe inzulínom glargín v porovnaní s celkovou študovanou populáciou.
Paediatrická populácia
Špecifická farmakokinetická štúdia na deťoch alebo dospievajúcich sa nerobila.
5.3 Predklinické údaje o bezpečnosti
Predklinické údaje získané na základe obvyklých farmakologických štúdií bezpečnosti, toxicity po opakovanom podaní, genotoxicity, karcinogénneho potenciálu a reprodukčnej toxicity neodhalili žiadne osobitné riziko pre ľudí.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
chlorid zinočnatý, metakrezol, glycerol,
kyselina chlorovodíková, hydroxid sodný,
voda na injekciu.
6.2 Inkompatibility
Tento liek sa nesmie miešať so žiadnymi inými liekmi. Je dôležité zabezpečiť, aby injekčné striekačky neobsahovali stopy žiadnych iných látok.
6.3 Čas použiteľnosti
3 roky.
Čas použiteľnosti po prvom použití náplne
Liek sa môže uchovávať maximálne 4 týždne pri teplote neprevyšujúcej 25 °C tak, aby nebol vystavený priamemu teplu ani priamemu svetlu.
Pero obsahujúce náplň sa nesmie uchovávať v chladničke.
Po každej injekcii sa musí na pero opäť nasadiť uzáver na ochranu pred svetlom.
6.4 Špeciálne upozornenia na uchovávanieNeotvorené náplneUchovávajte v chladničke (2 °C–8 °C). Neuchovávajte v mrazničke.
Nedávajte Lantus blízko mraziacej časti ani zmrazeného balenia. Uchovávajte náplň vo vonkajšom obale na ochranu pred svetlom.
Používané náplneUpozornenia na uchovávanie, pozri časť 6.3.
6.5 Druh obalu a obsah balenia3 ml roztoku v náplni (bezfarebné sklo typu I) s čiernym piestom (bromobutylová guma) a tesniacim krytom (hliník) so zátkou (guma z bromobutylu alebo polyizoprénového laminátu a bromobutylu). Dostupné sú balenia 1, 3, 4, 5, 6, 8, 9 a 10 náplní. Nie všetky veľkosti balenia musia byť uvedené na trh.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekomLantus sa nesmie miešať so žiadnym iným inzulínom a nesmie sa ani riediť. Miešanie alebo riedenie môže zmeniť jeho čas/profil účinku a miešanie môže spôsobiť precipitáciu.
Inzulínové pero
Náplne sa majú používať spolu s inzulínovým perom ako je OptiPen a ďalšie perá, ktoré sú vhodné na používanie náplní Lantus, podľa odporúčaní v informácii poskytovanej výrobcom pomôcky.
Pokyny výrobcu týkajúce sa vkladania náplne, upevnenia ihly a podávania inzulínovej injekcie, ktoré sú uvedené v návode na používanie pera, sa musia dôsledne dodržiavať.
Ak sa inzulínové pero poškodí, alebo dobre nefunguje (pre mechanické závady), musí sa zlikvidovať
a použiť nové inzulínové pero.
Ak je pero nefunkčné (pozri návod na používanie pera), roztok sa môže natiahnuť z náplne do injekčnej striekačky (vhodnej pre inzulín s koncentráciou 100 jednotiek/ml) a podať.
NáplneNáplň sa pred vložením do pera musí uchovávať pri izbovej teplote 1 až 2 hodiny.
Pred použitím skontrolujte náplň. Môže sa použiť len ak je roztok číry, bezfarebný, bez viditeľných tuhých častíc a len ak má konzistenciu podobnú vode. Keďže Lantus je roztok, nevyžaduje pred použitím resuspenzáciu.
Pred injekciou sa musia z náplne odstrániť vzduchové bubliny (pozri návod na používanie pera). Prázdne náplne sa nesmú opätovne napĺňať.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCIISanofi-Aventis Deutschland GmbH, D-65926 Frankfurt am Main, Nemecko.
8. REGISTRAČNÉ ČÍSLA
EU/1/00/134/005-007
EU/1/00/134/013-017
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIEDátum prvej registrácie: 9. jún 2000
Dátum posledného predĺženia: 9. jún 2010
10. DÁTUM REVÍZIE TEXTUPodrobné informácie o tomto lieku sú dostupné na internetovej stránke Európskej liekovej agentúry
http://www.ema.europa.eu/.
1. NÁZOV LIEKU
Lantus 100 jednotiek/ml injekčný roztok v náplni pre OptiClik
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Každý ml obsahuje 100 jednotiek inzulínu glargín (zodpovedá 3,64 mg). Každá náplň obsahuje 3 ml injekčného roztoku, čo zodpovedá 300 jednotkám. Inzulín glargín sa vyrába rekombinantnou DNA technológiou v Escherichia coli. Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčný roztok.
Číry, bezfarebný roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Liečba dospelých, adolescentov a detí vo veku 6 rokov a starších s diabetom mellitus, kde sa vyžaduje liečba inzulínom.
4.2 Dávkovanie a spôsob podávania
Dávkovanie
Lantus obsahuje inzulín glargín, analóg inzulínu a má predĺžené trvanie účinku.
Lantus sa má podávať raz denne, kedykoľvek počas dňa, ale každý deň v tom istom čase.
Dávkovacia schéma Lantusu (dávka a čas podania) sa musí prispôsobiť individuálne. Pacientom s diabetes mellitus 2. typu sa môže podávať Lantus spolu s perorálnymi antidiabetikami. Účinnosť tohto lieku je daná v jednotkách. Tieto jednotky sú špecifické len pre Lantus a nie sú rovnaké ako IU alebo jednotky, ktoré sa používajú na vyjadrenie účinnosti iných inzulínových analógov. Pozri časť 5.1.
Populácia starších pacientov (≥ 65 rokov)
U starších pacientov môže progresívne zhoršovanie renálnej funkcie viesť k stálemu poklesu nárokov na inzulín.
Zhrošená renálna funkcia
U pacientov so zhoršenou renálnou funkciou môžu byť nároky na inzulín znížené z dôvodu zníženého inzulínového metabolizmu.
Zhoršená funkcia pečene
U pacientov so zhoršenou funkciou pečene môžu byť nároky na inzulín znížené z dôvodu zníženej kapacity pre glukoneogenézu a zníženého inzulínového metabolizmu.
Pediatrická populácia
Bezpečnosť a účinnosť Lantusu bola stanovená u dospievajúcich a detí vo veku 6 rokov a starších.
U detí sa účinnosť a bezpečnosť Lantusu preukázala iba pri podávaní večer. Vzhľadom
k obmedzeným skúsenostiam s účinnosťou a bezpečnosťou Lantusu u detí mladších ako 6 rokov sa má Lantus podávať v tejto vekovej skupine pod dôsledným lekárskym dohľadom.
Prechod z iných inzulínov na Lantus
Zmena liečebného režimu zo strednodobo alebo dlhodobo pôsobiaceho inzulínu na režim s Lantusom
si môže vyžiadať zmenu dávky bazálneho inzulínu a úpravu sprievodnej antidiabetickej liečby (dávok a časovania prídavných bežných inzulínov alebo rýchlo pôsobiacich analógov inzulínu alebo dávok perorálnych antidiabetík).
Pacienti, ktorí menia režim bazálneho inzulínu z NPH dvakrát denne na režim Lantus jedenkrát denne, musia v prvých týždňoch liečby znížiť dennú dávku bazálneho inzulínu o 20-30 %, aby sa zmenšilo riziko nočnej alebo skorej rannej hypoglykémie. Toto zníženie dávky počas prvých týždňov sa má aspoň čiastočne kompenzovať zvýšením prandiálneho inzulínu, po uplynutí tohto času sa režim má individuálne upraviť.
Pacienti, ktorí užívajú veľké dávky inzulínu, môžu pocítiť pri Lantuse zlepšenú inzulínovú odpoveď, rovnako ako pri iných analógoch inzulínu. Príčinou sú protilátky proti ľudskému inzulínu.
Pri prechode a v prvých týždňoch po ňom sa odporúča starostlivé sledovanie metabolizmu.
So zlepšením metabolickej kontroly a následným zvýšením citlivosti na inzulín môže byť potrebná ďalšia úprava dávky. Úpravu dávky si môže vyžiadať napríklad aj zmena pacientovej hmotnosti a/alebo životného štýlu, zmena času podania dávky inzulínu alebo iné okolnosti, ktoré zvyšujú náchylnosť na hypoglykémiu alebo na hyperglykémiu (pozri časť 4.4).
Spôsob podávania
Lantus sa podáva subkutánne.
Lantus sa nemá podávať intravenózne. Predĺžený účinok Lantusu závisí od jeho aplikácie do subkutánneho tkaniva. Intravenózne podanie dávky, ktorá sa obvykle podáva subkutánne, by mohlo spôsobiť ťažkú hypoglykémiu.
Po podaní Lantusu do brušnej steny, deltového svalu alebo do stehna nie sú klinicky významné rozdiely v hladinách glukózy alebo inzulínu v sére. Miesta podania injekcie sa musia v rámci danej oblasti meniť po každom podaní.
Lantus sa nesmie miešať so žiadnym iným inzulínom ani riediť. Miešanie alebo riedenie môže zmeniť
jeho časový profil účinku a miešanie môže spôsobiť precipitáciu. Podrobnejšie o zaobchádzaní s liekom, pozri časť 6.6.
4.3 Kontraindikácie
Precitlivenosť na liečivo alebo na ktorúkoľvek z pomocných látok.
4.4 Osobitné upozornenia a opatrenia pri používaní
Lantus nie je inzulín voľby na liečbu diabetickej ketoacidózy. Namiesto toho, sa v takýchto prípadoch odporúča intravenózne podať bežný inzulín.
V prípade nedostatočnej glukózovej kontroly alebo náchylnosti na hyper- alebo hypoglykemické príhody sa musí ešte pred zvážením úpravy dávok prehodnotiť ako pacient dodržiava predpísaný liečebný režim, injekčné miesta, správnu techniku aplikácie injekcií a iné významné faktory.
Prestavenie pacienta na iný typ alebo druh inzulínu sa musí robiť pod prísnym lekárskym dohľadom. Zmena sily, druhu (iný výrobca), typu (bežný, NPH, lente, s dlhotrvajúcim účinkom, atď.), pôvodu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo výrobného postupu môže mať za následok to, že je potrebné zmeniť dávku.
Podávanie inzulínu môže spôsobiť tvorbu protilátok. V zriedkavých prípadoch si môže prítomnosť týchto inzulínových protilátok vyžiadať úpravu dávok inzulínu, aby sa upravil sklon ku hyper- alebo hypoglykémii. (pozri časť 4.8.)
Hypoglykémia
Čas výskytu hypoglykémie závisí od profilu účinku použitých inzulínov a preto sa môže zmeniť pri zmene liečebného režimu. V dôsledku dlhšie pretrvávajúcej suplementácie bazálneho inzulínu pri liečbe Lantusom možno očakávať menej nočnej hypoglykémie, ale viac skorej rannej hypoglykémie.
Vyžaduje sa mimoriadna opatrnosť a intenzívne monitorovanie krvnej glukózy sa odporúča
u pacientov, pre ktorých môžu byť hypoglykemické príhody obzvlášť klinicky významné, ako sú napríklad pacienti so signifikantnou stenózou koronárnych artérií alebo krvných ciev zásobujúcich mozog (riziko srdcových alebo mozgových hypoglykemických komplikácií), ako aj pacienti
s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou (riziko prechodnej amaurózy po hypoglykémii).
Pacienti majú byť upozornení na okolnosti, kedy sa varovné príznaky hypoglykémie zmenšujú. Varovné príznaky hypoglykémie sa môžu meniť, môžu byť menej výrazné alebo u určitých rizikových skupín môžu chýbať. Patria sem pacienti:
- s nápadne zlepšenou glykemickou kontrolou,
- s pozvoľným nástupom hypoglykémie,
- staršieho veku,
- po prechode zo zvieracieho na ľudský inzulín,
- s autonómnou neuropatiou v súčasnosti,
- s dlhodobou anamnézou cukrovky,
- s psychiatrickým ochorením,
- dostávajúci sprievodnú liečbu niektorými inými liekmi (pozri časť 4.5).
Tieto okolnosti môžu spôsobiť ťažkú hypoglykémiu (a možnú stratu vedomia) skôr, ako si pacient hypoglykémiu uvedomí.
Predĺžený účinok subkutánne podaného inzulínu glargín môže oneskoriť zotavenie sa po hypoglykémii.
Ak sa zistia normálne alebo znížené hodnoty glykovaného hemoglobínu, musí sa vziať do úvahy možnosť rekurentných nerozpoznaných (najmä nočných) príhod hypoglykémie.
Nevyhnutným predpokladom pre zníženie rizika hypoglykémie je to, aby pacient dodržiaval režim dávok a diétny režim, správne podávanie inzulínu a znalosť príznakov hypoglykémie.
Faktory, ktoré zvyšujú náchylnosť na hypoglykémiu, si vyžadujú obzvlášť podrobné sledovanie a môžu si vyžiadať aj úpravu dávok. K nim patria:
- zmena injekčného miesta,
- zlepšená vnímavosť na inzulín (napr. odstránením stresových faktorov),
- neobvyklá, zvýšená alebo predĺžená fyzická aktivita,
- interkurentné ochorenie (napr. vracanie, hnačka),
- neprimeraný príjem potravy,
- vynechanie jedla,
- konzumácia alkoholu,
- určité nekompenzované poruchy endokrinného systému (napr. pri hypotyreóze a pri nedostatočnej činnosti adenohypofýzy alebo kôry nadobličiek),
- súbežná liečba niektorými inými liekmi.
Interkurentné ochorenie
Interkurentné ochorenie si vyžaduje intenzívnejšie sledovanie metabolizmu. V mnohých prípadoch sa
indikujú močové testy na ketóny a často sa musí upraviť dávku inzulínu. Nároky na inzulín sú často zvýšené. Pacienti s diabetes mellitus 1. typu musia udržiavať pravidelný prísun aspoň malého
množstva sacharidov, aj keď sú schopní jesť len málo alebo vôbec nie, prípadne vracajú a pod. a nikdy nesmú inzulín úplne vynechať.
4.5 Liekové a iné interakcie
Celý rad látok ovplyvňuje glukózový metabolizmus a môže si vyžiadať úpravu dávky inzulínu glargín.
Medzi látky, ktoré môžu zosilňovať účinok znižujúci hladinu cukru v krvi a zvyšujú náchylnosť na hypoglykémiu, patria: perorálne antidiabetiká, inhibítory enzýmu konvertujúceho angiotenzín (ACE), disopyramid, fibráty, fluoxetín, inhibítory monoaminooxidázy (MAO), pentoxifylín, propoxyfén, salicyláty a sulfónamidové antibiotiká.
Medzi látky, ktoré môžu zoslabovať účinok znižujúci hladinu cukru v krvi, patria: kortikosteroidy, danazol, diazoxid, diuretiká, glukagón, izoniazid, estrogény a progestagény, fenotiazínové deriváty, somatotropín, sympatomimetiká (napr. epinefrín [adrenalín], salbutamol, terbutalín), tyroidné hormóny, atypické antipsychotické lieky (napr. klozapín a olanzapín) a inhibítory proteázy.
Betablokátory, klonidín, soli lítia alebo alkohol môžu buď zosilňovať alebo zoslabovať účinok inzulínu znižujúci hladinu cukru v krvi.
Pentamidín môže spôsobiť hypoglykémiu, po ktorej môže niekedy nasledovať hyperglykémia.
Pod vplyvom sympatolytík, ako sú betablokátory, klonidín, guanetidín a rezerpín, sa naviac môžu oslabiť alebo chýbať príznaky adrenergnej kontraregulácie.
4.6 Fertilita, gravidita a laktácia
Gravidita
Z kontrolovaných klinických štúdii nie sú k dispozícii žiadne klinické údaje o gravidných ženách vystavených účinku inzulínu glargín. Údaje o stredne veľkom počte gravidných žien (závery z počtu
300-1000 gravidít) vystavených účinku inzulínu glargín uvádzaného na trh nepreukázali nežiaduce účinky inzulínu glargín na graviditu a nepreukázali malformácie ani toxicitu inzulínu glargín pre plod/novorodenca.
Údaje o zvieratách nepreukázali reprodukčnú toxicitu.
Použitie Lantusu počas gravidity sa môže zvážiť, ak je to nevyhnutné.
Pre pacientky s predtým existujúcou alebo gestačnou cukrovkou je dôležité udržiavanie dobrej metabolickej kontroly počas gravidity. Nároky na inzulín môžu počas prvého trimestra poklesnúť a
v druhom a treťom trimestri všeobecne stúpajú. Okamžite po pôrode nároky na inzulín rapídne klesnú
(zvýšené riziko hypoglykémie). Nevyhnutné je starostlivé sledovanie glykémie.
Dojčenie
Nie je známe, či sa inzulín glargín vylučuje do materského mlieka. Nepredpokladajú sa žiadne metabolické účinky požitého inzulínu glargín na dojčeného novorodenca/dieťa, keďže inzulín glargín ako peptid sa spracováva na aminokyseliny v ľudskom tráviacom trakte. Dojčiacim matkám možno bude treba upraviť dávky inzulínu a diétu.
Fertilita
Štúdie na zvieratách nepreukázali priame škodlivé účinky na fertilitu.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Následkom hypoglykémie alebo hyperglykémie, alebo napríklad ako dôsledok zhoršenia zraku, sa môže zhoršiť pacientova schopnosť sústrediť sa a reagovať. To môže predstavovať riziko
v situáciách, kedy sú tieto schopnosti zvlášť dôležité (napr. vedenie vozidla alebo obsluha strojov).
Pacientom majú byť odporučené také opatrenia, aby sa počas vedenia vozidla vyhli hypoglykémii. To je obzvlášť dôležité pre tých, ktorí majú oslabené alebo chýbajúce varovné príznaky hypoglykémie, alebo majú časté hypoglykemické príhody. Za týchto okolností sa musí zvážiť, či je vhodné viesť vozidlo alebo obsluhovať stroje.
4.8 Nežiaduce účinkyHypoglykémia je vo všeobecnosti najčastejšou nežiaducou reakciou inzulínovej liečby, ktorá sa môže vyskytnúť, ak je dávka inzulínu privysoká vzhľadom na potrebu inzulínu.
Z klinických štúdií vyplynuli nasledujúce nežiaduce účinky, ktoré sú zoradené podľa tried orgánových systémov a v poradí podľa klesajúceho výskytu (veľmi časté: ≥ 1/10; časté: ≥ 1/100 až < 1/10; menej časté: ≥ 1/1000 až < 1/100; zriedkavé: ≥ 1/10 000 až <1 /1000; veľmi zriedkavé: < 1/10 000).
MedDRA triedy orgánových systémov
| Veľmi časté
| Časté
| Menej časté
| Zriedkavé
| Veľmi zriedkavé
| Poruchy
imunitného systému
|
|
|
| Alergické
reakcie
|
| Poruchy metabolizmu a
výživy
| Hypoglykémia
|
|
|
|
| Poruchy
nervového systému
|
|
|
|
| Dysgeúzia
| Poruchy zraku
|
|
|
| Zhoršené
videnie
Retinopatia
|
| Poruchy kože
a podkožného tkaniva
|
| Lipohypertrofia
| Lipoatrofia
|
|
| Poruchy kostrovej
a svalovej sústavy
a spojivového tkaniva
|
|
|
|
| Myalgia
| Celkové poruchy
a reakcie
v mieste podania
|
| Reakcie v mieste
podania injekcie
|
| Edém
|
|
|
|
V rámci jednotlivých skupín frekvencií sú nežiaduce účinky usporiadané v poradí klesajúcej závažnosti.
Poruchy metabolizmu a výživyŤažké ataky hypoglykémie, najmä ak sú rekurentné, môžu spôsobiť neurologické poškodenie.
Dlhotrvajúce alebo ťažké hypoglykemické príhody môžu ohroziť život.
Znakom a príznakom neuroglykopénie predchádzajú u mnohých pacientov znaky adrenergnej kontraregulácie. Všeobecne čím väčší a rýchlejší je pokles krvnej glukózy, tým výraznejší je fenomén kontraregulácie a jej príznakov.
Poruchy imunitného systému
Bezprostredné alergické reakcie na inzulín sú zriedkavé. Takéto reakcie na inzulín (vrátane inzulínu
glargín) alebo na pomocné látky môžu byť spojené napríklad s generalizovanými kožnými reakciami, angioedémom, bronchospazmom, hypotenziou a šokom a môžu ohroziť život.
Podávanie inzulínu môže spôsobiť tvorbu protilátok. V klinických štúdiách sa pozorovali protilátky vykazujúce skrížené reakcie s ľudským inzulínom a inzulínom glargín rovnako v skupine pacientov liečených NPH inzulínom, ako aj v skupine pacientov liečených inzulínom glargín. V zriedkavých prípadoch si môže prítomnosť týchto inzulínových protilátok vyžiadať úpravu dávok inzulínu, aby sa upravil sklon ku hyper- alebo hypoglykémii.
Poruchy oka
Výrazné zmeny glykemickej kontroly môžu dočasne zhoršiť zrak tým, že sa prechodne zmení
zdurenie a refrakčný index šošovky.
Dlhodobo zlepšená glykemická kontrola zmenšuje riziko progresie diabetickej retinopatie. Avšak zintenzívnenie inzulínovej liečby s náhlym zlepšením glykemickej kontroly môže sprevádzať dočasné zhoršenie diabetickej retinopatie. U pacientov s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou, môžu ťažké hypoglykemické príhody vyústiť do prechodnej amaurózy.
Poruchy kože a podkožného tkaniva
Rovnako ako pri každej inzulínovej liečbe sa môže v mieste injekcie vyskytnúť lipodystrofia, ktorá
vedie k oneskorenej lokálnej absorpcii inzulínu. Priebežné striedanie miesta injekcie v rámci určitej injekčnej oblasti môže pomôcť znížiť alebo zabrániť takýmto reakciám.
Celkové poruchy a reakcie v mieste podania
K reakciám v mieste podania injekcie patrí sčervenanie kože, bolesť, svrbenie, žihľavka, opuch alebo
zápal. Väčšina miernych reakcií na inzulín v mieste injekcie obvykle vymizne za niekoľko dní až týždňov.
Inzulín môže zriedkavo spôsobiť retenciu sodíka a opuch, najmä ak sa pôvodne slabá metabolická kontrola zlepšila intenzifikovanou inzulínovou liečbou.
Pediatrickí pacienti
Vo všeobecnosti bezpečnostný profil u detí a dospievajúcich vo veku ≤ 18 rokov je podobný
bezpečnostnému profilu u dospelých.
Správy o nežiaducich reakciách z postmarketingového sledovania zahŕňali u detí a dospievajúcich vo veku ≤ 18 rokov pomerne častejšie reakcie v mieste vpichu (bolesť v mieste vpichu, reakcie v mieste vpichu) a kožné reakcie (vyrážka, urtikária) ako u dospelých (vek > 18 rokov).
Nie sú dostupné žiadne klinické štúdie s údajmi o bezpečnosti u detí mladších ako 6 rokov.
4.9 Predávkovanie
Príznaky
Predávkovanie inzulínom môže viesť k ťažkej a niekedy dlhotrvajúcej a život ohrozujúcej
hypoglykémii.
Liečba
Mierne hypoglykemické príhody sa obvykle liečia perorálnymi sacharidmi. Môže byť potrebná úprava
dávky lieku, jedálneho lístka alebo telesnej aktivity.
Závažnejšie príhody spojené s kómou, kŕčmi alebo neurologickým poškodením možno liečiť intramuskulárnym alebo subkutánnym podaním glukagónu alebo intravenóznym podaním koncentrovanej glukózy. Keďže hypoglykémia sa po zdanlivom klinickom zotavení môže vrátiť, pacient musí udržiavať príjem sacharidov a je nutné pacienta pozorovať.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Lieky používané na liečbu diabetu. Inzulíny a injekčné analógy, dlhopôsobiace.
ATC kód: A10A E04.
Inzulín glargín je ľudský inzulínový analóg vyvinutý tak, aby mal nízku rozpustnosť v neutrálnom pH. Je úplne rozpustný v injekčnom roztoku Lantusu s kyslým pH (pH 4). Po injekcii do podkožného tkaniva sa kyslý roztok neutralizuje, následkom čoho sa tvoria mikroprecipitáty, z ktorých sa priebežne uvoľňuje v malých množstvách inzulín glargín, čím sa zaisťuje hladký a predvídateľný profil priebehu koncentrácie v závislosti od času bez vrcholov s predĺženým trvaním účinku.
Väzba inzulínu na receptory: Vzhľadom na väzbovú kinetiku receptorov inzulínu sa inzulín glargín veľmi podobá ľudskému inzulínu. Preto možno hovoriť o tom istom spôsobe účinku cez receptory inzulínu ako u ľudského inzulínu.
Primárny účinok inzulínov, vrátane inzulínu glargín, je regulácia glukózového metabolizmu. Inzulín a jeho analógy znižujú hladinu krvnej glukózy stimuláciou periférneho vychytávania glukózy, najmä kostrovým svalstvom a tukom a inhibíciou tvorby glukózy v pečeni. Inzulín inhibuje lipolýzu
v adipocytoch, inhibuje proteolýzu a zvyšuje syntézu proteínov.
V klinických farmakologických štúdiách sa ukázalo, že intravenózny inzulín glargín a ľudský inzulín sú pri rovnakých dávkach rovnocenné. Telesná aktivita a iné premenné môžu ovplyvňovať časový priebeh účinku inzulínu glargín rovnako ako pri všetkých inzulínoch.
V euglykemických uzatvorených štúdiách so zdravými dobrovoľníkmi alebo pacientmi s diabetes
1. typu, bol nástup účinku subkutánneho inzulínu glargín pomalší ako u ľudského NPH inzulínu, jeho profil účinku bol hladký, bez vrcholov a s predĺženým trvaním účinku.
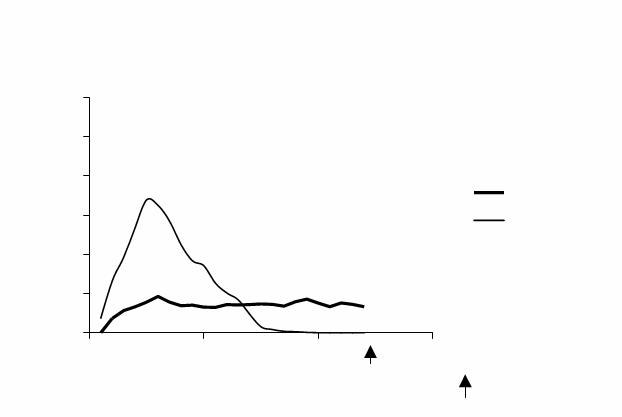
Nasledujúci graf zobrazuje výsledky štúdie u pacientov:
Profil účinku u pacientov s diabetes typu I
6
5
4
inzulín glargín
3 NPH inzulín
2
1
0
0 10 20 30
čas (h) po s.c. injekcii
ukončenie pozorovania





∗ udáva sa ako množstvo infundovanej glukózy na udržanie konštantných plazmatických hladín glukózy (priemerné hodinové hodnoty).
Dlhšie trvanie účinku podkožne podaného inzulínu glargín priamo súvisí s jeho nižšou absorpčnou rýchlosťou a umožňuje podávanie raz denne. Časový priebeh účinku inzulínu a inzulínových analógov, ako je inzulín glargín, sa môže značne líšiť u rôznych jedincov alebo u toho istého jedinca.
Príznaky hypoglykémie alebo hormonálnych odpovedí kontraregulácie boli v klinickej štúdii podobné po intravenóznom podaní inzulínu glargín a ľudského inzulínu u zdravých dobrovoľníkov aj u pacientov s diabetes 1. typu.
Účinky inzulínu glargín (podávaný jedenkrát denne) na diabetickú retinopatiu sa vyhodnocovali v otvorenej 5-ročnej štúdii kontrolovanej NPH (NPH podávaný dvakrát denne) u 1024 pacientov s diabetom 2. typu, u ktorých bola zistená progresia retinopatie o 3 stupne a viac na základe
vyhodnocovania snímky očného pozadia podľa škály Early Treatment Diabetic Retinopathy Study (ETDRS). Pri porovnaní inzulínu glargín s NPH inzulínom sa nepozoroval žiadny významný rozdiel v progresii diabetickej retinopatie.
Pediatrická populáciaV randomizovanej, kontrolovanej klinickej štúdii boli pediatrickí pacienti (vo veku od 6 do 15 rokov)
s diabetom 1. typu (n = 349) liečení po dobu 28 týždňov v inzulínovom režime bazál-bolus, kde bol použitý bežný ľudský inzulín pred každým jedlom. Inzulín glargín sa podával jedenkrát denne pred spaním a NPH ľudský inzulín sa podával jedenkrát alebo dvakrát denne. V obidvoch liečených skupinách sa pozorovali podobné účinky na glykohemoglobín a výskyt symptomatickej hypoglykémie, avšak hladina plazmatickej glukózy nalačno klesla z východiskovej hodnoty viac v skupine s inzulínom glargin ako v skupine s NPH. V skupine s inzulínom glargín bola taktiež menej častý výskyt ťažkej hypoglykémie. 143 pacientov liečených inzulínom glargín v tejto štúdii pokračovalo v liečbe inzulínom glargín v nekontrolovanom predĺžení štúdie pričom sledovanie trvalo priemerne 2 roky. Počas tejto predĺženej liečby inzulínom glargín sa nezaznamenali žiadne nové signály týkajúce sa bezpečnosti.
Taktiež sa uskutočnila „crossover“ štúdia (so skríženým dizajnom) porovnávajúca liečbu inzulínom glargín plus inzulín lispro s liečbou inzulínom NPH plus bežný ľudský inzulín (každá liečba sa podávala 16 týždňov v náhodnom poradí) u 26 dospievajúcich vo veku 12 až 18 rokov s diabetom
1. typu. Rovnako ako vo vyššie uvedenej pediatrickej štúdii pokles hladiny plazmatickej glukózy nalačno z východiskovej hodnoty bol väčší v skupine s inzulínom glargín ako v skupine s NPH. Zmeny HbA1c z východiskovej hodnoty boli v obidvoch liečených skupinách podobné; hodnoty hladiny glukózy v krvi zaznamenané počas noci boli významne vyššie v skupine inzulín glargín / lispro ako v skupine NPH/bežný ľudský inzulín, s priemernou najnižšou hodnotou (nadir) 5,4 mmol/l oproti 4,1 mmol/l. Tomu zodpovedal výskyt nočnej hypoglykémie, ktorý bol 32 % v skupine inzulín glargín / lispro oproti 52 % v skupine NPH / bežný ľudský inzulín.
5.2 Farmakokinetické vlastnosti
U zdravých jedincov a diabetikov ukázali sérové koncentrácie inzulínu pomalšiu a dlhšiu absorpciu a po subkutánnej injekcii inzulínu glargín v porovnaní s ľudským NPH inzulínom chýba vrchol. Koncentrácie teda zodpovedali časovému profilu farmakodynamického účinku inzulínu glargín. Vyššie uvedený graf ukazuje profily farmakodynamického účinku inzulínu glargín a NPH inzulínu.
Inzulín glargín podaný raz denne dosiahne hladiny rovnovážneho stavu za 2-4 dni po prvej dávke. Pri intravenóznom podaní je polčas eliminácie inzulínu glargín a ľudského inzulínu porovnateľný.
U ľudí sa inzulín glargín čiastočne degraduje v podkožnom tkanive v uhlíkovom zakončení beta reťazca a tvoria sa účinné metabolity 21A-gly-inzulín a 21A-gly-des-30B-Thr-inzulín.
V plazme je taktiež prítomný nezmenený inzulín glargín a produkty degradácie.
V klinických štúdiách sa v jednotlivých podskupinách rozdelených podľa veku a rodu nezistili žiadne rozdiely v bezpečnosti a účinnosti pri liečbe inzulínom glargín v porovnaní s celkovou študovanou populáciou.
Paediatrická populácia
Špecifická farmakokinetická štúdia na deťoch alebo dospievajúcich sa nerobila.
5.3 Predklinické údaje o bezpečnosti
Predklinické údaje získané na základe obvyklých farmakologických štúdií bezpečnosti, toxicity po opakovanom podaní, genotoxicity, karcinogénneho potenciálu a reprodukčnej toxicity neodhalili žiadne osobitné riziko pre ľudí.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
chlorid zinočnatý, metakrezol, glycerol,
kyselina chlorovodíková, hydroxid sodný,
voda na injekciu.
6.2 Inkompatibility
Tento liek sa nesmie miešať so žiadnymi inými liekmi. Je dôležité zabezpečiť, aby injekčné striekačky neobsahovali stopy žiadnych iných látok.
6.3 Čas použiteľnosti
3 roky.
Čas použiteľnosti po prvom použití náplne
Liek sa môže uchovávať maximálne 4 týždne pri teplote neprevyšujúcej 25 °C tak, aby nebol vystavený priamemu teplu ani priamemu svetlu. Pero obsahujúce náplň sa nesmie uchovávať v chladničke.
Po každej injekcii sa musí na pero opäť nasadiť uzáver na ochranu pred svetlom.
6.4 Špeciálne upozornenia na uchovávanie
Neotvorené náplne:
Uchovávajte v chladničke (2 °C–8 °C). Neuchovávajte v mrazničke.
Nedávajte Lantus blízko mraziacej časti ani zmrazeného balenia. Uchovávajte náplň vo vonkajšom obale na ochranu pred svetlom.
Používané náplne
Upozornenia na uchovávanie, pozri časť 6.3.
6.5 Druh obalu a obsah balenia
3 ml roztoku v náplni (bezfarebné sklo typu I) s čiernym piestom (bromobutylová guma) a tesniacim krytom (hliník) so zátkou (guma z bromobutylu alebo polyizoprénového laminátu a bromobutylu). Sklenená náplň je nezvratne integrovaná v priehľadnom puzdre a na jednom konci primontovaná
k plastovému mechanizmu závitovým jadrom.
Dostupné sú balenia 1, 3, 4, 5, 6, 8, 9 a 10 náplní pre OptiClik. Nie všetky veľkosti balenia musia byť
uvedené na trh.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Lantus sa nesmie miešať so žiadnym iným inzulínom a nesmie sa ani riediť. Miešanie alebo riedenie môže zmeniť jeho čas/profil účinku a miešanie môže spôsobiť precipitáciu.
Náplne pre OptiClik sa majú používať len spolu s OptiClikom a podľa odporúčaní v informácii poskytovanej výrobcom pomôcky.
Pokyny výrobcu týkajúce sa vkladania náplne, upevnenia ihly a podávania inzulínovej injekcie, ktoré sú uvedené v návode na používanie pera, sa musia dôsledne dodržiavať.
Ak sa OptiClik poškodí, alebo dobre nefunguje (pre mechanické závady), musí sa zlikvidovať
a použiť nový OptiClik.
Náplň sa pred vložením do pera musí uchovávať pri izbovej teplote 1 až 2 hodiny.
Pred použitím skontrolujte náplň. Môže sa použiť len ak je náplň nedotknutá a roztok číry, bezfarebný, bez viditeľných tuhých častíc a len ak má konzistenciu podobnú vode. Keďže Lantus je roztok, nevyžaduje pred použitím resuspenzáciu.
Pred injekciou sa musia z náplne odstrániť vzduchové bubliny (pozri návod na používanie pera). Prázdne náplne sa nesmú opätovne napĺňať.
Ak je pero nefunkčné, možno injekčný roztok natiahnuť z náplne do injekčnej striekačky (vhodnej na inzulín s koncentráciou 100 jednotiek/ml) a aplikovať ho.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Sanofi-Aventis Deutschland GmbH, D-65926 Frankfurt am Main, Nemecko.
8. REGISTRAČNÉ ČÍSLA
EU/1/00/134/022-029
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIEDátum prvej registrácie: 9. jún 2000
Dátum posledného predĺženia: 9. jún 2010
10. DÁTUM REVÍZIE TEXTUPodrobné informácie o tomto lieku sú dostupné na internetovej stránke Európskej liekovej agentúry
http://www.ema.europa.eu/.
1. NÁZOV LIEKU
Lantus OptiSet 100 jednotiek/ml, injekčný roztok v naplnenom pere
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Každý ml obsahuje 100 jednotiek inzulínu glargín (zodpovedá 3,64 mg). Každé pero obsahuje 3 ml injekčného roztoku, čo zodpovedá 300 jednotkám. Inzulín glargín sa vyrába rekombinantnou DNA technológiou v Escherichia coli. Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčný roztok.
Číry, bezfarebný roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Liečba dospelých, adolescentov a detí vo veku 6 rokov a starších s diabetom mellitus, kde sa vyžaduje liečba inzulínom.
4.2 Dávkovanie a spôsob podávania
Dávkovanie
Lantus obsahuje inzulín glargín, analóg inzulínu a má predĺžené trvanie účinku.
Lantus sa má podávať raz denne, kedykoľvek počas dňa, ale každý deň v tom istom čase.
Inzulín sa pomocou OptiSetu podáva v stúpajúcej dávke po 2 jednotkách až do maximálnej jednotlivej dávky 40 jednotiek.
Dávkovacia schéma Lantusu (dávka a čas podania) sa musí prispôsobiť individuálne. Pacientom s diabetes mellitus 2. typu sa môže podávať Lantus spolu s perorálnymi antidiabetikami. Účinnosť tohto lieku je daná v jednotkách. Tieto jednotky sú špecifické len pre Lantus a nie sú rovnaké ako IU alebo jednotky, ktoré sa používajú na vyjadrenie účinnosti iných inzulínových analógov. Pozri časť 5.1.
Populácia starších pacientov (≥ 65 rokov)
U starších pacientov môže progresívne zhoršovanie renálnej funkcie viesť k stálemu poklesu nárokov na inzulín.
Zhrošená renálna funkcia
U pacientov so zhoršenou renálnou funkciou môžu byť nároky na inzulín znížené z dôvodu zníženého inzulínového metabolizmu.
Zhoršená funkcia pečene
U pacientov so zhoršenou funkciou pečene môžu byť nároky na inzulín znížené z dôvodu zníženej kapacity pre glukoneogenézu a zníženého inzulínového metabolizmu.
Pediatrická populácia
Bezpečnosť a účinnosť Lantusu bola stanovená u dospievajúcich a detí vo veku 6 rokov a starších. U detí sa účinnosť a bezpečnosť Lantusu preukázala iba pri podávaní večer. Vzhľadom
k obmedzeným skúsenostiam s účinnosťou a bezpečnosťou Lantusu u detí mladších ako 6 rokov sa
má Lantus podávať v tejto vekovej skupine pod dôsledným lekárskym dohľadom.
Prechod z iných inzulínov na Lantus
Zmena liečebného režimu zo strednodobo alebo dlhodobo pôsobiaceho inzulínu na režim s Lantusom
si môže vyžiadať zmenu dávky bazálneho inzulínu a úpravu sprievodnej antidiabetickej liečby (dávok a časovania prídavných bežných inzulínov alebo rýchlo pôsobiacich analógov inzulínu alebo dávok perorálnych antidiabetík).
Pacienti, ktorí menia režim bazálneho inzulínu z NPH dvakrát denne na režim Lantus jedenkrát denne, musia v prvých týždňoch liečby znížiť dennú dávku bazálneho inzulínu o 20-30 %, aby sa zmenšilo riziko nočnej alebo skorej rannej hypoglykémie.
Toto zníženie dávky počas prvých týždňov sa má aspoň čiastočne kompenzovať zvýšením prandiálneho inzulínu, po uplynutí tohto času sa režim má individuálne upraviť.
Pacienti, ktorí užívajú veľké dávky inzulínu, môžu pocítiť pri Lantuse zlepšenú inzulínovú odpoveď, rovnako ako pri iných analógoch inzulínu. Príčinou sú protilátky proti ľudskému inzulínu.
Pri prechode a v prvých týždňoch po ňom sa odporúča starostlivé sledovanie metabolizmu.
So zlepšením metabolickej kontroly a následným zvýšením citlivosti na inzulín môže byť potrebná ďalšia úprava dávky. Úpravu dávky si môže vyžiadať napríklad aj zmena pacientovej hmotnosti a/alebo životného štýlu, zmena času podania dávky inzulínu alebo iné okolnosti, ktoré zvyšujú náchylnosť na hypoglykémiu alebo na hyperglykémiu (pozri časť 4.4).
Spôsob podávania
Lantus sa podáva subkutánne.
Lantus sa nemá podávať intravenózne. Predĺžený účinok Lantusu závisí od jeho aplikácie do subkutánneho tkaniva. Intravenózne podanie dávky, ktorá sa obvykle podáva subkutánne, by mohlo spôsobiť ťažkú hypoglykémiu.
Po podaní Lantusu do brušnej steny, deltového svalu alebo do stehna nie sú klinicky významné rozdiely v hladinách glukózy alebo inzulínu v sére. Miesta podania injekcie sa musia v rámci danej oblasti meniť po každom podaní.
Lantus sa nesmie miešať so žiadnym iným inzulínom ani riediť. Miešanie alebo riedenie môže zmeniť
jeho časový profil účinku a miešanie môže spôsobiť precipitáciu.
Pred použitím OptiSetu sa musí pozorne prečítať návod na používanie, ktorý je súčasťou písomnej informácie pre používateľov (pozri časť 6.6).
4.3 Kontraindikácie
Precitlivenosť na liečivo alebo na ktorúkoľvek z pomocných látok.
4.4 Osobitné upozornenia a opatrenia pri používaní
Lantus nie je inzulín voľby na liečbu diabetickej ketoacidózy. Namiesto toho, sa v takýchto prípadoch odporúča intravenózne podať bežný inzulín.
V prípade nedostatočnej glukózovej kontroly alebo náchylnosti na hyper- alebo hypoglykemické príhody sa musí ešte pred zvážením úpravy dávok prehodnotiť ako pacient dodržiava predpísaný liečebný režim, injekčné miesta, správnu techniku aplikácie injekcií a iné významné faktory.
Prestavenie pacienta na iný typ alebo druh inzulínu sa musí robiť pod prísnym lekárskym dohľadom. Zmena sily, druhu (iný výrobca), typu (bežný, NPH, lente, s dlhotrvajúcim účinkom, atď.), pôvodu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo výrobného postupu môže mať za následok to, že je potrebné zmeniť dávku.
Podávanie inzulínu môže spôsobiť tvorbu protilátok. V zriedkavých prípadoch si môže prítomnosť týchto inzulínových protilátok vyžiadať úpravu dávok inzulínu, aby sa upravil sklon ku hyper- alebo hypoglykémii. (pozri časť 4.8.)
Hypoglykémia
Čas výskytu hypoglykémie závisí od profilu účinku použitých inzulínov a preto sa môže zmeniť pri
zmene liečebného režimu. V dôsledku dlhšie pretrvávajúcej suplementácie bazálneho inzulínu pri liečbe Lantusom možno očakávať menej nočnej hypoglykémie, ale viac skorej rannej hypoglykémie.
Vyžaduje sa mimoriadna opatrnosť a intenzívne monitorovanie krvnej glukózy sa odporúča u pacientov, pre ktorých môžu byť hypoglykemické príhody obzvlášť klinicky významné, ako sú napríklad pacienti so signifikantnou stenózou koronárnych artérií alebo krvných ciev zásobujúcich mozog (riziko srdcových alebo mozgových hypoglykemických komplikácií), ako aj pacienti
s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou (riziko prechodnej amaurózy po hypoglykémii).
Pacienti majú byť upozornení na okolnosti, kedy sa varovné príznaky hypoglykémie zmenšujú. Varovné príznaky hypoglykémie sa môžu meniť, môžu byť menej výrazné alebo u určitých rizikových skupín môžu chýbať. Patria sem pacienti:
- s nápadne zlepšenou glykemickou kontrolou,
- s pozvoľným nástupom hypoglykémie,
- staršieho veku,
- po prechode zo zvieracieho na ľudský inzulín,
- s autonómnou neuropatiou v súčasnosti,
- s dlhodobou anamnézou cukrovky,
- s psychiatrickým ochorením,
- dostávajúci sprievodnú liečbu niektorými inými liekmi (pozri časť 4.5).
Tieto okolnosti môžu spôsobiť ťažkú hypoglykémiu (a možnú stratu vedomia) skôr, ako si pacient hypoglykémiu uvedomí.
Predĺžený účinok subkutánne podaného inzulínu glargín môže oneskoriť zotavenie sa po hypoglykémii.
Ak sa zistia normálne alebo znížené hodnoty glykovaného hemoglobínu, musí sa vziať do úvahy možnosť rekurentných nerozpoznaných (najmä nočných) príhod hypoglykémie.
Nevyhnutným predpokladom pre zníženie rizika hypoglykémie je to, aby pacient dodržiaval režim dávok a diétny režim, správne podávanie inzulínu a znalosť príznakov hypoglykémie.
Faktory, ktoré zvyšujú náchylnosť na hypoglykémiu, si vyžadujú obzvlášť podrobné sledovanie a môžu si vyžiadať aj úpravu dávok. K nim patria:
- zmena injekčného miesta,
- zlepšená vnímavosť na inzulín (napr. odstránením stresových faktorov),
- neobvyklá, zvýšená alebo predĺžená fyzická aktivita,
- interkurentné ochorenie (napr. vracanie, hnačka),
- neprimeraný príjem potravy,
- vynechanie jedla,
- konzumácia alkoholu,
- určité nekompenzované poruchy endokrinného systému (napr. pri hypotyreóze a pri nedostatočnej činnosti adenohypofýzy alebo kôry nadobličiek),
- súbežná liečba niektorými inými liekmi.
Interkurentné ochorenie
Interkurentné ochorenie si vyžaduje intenzívnejšie sledovanie metabolizmu. V mnohých prípadoch sa
indikujú močové testy na ketóny a často sa musí upraviť dávka inzulínu. Nároky na inzulín sú často zvýšené. Pacienti s diabetes mellitus 1. typu musia udržiavať pravidelný prísun aspoň malého
množstva sacharidov, aj keď sú schopní jesť len málo alebo vôbec nie, prípadne vracajú a pod. a nikdy nesmú inzulín úplne vynechať.
Zaobchádzanie s perom
Pred použitím OptiSetu sa musí pozorne prečítať návod na používanie, ktorý je súčasťou písomnej
informácie pre používateľov, OptiSet sa musí používať podľa odporúčaní v tomto návode na používanie (pozri časť 6.6).
4.5 Liekové a iné interakcie
Celý rad látok ovplyvňuje glukózový metabolizmus a môže si vyžiadať úpravu dávky inzulínu glargín.
Medzi látky, ktoré môžu zosilňovať účinok znižujúci hladinu cukru v krvi a zvyšujú náchylnosť na hypoglykémiu, patria: perorálne antidiabetiká, inhibítory enzýmu konvertujúceho angiotenzín (ACE), disopyramid, fibráty, fluoxetín, inhibítory monoaminooxidázy (MAO), pentoxifylín, propoxyfén, salicyláty a sulfónamidové antibiotiká.
Medzi látky, ktoré môžu zoslabovať účinok znižujúci hladinu cukru v krvi, patria: kortikosteroidy, danazol, diazoxid, diuretiká, glukagón, izoniazid, estrogény a progestagény, fenotiazínové deriváty, somatotropín, sympatomimetiká (napr. epinefrín [adrenalín], salbutamol, terbutalín), tyroidné hormóny, atypické antipsychotické lieky (napr. klozapín a olanzapín) a inhibítory proteázy.
Betablokátory, klonidín, soli lítia alebo alkohol môžu buď zosilňovať alebo zoslabovať účinok inzulínu znižujúci hladinu cukru v krvi. Pentamidín môže spôsobiť hypoglykémiu, po ktorej môže niekedy nasledovať hyperglykémia.
Pod vplyvom sympatolytík, ako sú betablokátory, klonidín, guanetidín a rezerpín, sa naviac môžu oslabiť alebo chýbať príznaky adrenergnej kontraregulácie.
4.6 Fertilita, gravidita a laktácia
Gravidita
Z kontrolovaných klinických štúdii nie sú k dispozícii žiadne klinické údaje o gravidných ženách vystavených účinku inzulínu glargín. Údaje o stredne veľkom počte gravidných žien (závery z počtu
300-1000 gravidít) vystavených účinku inzulínu glargín uvádzaného na trh nepreukázali nežiaduce účinky inzulínu glargín na graviditu a nepreukázali malformácie ani toxicitu inzulínu glargín pre plod/novorodenca.
Údaje o zvieratách nepreukázali reprodukčnú toxicitu.
Použitie Lantusu počas gravidity sa môže zvážiť, ak je to nevyhnutné.
Pre pacientky s predtým existujúcou alebo gestačnou cukrovkou je dôležité udržiavanie dobrej metabolickej kontroly počas gravidity. Nároky na inzulín môžu počas prvého trimestra poklesnúť a
v druhom a treťom trimestri všeobecne stúpajú. Okamžite po pôrode nároky na inzulín rapídne klesnú
(zvýšené riziko hypoglykémie). Nevyhnutné je starostlivé sledovanie glykémie.
Dojčenie
Nie je známe, či sa inzulín glargín vylučuje do materského mlieka. Nepredpokladajú sa žiadne metabolické účinky požitého inzulínu glargín na dojčeného novorodenca/dieťa, keďže inzulín glargín ako peptid sa spracováva na aminokyseliny v ľudskom tráviacom trakte. Dojčiacim matkám možno bude treba upraviť dávky inzulínu a diétu.
FertilitaŠtúdie na zvieratách nepreukázali priame škodlivé účinky na fertilitu.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať strojeNásledkom hypoglykémie alebo hyperglykémie, alebo napríklad ako dôsledok zhoršenia zraku, sa môže zhoršiť pacientova schopnosť sústrediť sa a reagovať. To môže predstavovať riziko
v situáciách, kedy sú tieto schopnosti zvlášť dôležité (napr. vedenie vozidla alebo obsluha strojov).
Pacientom majú byť odporučené také opatrenia, aby sa počas vedenia vozidla vyhli hypoglykémii. To je obzvlášť dôležité pre tých, ktorí majú oslabené alebo chýbajúce varovné príznaky hypoglykémie, alebo majú časté hypoglykemické príhody. Za týchto okolností sa musí zvážiť, či je vhodné viesť vozidlo alebo obsluhovať stroje.
4.8 Nežiaduce účinkyHypoglykémia je vo všeobecnosti najčastejšou nežiaducou reakciou inzulínovej liečby, ktorá sa môže vyskytnúť, ak je dávka inzulínu privysoká vzhľadom na potrebu inzulínu.
Z klinických štúdií vyplynuli nasledujúce nežiaduce účinky, ktoré sú zoradené podľa tried orgánových systémov a v poradí podľa klesajúceho výskytu (veľmi časté: ≥ 1/10; časté: ≥ 1/100 až < 1/10; menej časté: ≥ 1/1000 až < 1/100; zriedkavé: ≥ 1/10 000 až < 1/1000; veľmi zriedkavé: < 1/10 000).
V rámci jednotlivých skupín frekvencií sú nežiaduce účinky usporiadané v poradí klesajúcej závažnosti.
MedDRA
triedy orgánových systémov
| Veľmi časté
| Časté
| Menej časté
| Zriedkavé
| Veľmi zriedkavé
|
Poruchy
imunitného systému
|
|
|
| Alergické
reakcie
|
|
Poruchy
metabolizmu a výživy
| Hypoglykémia
|
|
|
|
|
Poruchy
nervového systému
|
|
|
|
| Dysgeúzia
|
Poruchy zraku
|
|
|
| Zhoršené videnie
Retinopatia
|
|
Poruchy kože
a podkožného tkaniva
|
| Lipohypertrofia
| Lipoatrofia
|
|
|
Poruchy
kostrovej
a svalovej sústavy
a spojivového tkaniva
|
|
|
|
| Myalgia
|
Celkové poruchy
a reakcie
v mieste podania
|
|
Reakcie v mieste
podania injekcie
|
|
Edém
|
|
Poruchy metabolizmu a výživy
Ťažké ataky hypoglykémie, najmä ak sú rekurentné, môžu spôsobiť neurologické poškodenie.
Dlhotrvajúce alebo ťažké hypoglykemické príhody môžu ohroziť život.
Znakom a príznakom neuroglykopénie predchádzajú u mnohých pacientov znaky adrenergnej kontraregulácie. Všeobecne čím väčší a rýchlejší je pokles krvnej glukózy, tým výraznejší je fenomén kontraregulácie a jej príznakov.
Poruchy imunitného systémuBezprostredné alergické reakcie na inzulín sú zriedkavé. Takéto reakcie na inzulín (vrátane inzulínu
glargín) alebo na pomocné látky môžu byť spojené napríklad s generalizovanými kožnými reakciami, angioedémom, bronchospazmom, hypotenziou a šokom a môžu ohroziť život.
Podávanie inzulínu môže spôsobiť tvorbu protilátok. V klinických štúdiách sa pozorovali protilátky vykazujúce skrížené reakcie s ľudským inzulínom a inzulínom glargín rovnako v skupine pacientov liečených NPH inzulínom, ako aj v skupine pacientov liečených inzulínom glargín. V zriedkavých prípadoch si môže prítomnosť týchto inzulínových protilátok vyžiadať úpravu dávok inzulínu, aby sa upravil sklon ku hyper- alebo hypoglykémii.
Poruchy okaZriedkavé: Zhoršenie zrakuVýrazné zmeny glykemickej kontroly môžu dočasne zhoršiť zrak tým, že sa prechodne zmení zdurenie a refrakčný index šošovky.
Dlhodobo zlepšená glykemická kontrola zmenšuje riziko progresie diabetickej retinopatie. Avšak zintenzívnenie inzulínovej liečby s náhlym zlepšením glykemickej kontroly môže sprevádzať dočasné zhoršenie diabetickej retinopatie. U pacientov s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou, môžu ťažké hypoglykemické príhody vyústiť do prechodnej amaurózy.
Poruchy kože a podkožného tkanivaRovnako ako pri každej inzulínovej liečbe sa môže v mieste injekcie vyskytnúť lipodystrofia, ktorá
vedie k oneskorenej lokálnej absorpcii inzulínu. Priebežné striedanie miesta injekcie v rámci určitej injekčnej oblasti môže pomôcť znížiť alebo zabrániť takýmto reakciám.
Celkové poruchy a reakcie v mieste podaniaK reakciám v mieste podania injekcie patrí sčervenanie kože, bolesť, svrbenie, žihľavka, opuch alebo
zápal. Väčšina miernych reakcií na inzulín v mieste injekcie obvykle vymizne za niekoľko dní až týždňov.
Inzulín môže zriedkavo spôsobiť retenciu sodíka a opuch, najmä ak sa pôvodne slabá metabolická kontrola zlepšila intenzifikovanou inzulínovou liečbou.
Pediatrickí pacientiVo všeobecnosti bezpečnostný profil u detí a dospievajúcich vo veku ≤ 18 rokov je podobný
bezpečnostnému profilu u dospelých.
Správy o nežiaducich reakciách z postmarketingového sledovania zahŕňali u detí a dospievajúcich vo veku ≤ 18 rokov pomerne častejšie reakcie v mieste vpichu (bolesť v mieste vpichu, reakcie v mieste vpichu) a kožné reakcie (vyrážka, urtikária) ako u dospelých (vek > 18 rokov).
Nie sú dostupné žiadne klinické štúdie s údajmi o bezpečnosti u detí mladších ako 6 rokov.
4.9 Predávkovanie
Príznaky
Predávkovanie inzulínom môže viesť k ťažkej a niekedy dlhotrvajúcej a život ohrozujúcej
hypoglykémii.
Liečba
Mierne hypoglykemické príhody sa obvykle liečia perorálnymi sacharidmi. Môže byť potrebná úprava
dávky lieku, jedálneho lístka alebo telesnej aktivity.
Závažnejšie príhody spojené s kómou, kŕčmi alebo neurologickým poškodením možno liečiť intramuskulárnym alebo subkutánnym podaním glukagónu alebo intravenóznym podaním koncentrovanej glukózy. Keďže hypoglykémia sa po zdanlivom klinickom zotavení môže vrátiť, pacient musí udržiavať príjem sacharidov a je nutné pacienta pozorovať.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Lieky používané na liečbu diabetu. Inzulíny a injekčné analógy, dlhopôsobiace.
ATC kód: A10A E04.
Inzulín glargín je ľudský inzulínový analóg vyvinutý tak, aby mal nízku rozpustnosť v neutrálnom pH. Je úplne rozpustný v injekčnom roztoku Lantusu s kyslým pH (pH 4). Po injekcii do podkožného tkaniva sa kyslý roztok neutralizuje, následkom čoho sa tvoria mikroprecipitáty, z ktorých sa priebežne uvoľňuje v malých množstvách inzulín glargín, čim sa zaisťuje hladký a predvídateľný profil priebehu koncentrácie v závislosti od času bez vrcholov s predĺženým trvaním účinku.
Väzba inzulínu na receptory: Vzhľadom na väzbovú kinetiku receptorov inzulínu sa inzulín glargín veľmi podobá ľudskému inzulínu. Preto možno hovoriť o tom istom spôsobe účinku cez receptory inzulínu ako u ľudského inzulínu.
Primárny účinok inzulínov, vrátane inzulínu glargín, je regulácia glukózového metabolizmu. Inzulín a jeho analógy znižujú hladinu krvnej glukózy stimuláciou periférneho vychytávania glukózy, najmä kostrovým svalstvom a tukom a inhibíciou tvorby glukózy v pečeni. Inzulín inhibuje lipolýzu
v adipocytoch, inhibuje proteolýzu a zvyšuje syntézu proteínov.
V klinických farmakologických štúdiách sa ukázalo, že intravenózny inzulín glargín a ľudský inzulín sú pri rovnakých dávkach rovnocenné. Telesná aktivita a iné premenné môžu ovplyvňovať časový priebeh účinku inzulínu glargín rovnako ako pri všetkých inzulínoch.
V euglykemických uzatvorených štúdiách so zdravými dobrovoľníkmi alebo pacientmi s diabetes
1. typu, bol nástup účinku subkutánneho inzulínu glargín pomalší ako u ľudského NPH inzulínu, jeho profil účinku bol hladký, bez vrcholov a s predĺženým trvaním účinku.
Nasledujúci graf zobrazuje výsledky štúdie u pacientov:
Profil účinku u pacientov s diabetes typu I
6
5
4
inzulín glargín

3 NPH inzulín
2
1
0
0 10 20 30
čas (h) po s.c. injekcii
ukončenie pozorovania





∗ udáva sa ako množstvo infundovanej glukózy na udržanie konštantných plazmatických hladín glukózy (priemerné hodinové hodnoty).
Dlhšie trvanie účinku podkožne podaného inzulínu glargín priamo súvisí s jeho nižšou absorpčnou rýchlosťou a umožňuje podávanie raz denne. Časový priebeh účinku inzulínu a inzulínových analógov, ako je inzulín glargín, sa môže značne líšiť u rôznych jedincov alebo u toho istého jedinca.'
Príznaky hypoglykémie alebo hormonálnych odpovedí kontraregulácie boli v klinickej štúdii podobné po intravenóznom podaní inzulínu glargín a ľudského inzulínu u zdravých dobrovoľníkov aj u pacientov s diabetes 1. typu.
Účinky inzulínu glargín (podávaný jedenkrát denne) na diabetickú retinopatiu sa vyhodnocovali v otvorenej 5-ročnej štúdii kontrolovanej NPH (NPH podávaný dvakrát denne) u 1024 pacientov s diabetom 2. typu, u ktorých bola zistená progresia retinopatie o 3 stupne a viac na základe
vyhodnocovania snímky očného pozadia podľa škály Early Treatment Diabetic Retinopathy Study (ETDRS). Pri porovnaní inzulínu glargín s NPH inzulínom sa nepozoroval žiadny významný rozdiel v progresii diabetickej retinopatie.
Pediatrická populáciaV randomizovanej, kontrolovanej klinickej štúdii boli pediatrickí pacienti (vo veku od 6 do 15 rokov)
s diabetom 1. typu (n = 349) liečení po dobu 28 týždňov v inzulínovom režime bazál-bolus, kde bol použitý bežný ľudský inzulín pred každým jedlom. Inzulín glargín sa podával jedenkrát denne pred spaním a NPH ľudský inzulín sa podával jedenkrát alebo dvakrát denne. V obidvoch liečených skupinách sa pozorovali podobné účinky na glykohemoglobín a výskyt symptomatickej hypoglykémie, avšak hladina plazmatickej glukózy nalačno klesla z východiskovej hodnoty viac v skupine s inzulínom glargin ako v skupine s NPH. V skupine s inzulínom glargín bola taktiež menej častý výskyt ťažkej hypoglykémie. 143 pacientov liečených inzulínom glargín v tejto štúdii pokračovalo v liečbe inzulínom glargín v nekontrolovanom predĺžení štúdie pričom sledovanie trvalo priemerne 2 roky. Počas tejto predĺženej liečby inzulínom glargín sa nezaznamenali žiadne nové signály týkajúce sa bezpečnosti.
Taktiež sa uskutočnila „crossover“ štúdia (so skríženým dizajnom) porovnávajúca liečbu inzulínom glargín plus inzulín lispro s liečbou inzulínom NPH plus bežný ľudský inzulín (každá liečba sa podávala 16 týždňov v náhodnom poradí) u 26 dospievajúcich vo veku 12 až 18 rokov s diabetom
1. typu. Rovnako ako vo vyššie uvedenej pediatrickej štúdii pokles hladiny plazmatickej glukózy nalačno z východiskovej hodnoty bol väčší v skupine s inzulínom glargín ako v skupine s NPH. Zmeny HbA1c z východiskovej hodnoty boli v obidvoch liečených skupinách podobné; hodnoty hladiny glukózy v krvi zaznamenané počas noci boli významne vyššie v skupine inzulín glargín / lispro ako v skupine NPH/bežný ľudský inzulín, s priemernou najnižšou hodnotou (nadir) 5,4 mmol/l oproti 4,1 mmol/l. Tomu zodpovedal výskyt nočnej hypoglykémie, ktorý bol 32 % v skupine inzulín glargín / lispro oproti 52 % v skupine NPH / bežný ľudský inzulín.
5.2 Farmakokinetické vlastnosti
U zdravých jedincov a diabetikov ukázali sérové koncentrácie inzulínu pomalšiu a dlhšiu absorpciu a po subkutánnej injekcii inzulínu glargín v porovnaní s ľudským NPH inzulínom chýba vrchol. Koncentrácie teda zodpovedali časovému profilu farmakodynamického účinku inzulínu glargín. Vyššie uvedený graf ukazuje profily farmakodynamického účinku inzulínu glargín a NPH inzulínu.
Inzulín glargín podaný raz denne dosiahne hladiny rovnovážneho stavu za 2-4 dni po prvej dávke. Pri intravenóznom podaní je polčas eliminácie inzulínu glargín a ľudského inzulínu porovnateľný.
U ľudí sa inzulín glargín čiastočne degraduje v podkožnom tkanive v uhlíkovom zakončení beta reťazca a tvoria sa účinné metabolity 21A-gly-inzulín a 21A-gly-des-30B-Thr-inzulín.
V plazme je taktiež prítomný nezmenený inzulín glargín a produkty degradácie.
V klinických štúdiách sa v jednotlivých podskupinách rozdelených podľa veku a rodu nezistili žiadne rozdiely v bezpečnosti a účinnosti pri liečbe inzulínom glargín v porovnaní s celkovou študovanou populáciou.
Paediatrická populácia
Špecifická farmakokinetická štúdia na deťoch alebo dospievajúcich sa nerobila.
5.3 Predklinické údaje o bezpečnosti
Predklinické údaje získané na základe obvyklých farmakologických štúdií bezpečnosti, toxicity po opakovanom podaní, genotoxicity, karcinogénneho potenciálu a reprodukčnej toxicity neodhalili žiadne osobitné riziko pre ľudí.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
chlorid zinočnatý, metakrezol, glycerol,
kyselina chlorovodíková, hydroxid sodný,
voda na injekciu.
6.2 Inkompatibility
Tento liek sa nesmie miešať so žiadnymi inými liekmi.
6.3 Čas použiteľnosti
3 roky.
Čas použiteľnosti po prvom použití pera
Liek sa môže uchovávať maximálne 4 týždne pri teplote neprevyšujúcej 25 °C tak, aby nebol vystavený priamemu teplu ani priamemu svetlu. Perá, ktoré sa používajú, sa nesmú uchovávať v chladničke.
Po každej injekcii sa musí na pero opäť nasadiť kryt na ochranu pred svetlom
6.4 Špeciálne upozornenia na uchovávanie
Nepoužívané perá
Uchovávajte v chladničke (2 °C–8 °C). Neuchovávajte v mrazničke.
Nedávajte Lantus blízko mraziacej časti ani zmrazeného balenia. Uchovávajte naplnené pero vo vonkajšom obale na ochranu pred svetlom.
Používané perá
Upozornenia na uchovávanie, pozri časť 6.3.
6.5 Druh obalu a obsah balenia
3 ml roztoku v náplni (bezfarebné sklo typu I) s čiernym piestom (bromobutylová guma) a tesniacim krytom (hliník) so zátkou (guma z bromobutylu alebo z polyizoprénového laminátu a bromobutylu). Náplne sú zaplombované do jednorazových perových injektorov. Balenie neobsahuje ihly.
Dostupné sú balenia 1, 3, 4, 5, 6, 8, 9 a 10 pier. Nie všetky veľkosti balenia musia byť uvedené na trh.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Pred prvým použitím sa pero musí skladovať 1 až 2 hodiny pri izbovej teplote.
Pred použitím skontrolujte náplň. Môže sa použiť len ak je roztok číry, bezfarebný a neobsahuje viditeľné tuhé častice a ak má konzistenciu podobnú ako voda. Keďže Lantus je roztok, nevyžaduje sa pred použitím resuspenzácia.
Lantus sa nesmie miešať so žiadnym iným inzulínom a nesmie sa ani riediť. Miešanie alebo riedenie môže zmeniť jeho čas/profil účinku a miešanie môže spôsobiť precipitáciu.
Prázdne perá nesmú byť opätovne použité a musia byť náležite zlikvidované.
Aby sa zabránilo možným prenosným ochoreniam, musí každé pero používať len jeden pacient.
Zaobchádzanie s perom
Pacient musí byť upozornený, aby si pred použitím OptiSetu pozorne prečítal návod na používanie, ktorý je súčasťou písomnej informácie pre používateľov.
Uzáver pera Ihla pera (nie je súčasťou balenia)
Telo pera
Ochranné tesnenie
Inzulínový zásobník
Čierny piest
Názov inzulínu a farebné označenie
Dávkovacia šípka
Vonkajší kryt ihly
Vnútorný
kryt ihly Ihla
Farebná čiara
Gumené
tesnenie
Ukazovateľ
zvyšného inzulínu
Prepínač
dávky
Injekčné tlačidlo
Schematický nákres pera
Dôležité informácie pre používanie OptiSetu:
• Pred každým použitím sa musí upevniť nová ihla. Musia sa používať iba ihly určené pre použitie s OptiSetom.
• Pred každou injekciou sa musí vždy urobiť skúška bezpečnosti.
• V prípade použitia nového OptiSetu sa musí prvá skúška bezpečnosti urobiť s dávkou
8 jednotiek už vopred nastavenou výrobcom.
• Prepínač dávky sa môže otáčať iba jedným smerom.
• Nikdy sa nesmie otáčať prepínačom dávky (zmena dávky) po vytiahnutí injekčného tlačidla.
• Toto pero je určené iba pre jedného pacienta. Nesmie ho zdieľať s nikým iným.
• Ak podáva pacientovi injekciu iná osoba, vyžaduje sa od nej špeciálna opatrnosť, aby sa
predišlo náhodnému poraneniu ihlou a prenosu infekcie.
• Nikdy sa nesmie použiť OptiSet , ak je poškodený, alebo ak si nie je pacient istý, či funguje správne.
• Pre prípad straty alebo poškodenia OptiSetu musí mať vždy pacient k dispozícii náhradný
OptiSet.
Pokyny na uchovávanie
Pozrite si prosím časť 6.4 tohto SPC, kde sú uvedené pokyny ako uchovávať OptiSet.
Ak sa OptiSet uchováva na chladnom mieste, musí sa odtiaľ vziať 1 až 2 hodiny pred podaním injekcie, aby sa oteplil. Injikovanie chladného inzulínu je bolestivejšie.
Použitý OptiSet sa musí zlikvidovať v súlade s lokálnymi požiadavkami.
Údržba
OptiSet je nutné chrániť pred prachom a nečistotami.
Vonkajšiu stranu OptiSetu je možné čistiť vlhkou handričkou.
Pero sa nesmie namáčať, umývať ani mastiť, môže sa tým poškodiť.
OptiSet je navrhnutý tak, aby sa s ním pracovalo presne a bezpečne. Má sa s ním zaobchádzať starostlivo. Pacient sa musí vyhýbať situáciám, kde sa môže OptiSet poškodiť. Ak má pacient obavy, že OptiSet môže byť poškodený, musí použiť nový OptiSet.
Krok 1. Kontrola inzulínu
Po odstránení uzáveru pera sa musí skontrolovať štítok na pere a inzulínovom zásobníku, aby bolo isté, že obsahuje správny inzulín. Taktiež sa musí skontrolovať vzhľad inzulínu: roztok inzulínu musí byť číry, bezfarebný, nesmú byť viditeľné tuhé častice a musí mať konzistenciu podobnú vode. OptiSet sa nesmie použiť, keď roztok inzulínu je zakalený, sfarbený alebo obsahuje častice.
Krok 2. Upevnenie ihly
Ihla sa musí dôkladne nasadiť na pero tak, aby bola s ním v jednej rovine.
Krok 3. Skúška bezpečnosti
Pred každou injekciou sa musí urobiť skúška bezpečnosti.
Pre nový a ešte nepoužitý OptiSet sa musí prvá skúška bezpečnosti urobiť s dávkou 8 jednotiek, ktorá je už nastavená výrobcom.
V prípade už používaného OptiSetu, sa nastaví dávka 2 jednotiek otáčaním prepínača dávky smerom dopredu, až kým dávkovacia šípka nebude ukazovať na číslo 2. Prepínač dávky sa môže otáčať iba jedným smerom.
Na nastavenie dávky sa musí úplne vytiahnuť injekčné tlačidlo. Nikdy sa nesmie otáčať prepínačom dávky po vytiahnutí injekčného tlačidla.
Vonkajší a vnútorný kryt ihly sa musia odstrániť. Vonkajší kryt ihly sa má odložiť na odstránenie použitej ihly.
Pero sa musí držať tak, aby ihla smerovala nahor, a súčasne sa musí jemne poklepávať prstom na inzulínový zásobník, aby sa všetky vzduchové bubliny dostali k ihle.
Potom sa injekčné tlačidlo musí úplne stlačiť.
Ak inzulín vystrekne cez hrot ihly, znamená to, že pero a ihla fungujú správne.
Ak sa na hrote ihly neobjaví žiadny inzulín, krok 3 sa musí opakovať ešte dvakrát, až kým sa inzulín na hrote ihly neobjaví. Ak inzulín ešte stále nevystrekne, ihla sa musí vymeniť, pretože môže byť upchatá a pokus sa musí opakovať. Ak inzulín ani po výmene ihly nevystrekne, OptiSet môže byť poškodený. Tento OptiSet sa už nesmie použiť.
Krok 4. Nastavenie dávky
Dávku možno nastaviť v krokoch po 2 jednotkách, od minimálnej hodnoty 2 jednotky až po maximálnu hodnotu 40 jednotiek. Ak sa vyžaduje dávka vyššia ako 40 jednotiek, musí sa podať v dvoch alebo viacerých injekciách.
Pacient musí skontrolovať, či má dosť inzulínu na potrebnú dávku.
Ukazovateľ zvyšného inzulínu na priehľadnom inzulínovom zásobníku ukazuje približne zostávajúce množstvo inzulínu v OptiSete. Tento ukazovateľ sa nesmie použiť na nastavenie dávky inzulínu.
Ak sa čierny piest nachádza na začiatku farebnej čiary, potom je k dispozícii približne 40 jednotiek inzulínu.
Ak sa čierny piest nachádza na konci farebnej čiary, potom je k dispozícii približne 20 jednotiek inzulínu.
Dávkovačom sa má otáčať smerom dopredu, kým dávkovacia šípka neukazuje na požadovanú dávku.
Krok 5. Natiahnutie dávky
Injekčné tlačidlo sa musí vytiahnuť tak ďaleko ako sa dá, aby sa dávka mohla natiahnuť.
Pacient musí skontrolovať, či zvolená dávka je úplne natiahnutá. Injekčné tlačidlo sa dá vytiahnuť len tak ďaleko, aké je zostávajúce množstvo inzulínu v zásobníku.
Injekčné tlačidlo umožní kontrolu aktuálnej natiahnutej dávky. Injekčné tlačidlo počas tejto kontroly musí zostať vytiahnuté. Posledná hrubá viditeľná čiara na injekčnom tlačidle ukazuje množstvo natiahnutého inzulínu. Keď injekčné tlačidlo je vytiahnuté, vidieť iba vrchnú časť tejto hrubej čiary.
Krok 6. Podanie dávky
Pacient musí byť informovaný o injekčnej technike svojím lekárom. Ihla sa musí vpichnúť do kože.
Injekčné tlačidlo sa musí úplne zatlačiť. Je možné počuť klikanie, ktoré prestane, keď sa injekčné tlačidlo úplne zatlačí. Potom sa musí držať zatlačené 10 sekúnd pred vytiahnutím ihly z kože. Tak sa zabezpečí, že bude podaná celá dávka inzulínu.
Krok 7. Odstránenie a likvidácia ihly
Po každej injekcii sa musí ihla odstrániť a zlikvidovať. Zabraňuje sa tým kontaminácii a/alebo infekcii ako aj prístupu vzduchu do inzulínového zásobníka a unikaniu inzulínu , čo by mohlo spôsobiť nepresné dávkovanie. Ihly sa nesmú používať opakovane.
Na pero sa musí opäť nasadiť uzáver.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCIISanofi-Aventis Deutschland GmbH, D-65926 Frankfurt am Main, Nemecko.
8. REGISTRAČNÉ ČÍSLAEU/1/00/134/008-011
EU/1/00/134/018-021
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIEDátum prvej registrácie: 9. jún 2000
Dátum posledného predĺženia: 9. jún 2010
10. DÁTUM REVÍZIE TEXTUPodrobné informácie o tomto lieku sú dostupné na internetovej stránke Európskej liekovej agentúry
http://www.ema.europa.eu/.
1. NÁZOV LIEKU
Lantus SoloStar 100 jednotiek/ml injekčný roztok v naplnenom pere
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Každý ml obsahuje 100 jednotiek inzulínu glargín (zodpovedá 3,64 mg). Každé pero obsahuje 3 ml injekčného roztoku, čo zodpovedá 300 jednotkám. Inzulín glargín sa vyrába rekombinantnou DNA technológiou v Escherichia coli. Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA
Injekčný roztok.
Číry, bezfarebný roztok.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Liečba dospelých, adolescentov a detí vo veku 6 rokov a starších s diabetom mellitus, kde sa vyžaduje liečba inzulínom.
4.2 Dávkovanie a spôsob podávania
Lantus obsahuje inzulín glargín, analóg inzulínu a má predĺžené trvanie účinku.
Lantus sa má podávať raz denne, kedykoľvek počas dňa, ale každý deň v tom istom čase.
Dávkovacia schéma Lantusu (dávka a čas podania) sa musí prispôsobiť individuálne. Pacientom s diabetes mellitus 2. typu sa môže podávať Lantus spolu s perorálnymi antidiabetikami. Účinnosť tohto lieku je daná v jednotkách. Tieto jednotky sú špecifické len pre Lantus a nie sú rovnaké ako IU alebo jednotky, ktoré sa používajú na vyjadrenie účinnosti iných inzulínových analógov. Pozri časť 5.1.
Populácia starších pacientov (≥ 65 rokov)
U starších pacientov môže progresívne zhoršovanie renálnej funkcie viesť k stálemu poklesu nárokov na inzulín.
Zhrošená renálna funkcia
U pacientov so zhoršenou renálnou funkciou môžu byť nároky na inzulín znížené z dôvodu zníženého inzulínového metabolizmu.
Zhoršená funkcia pečene
U pacientov so zhoršenou funkciou pečene môžu byť nároky na inzulín znížené z dôvodu zníženej kapacity pre glukoneogenézu a zníženého inzulínového metabolizmu.
Pediatrická populácia
Bezpečnosť a účinnosť Lantusu bola stanovená u dospievajúcich a detí vo veku 6 rokov a starších.
U detí sa účinnosť a bezpečnosť Lantusu preukázala iba pri podávaní večer. Vzhľadom
k obmedzeným skúsenostiam s účinnosťou a bezpečnosťou Lantusu u detí mladších ako 6 rokov sa má Lantus podávať v tejto vekovej skupine pod dôsledným lekárskym dohľadom.
Prechod z iných inzulínov na Lantus
Zmena liečebného režimu zo strednodobo alebo dlhodobo pôsobiaceho inzulínu na režim s Lantusom
si môže vyžiadať zmenu dávky bazálneho inzulínu a úpravu sprievodnej antidiabetickej liečby (dávok a časovania prídavných bežných inzulínov alebo rýchlo pôsobiacich analógov inzulínu alebo dávok perorálnych antidiabetík).
Pacienti, ktorí menia režim bazálneho inzulínu z NPH dvakrát denne na režim Lantus jedenkrát denne, musia v prvých týždňoch liečby znížiť dennú dávku bazálneho inzulínu o 20-30 %, aby sa zmenšilo riziko nočnej alebo skorej rannej hypoglykémie.
Toto zníženie dávky počas prvých týždňov sa má aspoň čiastočne kompenzovať zvýšením prandiálneho inzulínu, po uplynutí tohto času sa režim má individuálne upraviť.
Pacienti, ktorí užívajú veľké dávky inzulínu, môžu pocítiť pri Lantuse zlepšenú inzulínovú odpoveď, rovnako ako pri iných analógoch inzulínu. Príčinou sú protilátky proti ľudskému inzulínu.
Pri prechode a v prvých týždňoch po ňom sa odporúča starostlivé sledovanie metabolizmu.
So zlepšením metabolickej kontroly a následným zvýšením citlivosti na inzulín môže byť potrebná ďalšia úprava dávky. Úpravu dávky si môže vyžiadať napríklad aj zmena pacientovej hmotnosti a/alebo životného štýlu, zmena času podania dávky inzulínu alebo iné okolnosti, ktoré zvyšujú náchylnosť na hypoglykémiu alebo na hyperglykémiu (pozri časť 4.4).
Spôsob podávania
Lantus sa podáva subkutánne.
Lantus sa nemá podávať intravenózne. Predĺžené trvanie účinku Lantusu závisí od jeho aplikácie do subkutánneho tkaniva. Intravenózne podanie dávky, ktorá sa obvykle podáva subkutánne, by mohlo spôsobiť ťažkú hypoglykémiu.
Po podaní Lantusu do brušnej steny, deltového svalu alebo do stehna nie sú klinicky významné rozdiely v hladinách glukózy alebo inzulínu v sére. Miesta podania injekcie sa musia v rámci danej oblasti meniť po každom podaní.
Lantus sa nesmie miešať so žiadnym iným inzulínom ani riediť. Miešanie alebo riedenie môže zmeniť
jeho časový profil účinku a miešanie môže spôsobiť precipitáciu.
Pred použitím SoloStaru sa musí pozorne prečítať návod na používanie, ktorý je súčasťou písomnej informácie pre používateľov (pozri časť 6.6).
4.3 Kontraindikácie
Precitlivenosť na liečivo alebo na ktorúkoľvek z pomocných látok.
4.4 Osobitné upozornenia a opatrenia pri používaní
Lantus nie je inzulín voľby na liečbu diabetickej ketoacidózy. Namiesto toho sa v takýchto prípadoch odporúča intravenózne podať bežný inzulín.
V prípade nedostatočnej glukózovej kontroly alebo náchylnosti na hyper- alebo hypoglykemické príhody sa musí ešte pred zvážením úpravy dávok prehodnotiť ako pacient dodržiava predpísaný liečebný režim, injekčné miesta, správnu techniku aplikácie injekcií a iné významné faktory.
Prestavenie pacienta na iný typ alebo druh inzulínu sa musí robiť pod prísnym lekárskym dohľadom. Zmena sily, druhu (iný výrobca), typu (bežný, NPH, lente, s dlhotrvajúcim účinkom, atď.), pôvodu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo výrobného postupu môže mať za následok to, že je potrebné zmeniť dávku.
Podávanie inzulínu môže spôsobiť tvorbu protilátok. V zriedkavých prípadoch si môže prítomnosť týchto inzulínových protilátok vyžiadať úpravu dávok inzulínu, aby sa upravil sklon ku hyper- alebo hypoglykémii. (pozri časť 4.8.)
Hypoglykémia
Čas výskytu hypoglykémie závisí od profilu účinku použitých inzulínov a preto sa môže zmeniť pri
zmene liečebného režimu. V dôsledku dlhšie pretrvávajúcej suplementácie bazálneho inzulínu pri liečbe Lantusom možno očakávať menej nočnej hypoglykémie, ale viac skorej rannej hypoglykémie.
Vyžaduje sa mimoriadna opatrnosť a intenzívne monitorovanie krvnej glukózy sa odporúča u pacientov, pre ktorých môžu byť hypoglykemické príhody obzvlášť klinicky významné, ako sú napríklad pacienti so signifikantnou stenózou koronárnych artérií alebo krvných ciev zásobujúcich mozog (riziko srdcových alebo mozgových hypoglykemických komplikácií), ako aj pacienti
s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou (riziko prechodnej amaurózy po hypoglykémii).
Pacienti majú byť upozornení na okolnosti, kedy sa varovné príznaky hypoglykémie zmenšujú. Varovné príznaky hypoglykémie sa môžu meniť, môžu byť menej výrazné alebo u určitých rizikových skupín môžu chýbať. Patria sem pacienti:
- s nápadne zlepšenou glykemickou kontrolou,
- s pozvoľným nástupom hypoglykémie,
- staršieho veku,
- po prechode zo zvieracieho na ľudský inzulín,
- s autonómnou neuropatiou v súčasnosti,
- s dlhodobou anamnézou cukrovky,
- s psychiatrickým ochorením,
- dostávajúci sprievodnú liečbu niektorými inými liekmi (pozri časť 4.5).
Tieto okolnosti môžu spôsobiť ťažkú hypoglykémiu (a možnú stratu vedomia) skôr, ako si pacient hypoglykémiu uvedomí.
Predĺžený účinok subkutánne podaného inzulínu glargín môže oneskoriť zotavenie sa po hypoglykémii.
Ak sa zistia normálne alebo znížené hodnoty glykovaného hemoglobínu, musí sa vziať do úvahy možnosť rekurentných nerozpoznaných (najmä nočných) príhod hypoglykémie.
Nevyhnutným predpokladom pre zníženie rizika hypoglykémie je to, aby pacient dodržiaval režim dávok a diétny režim, správne podávanie inzulínu a znalosť príznakov hypoglykémie.
Faktory, ktoré zvyšujú náchylnosť na hypoglykémiu, si vyžadujú obzvlášť podrobné sledovanie a môžu si vyžiadať aj úpravu dávky. K nim patria:
- zmena injekčného miesta,
- zlepšená citlivosť na inzulín (napr. odstránením stresových faktorov),
- neobvyklá, zvýšená alebo predĺžená fyzická aktivita,
- interkurentné ochorenie (napr. vracanie, hnačka),
- neprimeraný príjem potravy,
- vynechanie jedla,
- konzumácia alkoholu,
- určité nekompenzované poruchy endokrinného systému (napr. pri hypotyreóze a pri nedostatočnej činnosti adenohypofýzy alebo kôry nadobličiek),
- súbežná liečba niektorými inými liekmi.
Interkurentné ochorenie
Interkurentné ochorenie si vyžaduje intenzívnejšie sledovanie metabolizmu. V mnohých prípadoch sa
indikujú močové testy na ketóny a často sa musí upraviť dávka inzulínu. Nároky na inzulín sú často zvýšené. Pacienti s diabetes mellitus 1. typu musia udržiavať pravidelný prísun aspoň malého
množstva sacharidov, aj keď sú schopní jesť len málo alebo vôbec nie, prípadne vracajú a pod. a nikdy nesmú inzulín úplne vynechať.
Zaobchádzanie s perom
Pred použitím SoloStaru sa musí pozorne prečítať návod na používanie, ktorý je súčasťou písomnej
informácie pre používateľov SoloStar sa musí používať podľa odporúčaní v tomto návode na používanie (pozri časť 6.6).
4.5 Liekové a iné interakcie
Celý rad látok ovplyvňuje glukózový metabolizmus a môže si vyžiadať úpravu dávky inzulínu glargín.
Medzi látky, ktoré môžu zosilňovať účinok znižujúci hladinu cukru v krvi a zvyšujú náchylnosť na hypoglykémiu, patria: perorálne antidiabetiká, inhibítory enzýmu konvertujúceho angiotenzín (ACE), disopyramid, fibráty, fluoxetín, inhibítory monoaminooxidázy (MAO), pentoxifylín, propoxyfén, salicyláty a sulfónamidové antibiotiká.
Medzi látky, ktoré môžu zoslabovať účinok znižujúci hladinu cukru v krvi, patria: kortikosteroidy, danazol, diazoxid, diuretiká, glukagón, izoniazid, estrogény a progestagény, fenotiazínové deriváty, somatotropín, sympatomimetiká (napr. epinefrín [adrenalín], salbutamol, terbutalín), tyroidné hormóny, atypické antipsychotické lieky (napr. klozapín a olanzapín) a inhibítory proteázy.
Betablokátory, klonidín, soli lítia alebo alkohol môžu buď zosilňovať alebo zoslabovať účinok inzulínu znižujúci hladinu cukru v krvi.Pentamidín môže spôsobiť hypoglykémiu, po ktorej môže niekedy nasledovať hyperglykémia.
Pod vplyvom sympatolytík, ako sú betablokátory, klonidín, guanetidín a rezerpín, sa naviac môžu oslabiť alebo chýbať príznaky adrenergnej kontraregulácie.
4.6 Fertilita, gravidita a laktácia
Gravidita
Z kontrolovaných klinických štúdii nie sú k dispozícii žiadne klinické údaje o gravidných ženách vystavených účinku inzulínu glargín. Údaje o stredne veľkom počte gravidných žien (závery z počtu
300-1000 gravidít) vystavených účinku inzulínu glargín uvádzaného na trh nepreukázali nežiaduce účinky inzulínu glargín na graviditu a nepreukázali malformácie ani toxicitu inzulínu glargín pre plod/novorodenca.
Údaje o zvieratách nepreukázali reprodukčnú toxicitu.
Použitie Lantusu počas gravidity sa môže zvážiť, ak je to nevyhnutné.
Pre pacientky s predtým existujúcou alebo gestačnou cukrovkou je dôležité udržiavanie dobrej metabolickej kontroly počas gravidity. Nároky na inzulín môžu počas prvého trimestra poklesnúť a
v druhom a treťom trimestri všeobecne stúpajú. Okamžite po pôrode nároky na inzulín rapídne klesnú
(zvýšené riziko hypoglykémie). Nevyhnutné je starostlivé sledovanie glykémie.
Dojčenie
Nie je známe, či sa inzulín glargín vylučuje do materského mlieka. Nepredpokladajú sa žiadne metabolické účinky požitého inzulínu glargín na dojčeného novorodenca/dieťa, keďže inzulín glargín ako peptid sa spracováva na aminokyseliny v ľudskom tráviacom trakte. Dojčiace matky môžu vyžadovať úpravu dávky inzulínu a diétu.
Fertilita
Štúdie na zvieratách nepreukázali priame škodlivé účinky na fertilitu.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať strojeNásledkom hypoglykémie alebo hyperglykémie, alebo napríklad ako dôsledok zhoršenia zraku, sa môže zhoršiť pacientova schopnosť sústrediť sa a reagovať. To môže predstavovať riziko
v situáciách, kedy sú tieto schopnosti zvlášť dôležité (napr. vedenie vozidla alebo obsluha strojov).
Pacientom majú byť odporučené také opatrenia, aby sa počas vedenia vozidla vyhli hypoglykémii. To je obzvlášť dôležité pre tých, ktorí majú oslabené alebo chýbajúce varovné príznaky hypoglykémie, alebo majú časté hypoglykemické príhody. Za týchto okolností sa musí zvážiť, či je vhodné viesť vozidlo alebo obsluhovať stroje.
4.8 Nežiaduce účinkyHypoglykémia je vo všeobecnosti najčastejšou nežiaducou reakciou inzulínovej liečby, ktorá sa môže vyskytnúť, ak je dávka inzulínu privysoká vzhľadom na potrebu inzulínu.
Z klinických štúdií vyplynuli nasledujúce nežiaduce účinky, ktoré sú zoradené podľa tried orgánových systémov a v poradí podľa klesajúceho výskytu (veľmi časté: ≥ 1/10; časté: ≥ 1/100 až < 1/10; menej časté: ≥ 1/1000 až < 1/100; zriedkavé: ≥ 1/10 000 až < 1/1000; veľmi zriedkavé: < 1/10 000).
V rámci jednotlivých skupín frekvencií sú nežiaduce účinky usporiadané v poradí klesajúcej závažnosti.
MedDRA
triedy orgánových systémov
| Veľmi časté
| Časté
| Menej časté
| Zriedkavé
| Veľmi zriedkavé
|
Poruchy
imunitného systému
|
|
|
| Alergické
reakcie
|
|
Poruchy
metabolizmu a výživy
| Hypoglykémia
|
|
|
|
|
Poruchy nervového
systému
|
|
|
|
| Dysgeúzia
|
Poruchy zraku
|
|
|
| Zhoršené
videnie
Retinopatia
|
|
Poruchy kože
a podkožného tkaniva
|
| Lipohypertrofia
| Lipoatrofia
|
|
|
Poruchy
kostrovej
a svalovej sústavy
a spojivového tkaniva
|
|
|
|
| Myalgia
|
Celkové poruchy
a reakcie
v mieste podania
|
| Reakcie v mieste
podania injekcie
|
| Edém
|
|
Poruchy metabolizmu a výživy
Závažné ataky hypoglykémie, najmä ak sú rekurentné, môžu spôsobiť neurologické poškodenie.
Dlhotrvajúce alebo závažné hypoglykemické príhody môžu ohroziť život.
Znakom a príznakom neuroglykopénie predchádzajú u mnohých pacientov znaky adrenergnej kontraregulácie. Vo všeobecnosti platí, že čím väčší a rýchlejší je pokles krvnej glukózy, tým výraznejší je fenomén kontraregulácie a jej príznakov.
Poruchy imunitného systému
Bezprostredné alergické reakcie na inzulín sú zriedkavé. Takéto reakcie na inzulín (vrátane inzulínu
glargín) alebo na pomocné látky môžu byť spojené napríklad s generalizovanými kožnými reakciami, angioedémom, bronchospazmom, hypotenziou a šokom a môžu ohroziť život.
Podávanie inzulínu môže spôsobiť tvorbu protilátok. V klinických štúdiách sa pozorovali protilátky vykazujúce skrížené reakcie s ľudským inzulínom a inzulínom glargín rovnako v skupine pacientov liečených NPH inzulínom, ako aj v skupine pacientov liečených inzulínom glargín. V zriedkavých prípadoch si môže prítomnosť týchto inzulínových protilátok vyžiadať úpravu dávok inzulínu, aby sa upravil sklon ku hyper- alebo hypoglykémii.
Poruchy oka
Výrazné zmeny glykemickej kontroly môžu dočasne zhoršiť zrak tým, že sa prechodne zmení
zdurenie a refrakčný index šošovky.
Dlhodobo zlepšená glykemická kontrola zmenšuje riziko progresie diabetickej retinopatie. Avšak zintenzívnenie inzulínovej liečby s náhlym zlepšením glykemickej kontroly môže sprevádzať dočasné zhoršenie diabetickej retinopatie. U pacientov s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou, môžu ťažké hypoglykemické príhody vyústiť do prechodnej amaurózy.
Poruchy kože a podkožného tkaniva
Rovnako ako pri každej inzulínovej liečbe sa môže v mieste injekcie vyskytnúť lipodystrofia, ktorá
vedie k oneskorenej lokálnej absorpcii inzulínu. Priebežné striedanie miesta injekcie v rámci určitej injekčnej oblasti môže pomôcť znížiť alebo zabrániť takýmto reakciám.
Celkové poruchy a reakcie v mieste podania
K reakciám v mieste podania injekcie patrí sčervenanie kože, bolesť, svrbenie, žihľavka, opuch alebo
zápal. Väčšina miernych reakcií na inzulín v mieste injekcie obvykle vymizne za niekoľko dní až týždňov.
Inzulín môže zriedkavo spôsobiť retenciu sodíka a opuch, najmä ak sa pôvodne slabá metabolická kontrola zlepšila intenzifikovanou inzulínovou liečbou.
Pediatrickí pacienti
Vo všeobecnosti bezpečnostný profil u detí a dospievajúcich vo veku ≤ 18 rokov je podobný
bezpečnostnému profilu u dospelých.
Správy o nežiaducich reakciách z postmarketingového sledovania zahŕňali u detí a dospievajúcich vo veku ≤ 18 rokov pomerne častejšie reakcie v mieste vpichu (bolesť v miete vpichu, reakcie v mieste vpichu) a kožné reakcie (vyrážka, urtikária) ako u dospelých (vek > 18 rokov).
Nie sú dostupné žiadne klinické štúdie, ktoré by zahŕňali údaje o bezpečnosti u detí mladších ako
6 rokov.
4.9 Predávkovanie
Príznaky
Predávkovanie inzulínom môže viesť k ťažkej a niekedy dlhotrvajúcej a život ohrozujúcej
hypoglykémii.
Liečba
Mierne hypoglykemické príhody sa obvykle liečia perorálnymi sacharidmi. Môže byť potrebná úprava
dávky lieku, jedálneho lístka alebo telesnej aktivity.
Závažnejšie príhody spojené s kómou, záchvatmi alebo neurologickým poškodením možno liečiť intramuskulárnym alebo subkutánnym podaním glukagónu alebo intravenóznym podaním koncentrovanej glukózy. Keďže hypoglykémia sa po zdanlivom klinickom zotavení môže vrátiť, pacient musí udržiavať príjem sacharidov a je nutné pacienta pozorovať.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Lieky používané na liečbu diabetu. Inzulíny a injekčné analógy, dlhopôsobiace.
ATC kód: A10A E04.
Inzulín glargín je ľudský inzulínový analóg vyvinutý tak, aby mal nízku rozpustnosť v neutrálnom pH. Je úplne rozpustný v injekčnom roztoku Lantusu s kyslým pH (pH 4). Po injekcii do podkožného tkaniva sa kyslý roztok neutralizuje, následkom čoho sa tvoria mikroprecipitáty, z ktorých sa priebežne uvoľňuje v malých množstvách inzulín glargín, čim sa zaisťuje hladký a predvídateľný profil priebehu koncentrácie v závislosti od času bez vrcholov s predĺženým trvaním účinku.
Väzba inzulínu na receptory: Vzhľadom na väzbovú kinetiku receptorov inzulínu sa inzulín glargín veľmi podobá ľudskému inzulínu. Preto možno hovoriť o tom istom spôsobe účinku cez receptory inzulínu ako u ľudského inzulínu.
Primárny účinok inzulínu, vrátane inzulínu glargín, je regulácia glukózového metabolizmu. Inzulín a jeho analógy znižujú hladinu krvnej glukózy stimuláciou periférneho vychytávania glukózy, najmä kostrovým svalstvom a tukom a inhibíciou tvorby glukózy v pečeni. Inzulín inhibuje lipolýzu
v adipocytoch, inhibuje proteolýzu a zvyšuje syntézu proteínov.
V klinických farmakologických štúdiách sa ukázalo, že intravenózny inzulín glargín a ľudský inzulín sú pri rovnakých dávkach rovnocenné. Telesná aktivita a iné premenné môžu ovplyvňovať časový priebeh účinku inzulínu glargín rovnako ako pri všetkých inzulínoch.
V euglykemických uzatvorených štúdiách so zdravými dobrovoľníkmi alebo pacientami s diabetes
1. typu, bol nástup účinku subkutánneho inzulínu glargín pomalší ako u ľudského NPH inzulínu, jeho profil účinku bol hladký, bez vrcholov a s predĺženým trvaním účinku.
Nasledujúci graf zobrazuje výsledky štúdie u pacientov:
Profil účinku u pacientov s diabetes typu I
6
5
4
inzulín glargín

3 NPH inzulín
2
1
0
0 10 20 30
čas (h) po s.c. injekcii
ukončenie pozorovania





∗ udáva sa ako množstvo infundovanej glukózy na udržanie konštantných plazmatických hladín glukózy (priemerné hodinové hodnoty).
Dlhšie trvanie účinku podkožne podaného inzulínu glargín priamo súvisí s jeho nižšou absorbčnou rýchlosťou a umožňuje podávanie raz denne. Časový priebeh účinku inzulínu a inzulínových analógov, ako je inzulín glargín, sa môže značne líšiť u rôznych jedincov alebo u toho istého jedinca.
Príznaky hypoglykémie alebo hormonálnych odpovedí kontraregulácie boli v klinickej štúdii podobné po intravenóznom podaní inzulínu glargín a ľudského inzulínu u zdravých dobrovoľníkov aj u pacientov s diabetes 1. typu.
Účinky inzulínu glargín (podávaný jedenkrát denne) na diabetickú retinopatiu sa vyhodnocovali v otvorenej 5-ročnej štúdii kontrolovanej NPH (NPH podávaný dvakrát denne) u 1024 pacientov s diabetom 2. typu, u ktorých bola zistená progresia retinopatie o 3 stupne a viac na základe
vyhodnocovania snímky očného pozadia podľa škály Early Treatment Diabetic Retinopathy Study (ETDRS). Pri porovnaní inzulínu glargín s NPH inzulínom sa nepozoroval žiadny významný rozdiel v progresii diabetickej retinopatie.
Pediatrická populáciaV randomizovanej, kontrolovanej klinickej štúdii boli pediatrickí pacienti (vo veku od 6 do 15 rokov)
s diabetom 1. typu (n = 349) liečení po dobu 28 týždňov v inzulínovom režime bazál-bolus, kde bol použitý bežný ľudský inzulín pred každým jedlom. Inzulín glargín sa podával jedenkrát denne pred spaním a NPH ľudský inzulín sa podával jedenkrát alebo dvakrát denne. V obidvoch liečených skupinách sa pozorovali podobné účinky na glykohemoglobín a výskyt symptomatickej hypoglykémie, avšak hladina plazmatickej glukózy nalačno klesla z východiskovej hodnoty viac v skupine s inzulínom glargin ako v skupine s NPH. V skupine s inzulínom glargín bola taktiež menej častý výskyt ťažkej hypoglykémie. 143 pacientov liečených inzulínom glargín v tejto štúdii pokračovalo v liečbe inzulínom glargín v nekontrolovanom predĺžení štúdie pričom sledovanie trvalo priemerne 2 roky. Počas tejto predĺženej liečby inzulínom glargín sa nezaznamenali žiadne nové signály týkajúce sa bezpečnosti.
Taktiež sa uskutočnila „crossover“ štúdia (so skríženým dizajnom) porovnávajúca liečbu inzulínom glargín plus inzulín lispro s liečbou inzulínom NPH plus bežný ľudský inzulín (každá liečba sa podávala 16 týždňov v náhodnom poradí) u 26 dospievajúcich vo veku 12 až 18 rokov s diabetom
1. typu. Rovnako ako vo vyššie uvedenej pediatrickej štúdii pokles hladiny plazmatickej glukózy nalačno z východiskovej hodnoty bol väčší v skupine s inzulínom glargín ako v skupine s NPH. Zmeny HbA1c z východiskovej hodnoty boli v obidvoch liečených skupinách podobné; hodnoty hladiny glukózy v krvi zaznamenané počas noci boli významne vyššie v skupine inzulín glargín / lispro ako v skupine NPH/bežný ľudský inzulín, s priemernou najnižšou hodnotou (nadir) 5,4 mmol/l oproti 4,1 mmol/l. Tomu zodpovedal výskyt nočnej hypoglykémie, ktorý bol 32 % v skupine inzulín glargín / lispro oproti 52 % v skupine NPH / bežný ľudský inzulín.
5.2 Farmakokinetické vlastnosti
U zdravých jedincov a diabetikov ukázali sérové koncentrácie inzulínu pomalšiu a dlhšiu absorpciu a po subkutánnej injekcii inzulínu glargín v porovnaní s ľudským NPH inzulínom chýba vrchol. Koncentrácie teda zodpovedali časovému profilu farmakodynamického účinku inzulínu glargín. Vyššie uvedený graf ukazuje profily účinku inzulínu glargín a NPH inzulínu.
Inzulín glargín podaný raz denne dosiahne hladiny rovnovážneho stavu za 2-4 dni po prvej dávke. Pri intravenóznom podaní je polčas eliminácie inzulínu glargín a ľudského inzulínu porovnateľný.
U ľudí sa inzulín glargín čiastočne degraduje v podkožnom tkanive v uhlíkovom zakončení beta reťazca a tvoria sa účinné metabolity 21A-Gly-inzulín a 21A-gly-des-30B-Thr-inzulín.
V plazme je taktiež prítomný nezmenený inzulín glargín a produkty degradácie.
V klinických štúdiách sa v jednotlivých podskupinách rozdelených podľa veku a rodu nezistili žiadne rozdiely v bezpečnosti a účinnosti pri liečbe inzulínom glargín v porovnaní s celkovou študovanou populáciou.
Paediatrická populácia
Špecifická farmakokinetická štúdia na deťoch alebo dospievajúcich sa nerobila.
5.3 Predklinické údaje o bezpečnosti
Predklinické údaje získané na základe obvyklých farmakologických štúdií bezpečnosti, toxicity po opakovanom podaní, genotoxicity, karcinogénneho potenciálu a reprodukčnej toxicity neodhalili žiadne osobitné riziko pre ľudí.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
chlorid zinočnatý, metakrezol, glycerol,
kyselina chlorovodíková, hydroxid sodný,
voda na injekciu.
6.2 Inkompatibility
Tento liek sa nesmie miešať so žiadnymi inými liekmi.
6.3 Čas použiteľnosti
3 roky.
Čas použiteľnosti po prvom použití pera
Liek sa môže uchovávať maximálne 4 týždne pri teplote neprevyšujúcej 25 °C°tak, aby nebol vystavený priamemu teplu ani priamemu svetlu. Perá, ktoré sa používajú, sa nesmú uchovávať v chladničke. Po každej injekcii sa musí na pero opäť nasadiť kryt na ochranu pred svetlom.
6.4 Špeciálne upozornenia na uchovávanie
Nepoužívané perá
Uchovávajte v chladničke (2 °C–8 °C).
Neuchovávajte v mrazničke. Nedávajte Lantus blízko mraziacej časti ani zmrazeného balenia. Uchovávajte naplnené pero vo vonkajšom obale na ochranu pred svetlom.
Používané perá
Upozornenia na uchovávanie, pozri časť 6.3.
6.5 Druh obalu a obsah balenia
3 ml roztoku v náplni (bezfarebné sklo typu I) s čiernym piestom (bromobutylová guma) a tesniacim krytom (hliník) so zátkou (guma z bromobutylu alebo z polyizoprénového laminátu a bromobutylu). Náplne sú zaplombované do jednorazových perových injektorov. Balenie neobsahuje ihly. Dostupné sú balenia 1, 3, 4, 5, 6, 8, 9 a 10 pier. Nie všetky veľkosti balenia musia byť uvedené na trh.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Predtým ako sa pero použije prvýkrát, musí sa skladovať 1 až 2 hodiny pri izbovej teplote.
Pred použitím skontrolujte náplň. Môže sa použiť len ak je roztok číry, bezfarebný, bez viditeľných tuhých častíc a len ak má konzistenciu podobnú vode. Keďže Lantus je roztok, nevyžaduje pred použitím resuspenzáciu.
Lantus sa nesmie miešať so žiadnym iným inzulínom a nesmie sa ani riediť. Miešanie alebo riedenie môže zmeniť jeho čas/profil účinku a miešanie môže spôsobiť precipitáciu.
Prázdne perá nesmú byť opätovne použité a musia byť náležite zlikvidované.
Aby sa zabránilo možným prenosným ochoreniam, musí každé pero používať len jeden pacient.
Zaobchádzanie s perom
Pacient musí byť upozornený, aby si pred použitím SoloStaru pozorne prečítal návod na používanie, ktorý je súčasťou písomnej informácie pre používateľov.
Uzáver pera Ihla pera (nie je súčasťou balenia)
Ochranné tesnenie
Inzulínový zásobník
Telo pera
Ukazovateľ
dávky
Vonkajší
kryt ihly
Vnútorný kryt
hly

Ihla
Gumené tesnenie
Prepínač
dávky
Injekčné tlačidlo
Schematický nákres pera
Dôležité informácie pre používanie SoloStaru:
• Pred každým použitím sa musí dôkladne upevniť nová ihla a musí sa urobiť skúška bezpečnosti. Musia sa používať len ihly, ktoré sú vhodné na používanie so SoloStarom.
• Vyžaduje sa zvláštna opatrnosť, aby sa predišlo náhodným poraneniam ihlou a prenosu infekcií.
• Nikdy sa nesmie použiť SoloStar, ak je poškodený, alebo ak si nie je pacient istý či funguje správne.
• Pre prípad straty alebo poškodenia SoloStaru musí mať vždy pacient k dispozícii náhradný
SoloStar.
Pokyny na uchovávanie
Pozrite si, prosím, časť 6.4 tohto SPC, kde sú uvedené pokyny ako uchovávať SoloStar.
Ak sa SoloStar uchováva na chladnom mieste, musí sa odtiaľ vziať 1 až 2 hodiny pred podaním injekce, aby sa oteplil. Injikovanie chladného inzulínu je bolestivejšie.
Použitý SoloStar sa musí zlikvidovať v súlade s lokálnymi požiadavkami.
Obsluha
SoloStar je nutné chrániť pred prachom a nečistotami. Vonkajšiu stranu SoloStaru je možné čistiť vlhkou handričkou.
Pero sa nesmie namáčať, umývať ani mastiť, môže sa tým poškodiť.
SoloStar je navrhnutý tak, aby sa s ním pracovalo presne a bezpečne. Má sa s ním zaobchádzať starostlivo. Pacient sa musí vyhýbať situáciám, kde sa môže pero poškodiť. Ak má pacient obavy, že SoloStar môže byť poškodený, musí použiť nový SoloStar.
Krok 1. Kontrola inzulínu
Musí sa skontrolovať označenie na pere, aby bolo isté, že obsahuje správny inzulín. Lantus SoloStar je sivej farby s červeným injekčným tlačidlom. Po odstránení uzáveru pera sa musí skontrolovať vzhľad inzulínu: roztok inzulínu musí byť číry, bezfarebný, bez viditeľných tuhých častíc a musí mať konzistenciu podobnú vode.
Krok 2. Upevnenie ihly
Môžu sa používať len ihly, ktoré sú vhodné na používanie so SoloStarom.
Na každú injekciu sa musí použiť vždy nová sterilná ihla. Po odstránení uzáveru pera sa ihla musí dôkladne nasadiť na pero tak, aby bola s ním v jednej rovine.
Krok 3. Skúška bezpečnosti
Pred každou injekciou sa musí urobiť skúška bezpečnosti, aby sa uistilo, že pero a ihla fungujú správne, a aby sa odstránili vzduchové bubliny.
Musí sa nastaviť dávka 2 jednotky.
Vonkajší a vnútorný kryt ihly sa musia odstrániť.
Pero sa musí držať tak, aby ihla smerovala nahor, a súčasne sa musí jemne poklepávať prstom na inzulínový zásobník, aby sa všetky vzduchové bubliny dostali k ihle.
Potom sa injekčné tlačidlo musí úplne stlačiť.
Ak inzulín vystrekne cez hrot ihly, znamená to, že pero a ihla fungujú správne.
Ak sa na hrote ihly neobjaví žiadny inzulín, krok 3 sa musí opakovať dovtedy, kým sa inzulín na hrote ihly neobjaví.
Krok 4. Nastavenie dávky
Dávku možno nastaviť v krokoch po 1 jednotke, od minimálnej hodnoty 1 jednotky až po maximálnu hodnotu 80 jednotiek. Ak sa vyžaduje dávka vyššia ako 80 jednotiek, musí sa podať v dvoch alebo viacerých injekciách.
Ukazovateľ dávky musí po skúške bezpečnosti ukazovať „0“. Dávka sa tak môže nastaviť.
Krok 5. Podanie dávkyPacient musí byť o injekčnej technike informovaný svojím lekárom. Ihla sa musí vpichnúť do kože.
Injekčné tlačidlo sa musí úplne zatlačiť. Potom sa musí držať zatlačené 10 sekúnd pred vytiahnutím ihly. Tak sa zabezpečí, že bude podaná celá dávka inzulínu.
Krok 6. Odstránenie a likvidácia ihlyPo každej injekcii sa musí ihla odstrániť a zlikvidovať. To pomáha prevencii kontaminácie a/alebo infekcie, ako aj opätovnému nasatiu vzduchu a netesnosti. Ihly sa nesmú používať opakovane.
Vyžaduje sa špeciálna opatrnosť na odstránenie a likvidáciu ihly. Musia sa dodržiavať odporúčané bezpečnostné pokyny na odstránenie a likvidáciu ihly (uzatváracia technika použitím jednej ruky) za účelom zníženia rizika náhodných poranení ihlou a prenosu infekčných ochorení.
Na pero sa musí nasadiť uzáver.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCIISanofi-Aventis Deutschland GmbH, D-65926 Frankfurt am Main, Nemecko.
8. REGISTRAČNÉ ČÍSLAEU/1/00/134/030-037
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIEDátum prvej registrácie: 9. jún 2000
Dátum posledného predĺženia: 9. jún 2010
10. DÁTUM REVÍZIE TEXTUPodrobné informácie o tomto lieku sú dostupné na internetovej stránke Európskej liekovej agentúry
http://www.ema.europa.eu/.