
m boli hlásené prípady srdcového zlyhania, predovšetkým u pacientov s rizikovými faktormi pre rozvoj srdcového zlyhania. Preto je potrebné
súčasné použitie pioglitazónu a Insumanu starostlivo zvážiť. V prípade, že sa kombinácia použije,
u pacientov sa musia sledovať znaky a príznaky srdcového zlyhania, prírastku telesnej hmotnosti a edému. V prípade akéhokoľvek výskytu zhoršenia srdcových príznakov sa musí liečba
pioglitazónom ihneď prerušiť.
4.5 Liekové a iné interakcie
Niektoré látky ovplyvňujú glukózový metabolizmus a to si môže vyžiadať úpravu dávky ľudského inzulínu.
Látky, ktoré môžu stupňovať účinok znižujúci hladinu glukózy v krvi a zvýšiť náchylnosť na hypoglykémiu sú perorálne antidiabetiká, inhibítory enzýmu konvertujúceho angiotenzín (ACE), disopyramid, fibráty, fluoxetín, inhibítory monoaminooxidázy (MAO), pentoxifylín, propoxyfén, salicyláty a sulfónamidové antibiotiká.
Látky, ktoré môžu znižovať účinok znižujúci hladinu glukózy v krvi, sú kortikosteroidy, danazol, diazoxid, diuretiká, glukagón, izoniazid, estrogény a progestagény (napr. perorálna antikoncepcia), fenotiazínové deriváty, somatropín, sympatomimetiká (napríklad epinefrín [adrenalín], salbutamol, terbutalín), tyroidné hormóny, inhibítory proteázy a atypické antipsychotické lieky (napr. olanzapín a klozapín).
Betablokátory, klonidín, soli lítia alebo alkohol môžu buď zosilňovať alebo zoslabovať glykemický účinok inzulínu. Pentamidín môže spôsobiť hypoglykémiu, po ktorej môže niekedy nasledovať hyperglykémia.
Naviac príznaky adrenergnej protiregulácie sa môžu oslabiť alebo chýbať pod vplyvom sympatolytík ako sú betablokátory, klonidín, guanetidín a rezerpín.
4.6 Fertilita, gravidita a laktácia
G
r
avidita
Nie sú k dispozícii žiadne klinické údaje o gravidných ženách vystavených účinku ľudského inzulínu. Inzulín neprechádza placentárnou bariérou. Pri predpisovaní lieku gravidným ženám je potrebná opatrnosť.
Pre pacientky s preexistujúcim alebo gestačným diabetom je dôležité udržiavať dobrú kontrolu metabolizmu počas gravidity. Nároky na inzulín môžu klesnúť počas prvého trimestra a obvykle stúpajú počas druhého a tretieho trimestra. Bezprostredne po pôrode nároky na inzulín rapídne klesnú (zvýšené riziko hypoglykémie). Nevyhnutné je dôsledne monitorovať kontrolu glukózy.
Laktácia
Neočakávajú sa žiadne účinky na dojčatá. Počas dojčenia sa Insuman Infusat môže podávať. Pre dojčiace ženy býva potrebná úprava inzulínovej dávky a diéty.
Fertilita
Nie sú k dispozícii žiadne klinické údaje a údaje zo štúdií na zvieratách týkajúce sa ovplyvnenia mužskej alebo ženskej fertility ľudským inzulínom.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta sústrediť sa a reagovať môže byť následkom hypoglykémie alebo hyperglykémie, či napríklad zhoršeného videnia, narušená. Môže tak vzniknúť určité riziko v situáciách, kedy sú tieto schopnosti zvlášť dôležité (napr. vedenie vozidiel alebo obsluha strojov).
Pacienti majú byť poučení, aby urobili opatrenia na zabránenie hypoglykémie počas vedenia vozidla, čo je dôležité najmä u tých, ktorí majú zníženú alebo chýbajúcu schopnosť vnímať varovné príznaky hypoglykémie alebo majú časté hypoglykemické príhody. Za týchto okolností sa musí zvážiť, či je vedenie vozidiel alebo obsluha strojov vhodná.
4.8 Nežiaduce účinky
Súhrnbezpečnostnéhoprofilu
Hypoglykémia, vo všeobecnosti najčastejšia nežiaduca reakcia inzulínovej liečby, sa môže objaviť, ak je dávka inzulínu v porovnaní s požadovaným množstvom inzulínu príliš vysoká. V klinických
štúdiách a počas použitia lieku po jeho uvedení na trh sa frekvencia výskytu líši u jednotlivých skupín
pacientov a dávkovacích režimov. Preto nie je možné uviesť žiadne špecifické frekvencie.
Zoznamnežiaducichreakciívtabuľkovomformáte
Nasledujúce súvisiace nežiaduce reakcie z klinických štúdií sú uvedené nižšie a to v súlade s triedami orgánových systémov a v poradí klesajúceho výskytu: veľmi časté (≥1/10); časté (≥ 1/100 až < 1/10); menej časté (≥ 1/1000 až < 1/100); zriedkavé (≥ 1/10 000 až < 1/1000); veľmi zriedkavé (<1/10 000), neznáme (z dostupných údajov).
V rámci každej skupiny frekvencie sú nežiaduce reakcie uvedené v poradí klesajúcej závažnosti.
T
rieda orgánových systémov podľa MedDRA
|
Č
asté
|
Menej časté
|
N
eznáme
|
P
oruchy imunitného systému
|
|
Šok
|
Okamžité alergické
reakcie (hypotenzia, angioneurotický edém,
bronchospazmus,
generalizované kožné reakcie);
Inzulínové protilátky
|
P
oruchy metabolizmu a výživy
|
Edém
|
|
Hypoglykémia;
Retencia sodíka
|
P
oruchy oka
|
|
|
Proliferatívna
retinopatia;
Diabetická retinopatia; Porucha zraku
|
P
oruchy kože
a podkožného tkaniva
|
|
|
Lipodystrofia
|
C
elkové ochorenia a reakcie v mieste
podania
|
Reakcie v mieste
vpichu
|
Žihľavka v mieste
vpichu
|
Zápal v mieste vpichu;
Bolesť v mieste vpichu; Svrbenie v mieste
vpichu;
Sčervenanie v mieste vpichu;
Opuch v mieste vpichu
|
O
pis
vybraných
nežiaducich
reakcií
Poruchy imunitného systému
Okamžité alergické reakcie na inzulín alebo pomocné látky môžu byť život ohrozujúce.
Podávanie inzulínu môže spôsobiť vytváranie inzulínových protilátok. V zriedkavých prípadoch môže prítomnosť takýchto inzulínových protilátok vyžadovať úpravu dávky inzulínu, aby sa tak upravila náchylnosť k hyper- alebo hypoglykémii.
Poruchy metabolizmu a výživyZávažné hypoglykemické záchvaty, predovšetkým ak sa opakujú, môžu viesť k neurologickému poškodeniu. Dlhotrvajúce alebo závažné hypoglykemické príhody môžu byť život ohrozujúce.
U veľkého počtu pacientov predchádzajú príznakom a symptómom neuroglykopénie známky adrenergnej protiregulácie. Vo všeobecnosti platí, že čím väčší a rýchlejší je pokles hladiny glukózy v krvi, tým výraznejší je fenomén protiregulácie a jeho symptómov.
Inzulín môže spôsobovať retenciu sodíka a edém, predovšetkým ak sa slabá metabolická kontrola zvýšila zintezívnením inzulínovej liečby.
Poruchy okaVýrazná zmena kontroly glykémie môže spôsobovať dočasné zhoršenie zraku v dôsledku prechodnej zmeny v zdurení a indexe lomu šošoviek.
Dlhodobé zlepšenie kontroly glykémie znižuje riziko progresie diabetickej retinopatie. Avšak zintezívnenie inzulínovej liečby s náhlym zlepšením kontroly glykémie môže byť spojené s prechodným zhoršením diabetickej retinopatie.
Poruchy kože a podkožného tkanivaV mieste vpichu môže vzniknúť lipodystrofia a môže spomaliť lokálnu absorpciu inzulínu. Znížiť alebo zabrániť týmto reakciám pomôže neustále striedanie miesta vpichu v danej oblasti podania.
C
elkové poruchy a reakcie v mieste podania
Väčšina miernych reakcií na inzulín v mieste vpichu zvyčajne ustúpi v priebehu pár dní alebo týždňov.
Hláseniepodozrenínanežiaducereakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného
v
Prílohe V.4.9 PredávkovaniePríznakyPredávkovanie inzulínom môže spôsobiť závažnú a niekedy dlhotrvajúcu a životu nebezpečnú hypoglykémiu.
LiečbaMierne príhody hypoglykémie je zvyčajne možné liečiť perorálnym podávaním sacharidov.
V niektorých prípadoch sa vyžaduje úprava dávkovacej schémy lieku, stravovacích návykov alebo fyzickej aktivity.
Závažnejšie príhody sprevádzané kómou, záchvatom alebo neurologickým poškodením možno liečiť intramuskulárnym/subkutánnym podaním glukagónu alebo intravenóznym podaním koncentrovaného roztoku glukózy. Môže byť nevyhnutné udržiavať príjem sacharidov a pozorovať pacienta, pretože hypoglykémia sa po zdanlivom klinickom zotavení môže navrátiť.
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Antidiabetiká, inzulíny a analógy na injekciu, rýchlopôsobiace, ATC
kód: A10AB01.
SpôsobúčinkuInzulín
- znižuje hladinu krvej glukózy, podporuje anabolické účinky a tlmí katabolické deje,
- zvyšuje transport glukózy do buniek, ako aj tvorbu glykogénu v svaloch a pečeni a zlepšuje utilizáciu pyruvátu. Inhibuje glykogenolýzu a glukoneogenézu,
- zvyšuje lipogenézu v pečeni a tukovom tkanive a inhibuje lipolýzu,
- podporuje príjem aminokyselín do buniek a podporuje proteosyntézu,
- zvyšuje príjem draslíka do buniek.
FarmakodynamickéúčinkyInsuman Infusat je inzulín s rýchlym nástupom a krátkym trvaním účinku.
5.2 Farmakokinetické vlastnostiU zdravých jedincov je polčas inzulínu v sére približne 4 až 6 minút. Je dlhší u pacientov s ťažkou renálnou insuficienciou. Avšak je potrebné poznamenať, že farmakokinetika inzulínu neodzrkadľuje jeho metabolický účinok.
5.3 Predklinické údaje o bezpečnosti
Akútna toxicita sa sledovala u potkanov po subkutánnom podaní. Nenašli sa žiadne dôkazy toxických účinkov. Štúdie zamerané na lokálnu toleranciu po subkutánnom a intramuskulárnom podaní u králikov nepriniesli žiadne pozoruhodné zistenia. Štúdie farmakodynamických účinkov po subkutánnom podaní u králikov a psov odhalili očakávané hypoglykemické reakcie.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
fenol,
chlorid zinočnatý, trometamol,
poloxamér 171,
glycerol,
kyselina chlorovodíková (na úpravu pH), voda na injekciu.
6.2 Inkompatibility
Tento liek sa nesmie miešať s inými liekmi okrem tých, ktoré sú uvedené v časti 6.6.
Insuman Infusat sa nesmie miešať s roztokmi obsahujúcimi redukujúce látky ako tioly a sulfity. Miešanieinzulínov
Insuman Infusat sa nesmie miešať so žiadnym iným inzulínom alebo analógmi inzulínu.
Treba zabezpečiť, aby sa do roztoku inzulínu nedostal žiadny alkohol, ani iné dezinfekčné látky.
6.3 Čas použiteľnosti
2 roky.
Inzulín naplnený v zásobníku pumpy možno používať do 2 týždňov. Časpoužiteľnostipoprvompoužitíinjekčnejliekovky
Liek sa môže uchovávať maximálne 4 týždne pri teplote neprevyšujúcej 25°C tak, aby nebol
vystavený priamemu teplu ani priamemu svetlu.
Uchovávajte injekčnú liekovku vo vonkajšom obale na ochranu pred svetlom. Dátum prvého použitia sa odporúča zaznamenať na štítku.
6.4 Špeciálne podmienky na uchovávanie
Neotvorenéinjekčnéliekovky Uchovávajte v chladničke (2°C - 8°C). Neuchovávajte v mrazničke.
Nedávajte Insuman Infusat blízko mraziacej časti ani zmrazeného balenia. Uchovávajte injekčnú liekovku vo vonkajšom obale na ochranu pred svetlom.
Otvorenéinjekčnéliekovky
Podmienky na uchovávanie po prvom otvorení lieku, pozri časť 6.3.
6.5 Druh obalu a obsah balenia
10 ml roztoku v injekčnej liekovke (bezfarebné sklo typu I) s tesniacim krytom (hliník), zátkou
(chlorobutylová guma (typ I)) a odlamovacím krytom (polypropylén).
Dostupné sú balenia po 3 injekčných liekovkách.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekomInsuman Infusat sa musí použiť len ak je roztok číry, bezfarebný a bez viditeľných tuhých častíc a ak má podobnú konzistenciu ako voda.
Na použitie v inzulínovej pumpe sa Insuman Infusat naplní do sterilnej náplne v pumpe. Náplň sa musí použiť len jedenkrát.
Pred použitím sa musí plná náplň skladovať 1 – 2 hodiny pri izbovej teplote. Pred začiatkom infúzie sa musia odstrániť vzduchové bubliny (pozri návod na použitie pumpy).
Ak infúzna pumpa nefunguje, injekčný roztok možno natiahnuť z náplne do injekčnej striekačky
(vhodnej na inzulín s koncentráciou 100 IU/ml) a injikovať.
Insuman Infusat sa nesmie podávať v peristaltických pumpách so silikónovými hadicami. Pozri technický návod na použitie inzulínových púmp, časť Kontraindikácie.
Treba si uvedomiť, že neutrálny bežný inzulín precipituje pri pH približne 4,5 - 6,5.
Pred každou injekciou je nutné vždy skontrolovať označenie na inzulíne, aby sa zabránilo zámene ľudského inzulínu za iné inzulíny (pozri časť 4.4).
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými požiadavkami.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCIISanofi-Aventis Deutschland GmbH, D-65926 Frankfurt am Main, Nemecko
8. REGISTRAČNÉ ČÍSLAEU/1/97/030/053
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIEDátum prvej registrácie: 21. február 1997
Dátum posledného predĺženia: 21. február 2007
10 DÁTUM REVÍZIE TEXTUPodrobné informácie o tomto lieku sú dostupné na internetovej stránke Európskej agentúry pre lieky
http://www.ema.europa.eu.
1. NÁZOV LIEKU
Insuman Infusat 100 IU/ml injekčný roztok v náplni
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Každý ml obsahuje 100 IU ľudského inzulínu (zodpovedá 3,5 mg).
Každá náplň obsahuje 3,15 ml injekčného roztoku, čo zodpovedá 315 IU inzulínu. Jedna IU (medzinárodná jednotka) zodpovedá 0,035 mg bezvodého ľudského inzulínu.
Insuman Infusat je neutrálny inzulínový roztok (bežný inzulín).
Ľudský inzulín sa vyrába rekombinantnou DNA technológiou v Escherichia coli.
Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA Injekčný roztok v náplni. Roztok je číry, bezfarebný.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Diabetes mellitus, ktorý si vyžaduje inzulínovú liečbu.
4.2 Dávkovanie a spôsob podávania
Dávkovanie
Insuman Infusat bol špeciálne vyvinutý na používanie prostredníctvom externých prenosných inzulínových púmp. Je stabilizovaný, aby sa neznižovala jeho účinnosť pri mechanickej a teplotnej
záťaži v takýchto pumpách. Insuman Infusat je preto taktiež vhodný na kontinuálnu inzulínovú infúziu
pomocou iných konvenčných striekačkových púmp.
Požadované hladiny krvnej glukózy a dávkovacia schéma inzulínu sa musia určiť a prispôsobiť individuálne tak, aby vyhovovali pacientovej diéte, jeho fyzickej aktivite a životnému štýlu.
Denné dávky a časovanie podávania
Pri používaní externých inzulínových púmp časť dennej dávky inzulínu stečie v infúzii kontinuálne
(„základný podiel“) a zbytok sa podáva vo forme bolusových injekcií pred jedlami. Ďalšie informácie o infúznej pumpe nájdete v návode na použitie spolu s popisom funkcie a potrebnými bezpečnostnými
upozorneniami.
Nejestvujú žiadne pevné pravidlá pre dávkovaciu schému inzulínu. Priemerná denná potreba inzulínu je však obvykle 0,5 - 1,0 IU na kg telesnej hmotnosti. Základná metabolická potreba je 40% - 60% z celkovej dennej potreby. V dôsledku toho sa 40 – 60% podáva ako bazálny podiel a zbytok sa podáva vo forme bolusových injekcií pred jedlami.
Druhotná úprava dávky
Zlepšenie metabolickej kontroly môže zvýšiť citlivosť na inzulín, čo sa odrazí v zníženej potrebe inzulínu. Prispôsobenie dávky môže byť tiež potrebné napríklad ak:
- sa zmení hmotnosť pacienta,
- sa zmení životný štýl pacienta,
- sa objavia ďalšie okolnosti, ktoré môžu podporiť zvýšenú náchylnosť na hypo- alebo hyperglykémiu (pozri časť 4.4).
Osobitnéskupinypacientov
Starší pacienti (≧ 65 rokov)
U starších pacientov môže progresívna deteriorácia funkcie obličiek viesť k stálemu poklesu potreby inzulínu.
Poškodenie funkcie obličiek
U pacientov so zhoršenou funkciou obličiek sa môže dávka inzulínu znížiť na základe zníženého metabolizmu inzulínu.
Poškodenie funkcie pečene
U pacientov so závažne zhoršenou funkciou pečene sa môže znížiť potreba inzulínu na základe zníženej kapacity glukoneogenézy a zníženého metabolizmu inzulínu.
Spôsobpodania
Insuman Infusat sa nesmie podávať v peristaltických pumpách so silikónovými hadicami. Pozri technický návod na použitie inzulínových púmp, časť Kontraindikácie.
Insuman Infusat v náplniach sa môže podávať subkutánne, infúziou. Je vyvinutý pre podávanie v Hoechst Infusor a v H-Tron inzulínových pumpách. Môže sa taktiež podávať aj v iných inzulínových pumpách, ktoré sú opísané ako vhodné na tento inzulín a tento typ náplne (pozri návod na použitie pumpy). Používať sa musia iba tetraflouroetylénové a polyetylénové katétre.
Inzulín sa musí vždy podávať za antiseptických podmienok. Tieto zabezpečuje špeciálne zariadenie pre inzulínové pumpy (napr. katétre, kanyly).
Absorpcia inzulínu a tým aj účinok dávky na zníženie krvnej glukózy sa môže líšiť v závislosti od oblasti podania injekcie (napríklad brušná stena v porovnaní so stehnom). Miesta vpichu v rámci jednej injekčnej oblasti sa musia neustále striedať (vo všeobecnosti každý 1 až 3 dni).
Podrobnejšie informácie o použití, pozri časť 6.6.
4.3 Kontraindikácie
Precitlivenosť na inzulín alebo na ktorúkoľvek z pomocných látok uvedených v časti 6.1.
4.4 Osobitné upozornenia a opatrenia pri používaní
Pacienti precitlivení na Insuman Infusat, v prípade, keď nie je k dispozícii žiadny lepšie tolerovaný inzulínový liek, musia pokračovať v liečbe len pod prísnym lekárskym dohľadom a podľa potreby aj so sprievodnou protialergickou liečbou.
Ak pacienti s alergiou na zvierací inzulín prechádzajú na Insuman Infusat, odporúča sa pred liečbou intradermálne testovanie vzhľadom na možnosť skrížených imunologických reakcií.
V prípade hypoglykémie sa musí inzulínová pumpa dočasne vysadiť, aspoň dovtedy, kým pacient úplne nadobudne vedomie.
V prípade nedostatočnej kontroly glukózy alebo pri tendencii k hyper- alebo hypoglykemickým príhodám sa musí pred samotnou úpravou dávky zvážiť, či pacient dodržiava predpísaný liečebný režim, miesta vpichu a správnu techniku podania.
Prechod
na
Insuman
Infusat
Prestavenie pacienta na iný typ alebo druh inzulínu sa musí robiť pod prísnym lekárskym
dohľadom. Zmena sily, druhu (iný výrobca), typu (bežný, NPH, lente, s dlhotrvajúcim účinkom, atď.), pôvodu (zvierací, ľudský, analóg ľudského inzulínu) a/alebo výrobného postupu môže mať za
následok to, že je potrebné zmeniť dávku.
Potreba prispôsobiť (napr. znížiť) dávku môže nastať ihneď po prechode alebo sa môže vyvinúť postupne v priebehu niekoľkých týždňov.
Potreba zredukovať dávkovaciu schému inzulínu po prechode zo zvieracieho na ľudský inzulín môže nastať najmä u pacientov, ktorí:
- mali už predtým dosť nízke hladiny krvnej glukózy,
- majú sklon ku hypoglykémii,
- už predtým potrebovali vysoké dávky inzulínu ako dôsledok prítomnosti inzulínových protilátok.
Počas prechodu a v prvých týždňoch po ňom sa odporúča dôkladné sledovanie metabolizmu.
U pacientov vyžadujúcich vysoké dávky inzulínu, vzhľadom na prítomnosť inzulínových protilátok, sa musí zvážiť prechod pod lekárskym dohľadom v nemocnici alebo podobnom zariadení
Hypoglykémia
Hypoglykémia môže nastať, ak dávka inzulínu príliš prevyšuje jeho potrebu.
Zvýšená opatrnosť a prísna kontrola krvnej glukózy sa odporúčajú u pacientov so zvýšeným rizikom hypoglykémie, ako sú pacienti so signifikantnou stenózou koronárnych artérií alebo krvných ciev zásobujúcich mozog (riziko srdcových alebo mozgových hypoglykemických komplikácií) rovnako ako pacientom s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou (riziko prechodnej amaurózy následkom hypoglykémie).
Pacienti majú byť informovaní o prípadoch, kedy varovné príznaky hypoglykémie slabnú. Varovné príznaky hypoglykémie sa môžu meniť, môžu byť menej výrazné alebo u určitých rizikových skupín môžu chýbať. Patria sem pacienti:
- u ktorých sa výrazne zlepšila kontrola glykémie,
- u ktorých hypoglykémia nastupuje postupne,
- starší pacienti,
- po prechode zo zvieracieho inzulínu na ľudský inzulín,
- s autonómnou neuropatiou v súčasnosti,
- s dlhodobou anamnézou cukrovky,
- trpiaci psychickým ochorením,
- dostávajúci sprievodnú liečbu niektorými inými liekmi (pozri časť 4.5).
Tieto situácie môžu vyústiť do závažnej hypoglykémie (aj s možnou stratou vedomia), skôr ako si to pacient uvedomí.
Ak sa zaznamenajú normálne alebo znížené hodnoty glykovaného hemoglobínu, musí sa brať do úvahy možnosť rekurentných,nerozpoznaných (najmä nočných) príhod hypoglykémie.
Ak pacient dodržiava predpísanú dávkovaciu schému a diétny režim, správne podávanie inzulínu a pozná symptómy hypoglykémie, znižuje tým výrazne riziko hypoglykémie. Náchylnosť na hypoglykémiu, vyžadujúcu dôkladné monitorovanie, prípadne nevyhnutnosť úpravy dávky, zvyšuje veľký počet faktorov. Patria sem:
- zmena injekčnej oblasti,
- zvýšená citlivosť na inzulín (napr. po odstránení stresových faktorov),
- neobvyklá, zvýšená alebo dlhšie trvajúca fyzická aktivita,
- interkurentné ochorenie (napr. vracanie, hnačka),
- neprimeraný príjem potravy,
- vynechanie jedla,
- konzumácia alkoholu,
- určité nekompenzované poruchy endokrinného systému (napr. pri hypotyreóze a pri nedostatočnej činnosti adenohypofýzy alebo kôry nadobličiek),
- súbežné podávanie niektorých iných liekov.
Poruchyinzulínovejpumpy
Ak je katéter úplne zapchatý, behom pár hodín môže dôjsť k hyperglykémii, ketoacidóze a kóme. Akonáhle pacient zistí rýchly nárast glukózy v krvi, ktorý nesúvisí s bolusovou dávkou, musí sa skontrolovať, či katéter nie je upchatý.
Pre prípad poruchy pumpy musia pacienti vždy mať náhradu (injekčnú striekačku alebo pero) a dostatok inzulínu na subkutánnu injekciu. Ďalšie bezpečnostné upozornenia nájdete v návode na použitie pumpy.
Interkurentnéochorenia
Interkurentné ochorenia si vyžadujú intenzívne sledovanie metabolizmu. V mnohých prípadoch sa indikujú močové testy na ketóny a často býva potrebné upraviť dávku inzulínu. Nároky na inzulín sú
často zvýšené. Pacienti s diabetom mellitus 1.typu musia pravidelne konzumovať aspoň malé
množstvo sacharidov, dokonca aj keď sú schopní jesť len málo alebo vôbec nie alebo vracajú a pod. Inzulín sa nikdy nesmie úplne vynechať.
Omylypripoužitílieku
Boli hlásené omyly pri použití lieku, kedy boli náhodne použité iné formy Insumanu alebo iné inzulíny. Pred každou injekciou je nutné vždy skontrolovať označenie na inzulíne, aby sa zabránilo
zámene ľudského inzulínu za iné inzulíny.
KombináciaInsumanuspioglitazónom
Pri súčasnom použití pioglitazónu s inzulínom boli hlásené prípady srdcového zlyhania, predovšetkým u pacientov s rizikovými faktormi pre rozvoj srdcového zlyhania. Preto je potrebné
súčasné použitie pioglitazónu a Insumanu starostlivo zvážiť. V prípade, že sa kombinácia použije,
u pacientov sa musia sledovať znaky a príznaky srdcového zlyhania, prírastku telesnej hmotnosti a edému. V prípade akéhokoľvek výskytu zhoršenia srdcových príznakov sa musí liečba
pioglitazónom ihneď prerušiť.
4.5 Liekové a iné interakcie
Niektoré látky ovplyvňujú glukózový metabolizmus a to si môže vyžiadať úpravu dávky ľudského inzulínu.
Látky, ktoré môžu stupňovať účinok znižujúci hladinu glukózy v krvi a zvýšiť náchylnosť na hypoglykémiu sú perorálne antidiabetiká, inhibítory enzýmu konvertujúceho angiotenzín (ACE), disopyramid, fibráty, fluoxetín, inhibítory monoaminooxidázy (MAO), pentoxifylín, propoxyfén, salicyláty a sulfónamidové antibiotiká.
Látky, ktoré môžu znižovať účinok znižujúci hladinu glukózy v krvi, sú kortikosteroidy, danazol, diazoxid, diuretiká, glukagón, izoniazid, estrogény a progestagény (napr. perorálna antikoncepcia), fenotiazínové deriváty, somatropín, sympatomimetiká (napríklad epinefrín [adrenalín], salbutamol, terbutalín), tyroidné hormóny, inhibítory proteázy a atypické antipsychotické lieky (napr. olanzapín a klozapín).
Betablokátory, klonidín, soli lítia alebo alkohol môžu buď zosilňovať alebo zoslabovať glykemický účinok inzulínu. Pentamidín môže spôsobiť hypoglykémiu, po ktorej môže niekedy nasledovať hyperglykémia.
Naviac príznaky adrenergnej protiregulácie sa môžu oslabiť alebo chýbať pod vplyvom sympatolytík ako sú betablokátory, klonidín, guanetidín a rezerpín.
4.6 Fertilita, gravidita a laktácia
G
r
avidita
Nie sú k dispozícii žiadne klinické údaje o gravidných ženách vystavených účinku ľudského inzulínu. Inzulín neprechádza placentárnou bariérou. Pri predpisovaní lieku gravidným ženám je potrebná opatrnosť.
Pre pacientky s preexistujúcim alebo gestačným diabetom je dôležité udržiavať dobrú kontrolu metabolizmu počas gravidity. Nároky na inzulín môžu klesnúť počas prvého trimestra a obvykle stúpajú počas druhého a tretieho trimestra. Bezprostredne po pôrode nároky na inzulín rapídne klesnú (zvýšené riziko hypoglykémie). Nevyhnutné je dôsledne monitorovať kontrolu glukózy.
Laktácia
Neočakávajú sa žiadne účinky na dojčatá. Počas dojčenia sa Insuman Infusat môže podávať. Pre dojčiace ženy býva potrebná úprava inzulínovej dávky a diéty.
Fertilita
Nie sú k dispozícii žiadne klinické údaje a údaje zo štúdií na zvieratách týkajúce sa ovplyvnenia mužskej alebo ženskej fertility ľudským inzulínom.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta sústrediť sa a reagovať môže byť následkom hypoglykémie alebo hyperglykémie, či napríklad zhoršeného videnia, narušená. Môže tak vzniknúť určité riziko v situáciách, kedy sú tieto schopnosti zvlášť dôležité (napr. vedenie vozidiel alebo obsluha strojov).
Pacienti majú byť poučení, aby urobili opatrenia na zabránenie hypoglykémie počas vedenia vozidla, čo je dôležité najmä u tých, ktorí majú zníženú alebo chýbajúcu schopnosť vnímať varovné príznaky hypoglykémie alebo majú časté hypoglykemické príhody. Za týchto okolností sa musí zvážiť, či je vedenie vozidl alebo obsluha strojov vhodná.
4.8 Nežiaduce účinky
Súhrnbezpečnostnéhoprofilu
Hypoglykémia, vo všeobecnosti najčastejšia nežiaduca reakcia inzulínovej liečby, sa môže objaviť, ak je dávka inzulínu v porovnaní s požadovaným množstvom inzulínu príliš vysoká. V klinických
štúdiách a počas použitia lieku po jeho uvedení na trh sa frekvencia výskytu líši u jednotlivých skupín
pacientov a dávkovacích režimov. Preto nie je možné uviesť žiadne špecifické frekvencie.
Zoznamnežiaducichreakciívtabuľkovomformáte
Nasledujúce súvisiace nežiaduce reakcie z klinických štúdií sú uvedené nižšie a to v súlade s triedami orgánových systémov a v poradí klesajúceho výskytu: veľmi časté (≥1/10); časté (≥ 1/100 až < 1/10); menej časté (≥ 1/1000 až < 1/100); zriedkavé (≥ 1/10 000 až < 1/1000); veľmi zriedkavé (<1/10 000), neznáme (z dostupných údajov).
V rámci každej skupiny frekvencie sú nežiaduce reakcie uvedené v poradí klesajúcej závažnosti.
T
rieda orgánových systémov podľa MedDRA
|
Č
asté
|
Menej časté
|
N
eznáme
|
P
oruchy imunitného systému
|
|
Šok
|
Okamžité alergické
reakcie (hypotenzia, angioneurotický edém,
bronchospazmus,
generalizované kožné reakcie);
Inzulínové protilátky
|
P
oruchy metabolizmu a výživy
|
Edém
|
|
Hypoglykémia;
Retencia sodíka
|
P
oruchy oka
|
|
|
Proliferatívna
retinopatia;
Diabetická retinopatia; Porucha zraku
|
P
oruchy kože
a podkožného tkaniva
|
|
|
Lipodystrofia
|
C
elkové ochorenia a reakcie v mieste
podania
|
Reakcie v mieste
vpichu
|
Žihľavka v mieste
vpichu
|
Zápal v mieste vpichu;
Bolesť v mieste vpichu; Svrbenie v mieste
vpichu;
Sčervenanie v mieste vpichu;
Opuch v mieste vpichu
|
O
pis
vybraných
nežiaducich
reakcií
Poruchy imunitného systému
Okamžité alergické reakcie na inzulín alebo pomocné látky môžu byť život ohrozujúce.
Podávanie inzulínu môže spôsobiť vytváranie inzulínových protilátok. V zriedkavých prípadoch môže prítomnosť takýchto inzulínových protilátok vyžadovať úpravu dávky inzulínu, aby sa tak upravila náchylnosť k hyper- alebo hypoglykémii.
Poruchy metabolizmu a výživyZávažné hypoglykemické záchvaty, predovšetkým ak sa opakujú, môžu viesť k neurologickému poškodeniu. Dlhotrvajúce alebo závažné hypoglykemické príhody môžu byť život ohrozujúce.
U veľkého počtu pacientov predchádzajú príznakom a symptómom neuroglykopénie známky adrenergnej protiregulácie. Vo všeobecnosti platí, že čím väčší a rýchlejší je pokles hladiny glukózy v krvi, tým výraznejší je fenomén protiregulácie a jeho symptómov.
Inzulín môže spôsobovať retenciu sodíka a edém, predovšetkým ak sa slabá metabolická kontrola zvýšila zintezívnením inzulínovej liečby.
Poruchy okaVýrazná zmena kontroly glykémie môže spôsobovať dočasné zhoršenie zraku v dôsledku prechodnej zmeny v zdurení a indexe lomu šošoviek.
Dlhodobé zlepšenie kontroly glykémie znižuje riziko progresie diabetickej retinopatie. Avšak zintezívnenie inzulínovej liečby s náhlym zlepšením kontroly glykémie môže byť spojené s prechodným zhoršením diabetickej retinopatie.
Poruchy kože a podkožného tkanivaV mieste vpichu môže vzniknúť lipodystrofia a môže spomaliť lokálnu absorpciu inzulínu. Znížiť alebo zabrániť týmto reakciám pomôže neustále striedanie miesta vpichu v danej oblasti podania.
C
elkové poruchy a reakcie v mieste podania
Väčšina miernych reakcií na inzulín v mieste vpichu zvyčajne ustúpi v priebehu pár dní alebo týždňov.
Hláseniepodozrenínanežiaducereakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného
v
Prílohe V.4.9 PredávkovaniePríznakyPredávkovanie inzulínom môže spôsobiť závažnú a niekedy dlhotrvajúcu a životu nebezpečnú hypoglykémiu.
LiečbaMierne príhody hypoglykémie je zvyčajne možné liečiť perorálnym podávaním sacharidov.
V niektorých prípadoch sa vyžaduje úprava dávkovacej schémy lieku, stravovacích návykov alebo fyzickej aktivity.
Závažnejšie príhody sprevádzané kómou, záchvatom alebo neurologickým poškodením možno liečiť intramuskulárnym/subkutánnym podaním glukagónu alebo intravenóznym podaním koncentrovaného roztoku glukózy. Môže byť nevyhnutné udržiavať príjem sacharidov a pozorovať pacienta, pretože hypoglykémia sa po zdanlivom klinickom zotavení môže navrátiť.
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Antidiabetiká, inzulíny a analógy na injekciu, rýchlopôsobiace, ATC
kód: A10AB01.
SpôsobúčinkuInzulín
- znižuje hladinu krvej glukózy, podporuje anabolické účinky a tlmí katabolické deje,
- zvyšuje transport glukózy do buniek, ako aj tvorbu glykogénu v svaloch a pečeni a zlepšuje utilizáciu pyruvátu. Inhibuje glykogenolýzu a glukoneogenézu,
- zvyšuje lipogenézu v pečeni a tukovom tkanive a inhibuje lipolýzu,
- podporuje príjem aminokyselín do buniek a podporuje proteosyntézu,
- zvyšuje príjem draslíka do buniek.
FarmakodynamickéúčinkyInsuman Infusat je inzulín s rýchlym nástupom a krátkym trvaním účinku.
5.2 Farmakokinetické vlastnostiU zdravých jedincov je polčas inzulínu v sére približne 4 až 6 minút. Je dlhší u pacientov s ťažkou renálnou insuficienciou. Avšak je potrebné poznamenať, že farmakokinetika inzulínu neodzrkadľuje jeho metabolický účinok.
5.3 Predklinické údaje o bezpečnosti
Akútna toxicita sa sledovala u potkanov po subkutánnom podaní. Nenašli sa žiadne dôkazy toxických účinkov. Štúdie zamerané na lokálnu toleranciu po subkutánnom a intramuskulárnom podaní u králikov nepriniesli žiadne pozoruhodné zistenia. Štúdie farmakodynamických účinkov po subkutánnom podaní u králikov a psov odhalili očakávané hypoglykemické reakcie.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
fenol,
chlorid zinočnatý, trometamol, poloxamér 171, glycerol,
kyselina chlorovodíková (na úpravu pH), voda na injekciu.
6.2 Inkompatibility
Tento liek sa nesmie miešať s inými liekmi okrem tých, ktoré sú uvedené v časti 6.6.
Insuman Infusat sa nesmie miešať s roztokmi obsahujúcimi redukujúce látky ako tioly a sulfity. Miešanieinzulínov
Insuman Infusat sa nesmie miešať so žiadnym iným inzulínom alebo analógmi inzulínu.
Treba zabezpečiť, aby sa do roztoku inzulínu nedostal žiadny alkohol, ani iné dezinfekčné látky.
6.3 Čas použiteľnosti
2 roky.
Časpoužiteľnostipoprvompoužitínáplne
Liek (náplň, ktorá sa používa v pumpe) sa môže uchovávať maximálne 2 týždne.
6.4 Špeciálne podmienky na uchovávanie
Neotvorenénáplne
Uchovávajte v chladničke (2°C - 8°C). Neuchovávajte v mrazničke.
Nedávajte Insuman Infusat blízko mraziacej časti ani zmrazeného balenia. Náplň uchovávajte vo vonkajšom obale na ochranu pred svetlom.
Používanénáplne
Podmienky na uchovávanie po prvom otvorení lieku, pozri časť 6.3.
6.5 Druh obalu a obsah balenia
3,15 ml roztoku v náplni (bezfarebné sklo typu I) s piestom ( guma typu I, potiahnutá vrstvou fluoropolyméru (typu I, zmes chlorobutylu a prírodnej gumy)), tesniacim krytom (hliník) a zátkou s dierou (brombutylová guma (typ I)), s priloženým Luerovým kužeľom (bezfarebný polyetylén) a Luerovým krytom (bezfarebný polyetylén).
Dostupné sú balenia po 5 náplní.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Insuman Infusat sa musí použiť len ak je roztok číry, bezfarebný a bez viditeľných tuhých častíc a ak má podobnú konzistenciu ako voda.
Pred použitím sa musí Insuman Infusat skladovať 1 – 2 hodiny pri izbovej teplote. Pred začiatkom infúzie sa musia odstrániť vzduchové bubliny (pozri návod na použitie pumpy).
Ak infúzna pumpa nefunguje, injekčný roztok možno natiahnuť z náplne do injekčnej striekačky
(vhodnej na inzulín s koncentráciou 100 IU/ml) a injikovať.
Insuman Infusat sa nesmie podávať v peristaltických pumpách so silikónovými hadicami. Pozri technický návod na použitie inzulínových púmp, časť Kontraindikácie.
Treba si uvedomiť, že neutrálny bežný inzulín precipituje pri pH približne 4,5 - 6,5.
Pred každou injekciou je nutné vždy skontrolovať označenie na inzulíne, aby sa zabránilo zámene ľudského inzulínu za iné inzulíny (pozri časť 4.4).
Nepoužitý liek alebo odpad vzniknutý z lieku má byť zlikvidovaný v súlade s národnými požiadavkami.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCIISanofi-Aventis Deutschland GmbH, D-65926 Frankfurt am Main, Nemecko
8. REGISTRAČNÉ ČÍSLAEU/1/97/030/054
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIEDátum prvej registrácie: 21. február 1997
Dátum posledného predĺženia: 21. február 2007
10 DÁTUM REVÍZIE TEXTUPodrobné informácie o tomto lieku sú dostupné na internetovej stránke Európskej agentúry pre lieky
http://www.ema.europa.eu.
1. NÁZOV LIEKU
Insuman Implantable 400 IU/ml injekčný roztok v injekčnej liekovke
2. KVALITATÍVNE A KVANTITATÍVNE ZLOŽENIE
Jeden ml obsahuje 400 IU ľudského inzulínu (zodpovedá 14 mg).
Jedna injekčná liekovka obsahuje 10 ml injekčného roztoku, čo zodpovedá 4000 IU inzulínu. Jedna IU (medzinárodná jednotka) zodpovedá 0,035 mg bezvodého ľudského inzulínu.
Insuman Implantable je neutrálny inzulínový roztok (bežný inzulín).
Ľudský inzulín sa vyrába rekombinantnou DNA technológiou v Escherichia coli.
Úplný zoznam pomocných látok, pozri časť 6.1.
3. LIEKOVÁ FORMA Roztok na infúziu (infúzia). Roztok je číry, bezfarebný.
4. KLINICKÉ ÚDAJE
4.1 Terapeutické indikácie
Insuman Implantable aplikovaný pumpou Medtronic MiniMed Implantable je indikovaný na liečbu dospelých s diabetom mellitus I. typu, ktorý nie je možné zvládnuť subkutánnou inzulínovou liečbou (vrátane pumpy), prejavujúci sa častou a nevysvetliteľnou hyper- a/ alebo hypoglykémiou.
4.2 Dávkovanie a spôsob podávania
Tento liek môže byť predpisovaný len v centrách certifikovaných firmou Medtronic, ktorých zamestnanci boli primerane vyškolení na používanie pumpy Medtronic MiniMed Implantable.
Na užívanie Insumanu Implantable by mal dohliadať lekár, ktorý má skúsenosti s intraperitoneálnou inzulínovou liečbou cukrovky.
Dávkovanie
Naplnenie pumpy by sa malo uskutočniť každých 40 až 45 dní. Čas medzi dvoma naplneniami pumpy nesmie presiahnuť 45 dní z dôvodu stability používaného inzulínu. Pacienti môžu na základe svojich inzulínových potrieb požadovať častejšie naplnenie pumpy.
Požadované hladiny glykémie a dávkovacia schéma inzulínu (dávky a ich časovanie) sa musia určiť a prispôsobiť individuálne tak, aby vyhovovali pacientovej diéte, jeho telesnej aktivite a životnému štýlu. Po implantácii pumpy je potrebné niekoľko nasledujúcich týždňov často upravovať dávky inzulínu pod prísnym lekárskym dohľadom.
Keďže pumpa nie je pripojená na glukomer, pacienti sú poučení, aby si minimálne štyrikrát denne merali hladinu cukru v krvi z dôvodov odhalenia potenciálnej poruchy pumpy, monitorovania glykemickej kontroly a určenia požadovaných dávok inzulínu.
Denné dávky a časovanie podávania
Nejestvujú žiadne pevné pravidlá pre dávkovaciu schému inzulínu. Časť dennej dávky inzulínu
(„bazálna dávka“) je nepretržite infundovaná implantovanou pumpou a zostávajúcu časť si podá
pacient sám, tou istou pumpou, ako bolus pred jedlami. Základná denná dávka je obyčajne 40% až
60% z celkovej dennej dávky inzulínu. Zmeny v bazálnej a bolusovej dávke sú riadené prostredníctvom malej príručnej jednotky (Personal Pump Communicator), ktorá s pumpou
komunikuje prostredníctvom rádiových vĺn. Podrobné inštrukcie o používaní implantovateľnej pumpy, jej funkciách a potrebné bezpečnostné opatrenia sú uvedené v Návode pre lekára.
Prechod na Insuman Implantable
Nastavenie dávkovacej schémy môže byť potrebné, ak pacient prechádza z jedného inzulínového preparátu na iný. Toto platí, ak sa napríklad mení :
· zvierací inzulín ( obzlvášť hovädzí inzulín) na ľudský inzulín,
· jeden ľudský inzulín na druhý,
· dávkovacia schéma s bežným inzulínom na dávkovaciu schému s dlhodobo pôsobiacim inzulínom
Potreba prispôsobiť (napr. znížiť) dávku môže nastať ihneď po prechode alebo sa môže vyvinúť postupne v priebehu niekoľkých týždňov.
V súvislosti so zmenou zo zvieracieho na ľudský inzulín, môže byť potrebné zníženie dávky predovšetkým u pacientov, ktorí:
· už sú liečení a majú relatívne nízke glykémie,
· majú tendenciu k hypoglykémii,
· predtým potrebovali vyššie dávky inzulínu kvôli prítomnosti inzulínových protilátok
Starostlivé sledovanie metabolizmu sa odporúča počas prechodu a aj niekoľko nasledovných týždňov po ňom. U pacientov, ktorí potrebujú vyššie dávky z dôvodu prítomnosti inzulínových protilátok, sa má zvážiť prechod pod lekárskym dohľadom v nemocnici alebo za podobných podmienok ako v nemocnici.
Druhotná úprava dávky
Zlepšenie metabolickej kontroly môže zvýšiť citlivosť na inzulín, čo sa odrazí v zníženej potrebe inzulínu. Prispôsobenie dávky môže byť tiež potrebné, napríklad ak:
- sa zmení hmotnosť pacienta,
- sa zmení životný štýl pacienta,
- sa objavia ďalšie okolnosti, ktoré môžu podporiť zvýšenú náchylnosť na hypo- alebo hyperglykémiu (pozri časť 4.4).
Osobitnéskupinypacientov
Starší pacienti (≧ 65 rokov)
U starších pacientov môže progresívna deteriorácia funkcie obličiek viesť k stálemu poklesu potreby inzulínu.
Poškodenie funkcie obličiek
U pacientov so zhoršenou funkciou obličiek sa môže dávka inzulínu znížiť na základe zníženého metabolizmu inzulínu.
Poškodenie funkcie pečene
U pacientov so závažne zhoršenou funkciou pečene sa môže znížiť potreba inzulínu na základe zníženej kapacity glukoneogenézy a zníženého metabolizmu inzulínu.
Pediatrickí pacienti (menej ako 18-roční)
K dispozícii nie sú žiadne údaje. Preto nebola bezpečnosť ani účinnosť Insumanu Implantable
(intraperitoneálne použitie) u pediatrických pacientov stanovená.Insuman Implantable je teda kontraindikovaný u pacientov, ktorí nedosiali veľkosť dospelého človeka (pozri časť 4.3 a 4.4).
Spôsobpodávania
Insuman Implantable sa smie použiť len intraperitoneálne. Ostatné spôsoby podávania (napr.injekčný)
sú kontraindikované.
Insuman Implantable bol vyvinutý len na intraperitoneálnu inzulínovú liečbu pumpou Medtronic MiniMed Implantable, dodávanou firmou Medtronic MiniMed (označenou známkou kvality CE), ktorá dodáva inzulín priamo do brušnej dutiny.
Insuman Implantable sa nesmie používať v iných pumpách (vonkajších ani implantovateľných) ako v pumpe Medtronic MiniMed Implantable alebo pomocou iných zdravotných pomôcok, vrátane ihiel (pozri časť 6.6).
Opätovné naplnenie pumpy
Opätovné naplnenie pumpy by malo byť vykonané za aseptických podmienok v centrách certifikovaných spoločnosťou Medtronic. Naplnenie rezervoára (zásobníka) smie vykonať len vyškolený a kvalifikovaný personál v súlade s pokynmi výrobcu pumpy. Pre prípravu pokožky je nutné dodržiavať štandardné sterilné operačné postupy, aby sa zabránilo mikrobiálnej kontaminácii a infekcii. Všetky roztoky, ktoré sú určené na použitie v pumpe, musia byť pred naplnením do rezervoára pumpy zbavené vzduchových bublín, aby sa zabránilo agregácii inzulínu a jeho
poddávkovaniu. Inzulínové injekčné liekovky majú byť vytiahnuté z chladničky minimálne 4 hodiny a nie dlhšie ako 24 hodín pred použitím a majú byť skladované pri izbovej teplote vo vonkajšom
obale, aby boli chránené pred svetlom. Inzulínový roztok musí byť potom zbavený plynu v súlade
s Návodom pre lekára.
Pri procedúre opätovného naplnenia sa musí zvyškový inzulín z pumpy odstrániť a pumpa naplniť novým inzulínom. Rezervoár je úplne naplnený (približne 15 ml alebo 6000 jednotiek Insumanu Implantable), nezávisle na potrebách pacientov. Zvyškový a nový inzulín sa musia zvážiť za účelom zaznamenania hodnôt opätovného naplnenia a vypočítania vhodného kritéria pre opätovné naplnenie. Pre ďalšie podrobnosti týkajúce sa zaobchádzania pozri časť 6.6 a inštrukcie poskytnuté v Návode pre lekárov.
Vyplachovanie pumpy
Všetky roztoky, ktoré sú určené na použitie v pumpe, musia byť pred naplnením do rezervoára pumpy zbavené vzduchových bublín, aby sa zabránilo agregácii inzulínu a jeho poddávkovaniu. Je potrebné
vykonať vyplachovaciu procedúru roztokom hydroxidu sodného 0.1 M, aby sa rozpustili zvyšky
inzulínu v rezervoári, čerpacom mechanizme a v bočnom výstupe katétra. Vyplachovanie pumpy sa odporúča každých 6 mesiacov.
Vyplachovanie sa môže uskutočniť skôr, ak sa napríklad počas napĺňania odhalí poddávkovanie
inzulínu alebo ak je podozrenie na nedostatočnú kontrolu glykémie. Je potrebné diagnostikovať, či problém nastal kvôli pumpe alebo kvôli katétru.
· Ak je poddávkovanie inzulínu spôsobené upchatím katétra, bočný výstup katétra sa môže prepláchnuť s 5 až 10 ml pufrovacieho roztoku.
· Ak je poddávkovanie spôsobené problémami s pumpou, má sa uskutočniť vyplachovacia procedúra.
Pre ďalšie podrobnosti o zaobchádzaní pozri časť 6.6 a inštrukcie uvedené v Návode pre lekárov.
Nálepku na inzulínovej liekovke je potrebné pred použitím skontrolovať a uistiť sa, že ide o správny inzulín na daný spôsob podávania.
Pacienti majú byť informovaní o vysokej koncentrácii inzulínu v Insumane Implantable (400 IU/ml)
v porovnaní s inými inzulínmi v injekčných liekovkách alebo náplniach (obyčajne 100 IU/ml).
Zámena inzulínu
Insuman Implantable sa nesmie zameniť s iným inzulínom ani s inzulínovými analógmi.
4.3 Kontraindikácie
Insuman Implantable
Precitlivenosť na inzulín alebo na ktorúkoľvek z pomocných látok uvedených v časti 6.1.
Iné spôsoby podania (napr. injekcia) sú kontraindikované.
Pumpa
Medtronic
MiniMed
Implantable
Precitlivenosť na titánovú zliatinu, polysulfónové a silikónové materiály použité v implantovaných častiach pumpy.
Použitie iných inzulínových liekov je v pumpe Medtronic MiniMed Implantable takisto
kontraindikované.
Pretože je pumpa veľká, je jej použitie u pediatrických pacientov, ktorí nedosiahli veľkosť dospelého človeka kontraindikované (pozri časť 4.2 a 4.4).
Pacientom, ktorí trvale žijú v nadmorskej výške nad 2439 metrov (8000 stôp), nesmie byť pumpa implantovaná (pozri časť 4.4).
4.4 Osobitné upozornenia a opatrenia pri používaníPumpa Medtronic MiniMed Implantable sa nemá implantovať pacientom, ktorým ich zdravotný a psychický stav nedovoľuje naprogramovať úpravy pumpy na základe odčítania hodnôt glukózy v krvi a urobiť potrebné úpravy v prípade problémov s pumpou.
Pacienti s implantovanou pumpou Medtronic MiniMed Implantable musia dostať obsiahle inštrukcie o používaní pumpy a o nevyhnutných opatreniach v prípade choroby, hypoglykémie a hyperglykémie alebo v prípade zlyhania pumpy. Pacient si má prečítať a riadiť sa pokynmi z priloženého Návodu pre pacienta. Pre ďalšie podrobnosti o zaobchádzaní pozri časť 6.6.
LekárskazobrazovaciatechnikaPumpa Medtronic MiniMed Implantable sa nemá implantovať pacientom, ktorí očakávajú, že budú potrebovať častú alebo rutinnú magnetickú rezonanciu (MRI) alebo terapeutický ultrazvuk.
PrecitlivenosťPacienti precitlivení na Insuman Implantable, pre ktorých nie je dostupný žiadny lepšie tolerovaný liek, musia v liečbe pokračovať pod prísnym lekárskym dohľadom a ak je to nevyhnutné, tak aj v spojení s antialergickou liečbou.
Pacientom s alergiou na zvierací inzulín sa odporúča, aby pred prechodom na liečbu Insumanom

Implantable podstúpili intradermálne kožné vyšetrenia, pretože sa u nich môžu prejaviť skrížené imunologické reakcie.V prípade nedostatočnej kontroly glukózy alebo pri tendencii k hyper- alebo
hypoglykemickým príhodám sa musí pred samotnou úpravou dávky posúdiť, či pacient dodržiava
predpísaný liečebný režim a všetky ostatné relevantné faktory.
HypoglykémiaHypoglykémia môže nastať, ak dávka inzulínu príliš prevyšuje jeho potrebu.
Počas obdobia 4 rokov hodnotenia pumpy Medtronic MiniMed Implantable nebolo pozorované žiadne klinicky významné predávkovanie inzulínu. Nie je však vylúčené, žeby sa tak nemohlo stať. V prípade ťažkej hypoglykémie musia pacienti okamžite kontaktovať svojho lekára vyškoleného
vykonať prehliadku pumpy. Pumpu je potom potrebné prehliadnuť z dôvodu možného upchatia katétra vedúceho k hromadeniu inzulínu a jeho následnému uvoľneniu (pozri časť 6.6).
Počas opätovného napĺňania pumpy môže byť veľmi malé množstvo inzulínu uložené podkožne, čo
môže spôsobiť hypoglykémiu. Pacientov je potrebné upozorniť, aby si starostlivejšie sledovali hladinu glukózy v krvi počas dní, kedy sa pumpa opätovne napĺňa.
Zvýšená opatrnosť a prísna kontrola glukózy v krvi sa odporúča u pacientov so zvýšeným rizikom hypoglykémie, ako sú pacienti so signifikantnou stenózou koronárnych artérií alebo krvných ciev zásobujúcich mozog (riziko srdcových alebo mozgových hypoglykemických komplikácií) rovnako ako pacientom s proliferatívnou retinopatiou, najmä ak sa neliečia fotokoaguláciou (riziko prechodnej amaurózy následkom hypoglykémie).
Pacienti majú byť informovaní o prípadoch, kedy varovné príznaky hypoglykémie slabnú. Varovné príznaky hypoglykémie sa môžu meniť, môžu byť menej výrazné alebo u určitých rizikových skupín môžu chýbať. Patria sem pacienti:
- u ktorých sa výrazne zlepšila kontrola glykémie,
- u ktorých hypoglykémia nastupuje postupne,
- starší pacienti,
- po prechode zo zvieracieho inzulínu na ľudský inzulín,
- s autonómnou neuropatiou v súčasnosti,
- s dlhodobou anamnézou cukrovky,
- trpiaci psychickým ochorením,
- dostávajúci sprievodnú liečbu niektorými inými liekmi (pozri časť 4.5).
Tieto situácie môžu vyústiť do závažnej hypoglykémie (aj s možnou stratou vedomia), skôr ako si to pacient uvedomí.
Ak sa zaznamenajú normálne alebo znížené hodnoty glykovaného hemoglobínu, musí sa brať do úvahy možnosť rekurentných,nerozpoznaných (najmä nočných) príhod hypoglykémie.
Ak pacient dodržiava predpísanú dávkovaciu schému a diétny režim, správne podávanie inzulínu a pozná symptómy hypoglykémie, znižuje tým výrazne riziko hypoglykémie. Náchylnosť na hypoglykémiu, vyžadujúcu dôkladné monitorovanie, prípadne nevyhnutnosť úpravy dávky, zvyšuje veľký počet faktorov. Patria sem:
- zvýšená citlivosť na inzulín (napr. po odstránení stresových faktorov),
- neobvyklá, zvýšená alebo dlhšie trvajúca fyzická aktivita,
- interkurentné ochorenie (napr. vracanie, hnačka),
- neprimeraný príjem potravy,
- vynechanie jedla,
- konzumácia alkoholu,
- určité nekompenzované poruchy endokrinného systému (napr. pri hypotyreóze a pri nedostatočnej činnosti adenohypofýzy alebo kôry nadobličiek),
- súbežné podávanie niektorých iných liekov.
Hyperglykémia
Je známe, že ak je inzulín vystavený chemickej alebo fyzickej záťaži (napr. zvýšenej teplote alebo traseniu), môže tvoriť zhluky, vlákna a gélovité štruktúry. To môže viesť k upchatiu pumpy a
poddávkovaniu inzulínu. V prípade poruchy pumpového systému sa hyperglykémia, ketoacidóza alebo
kóma môžu vyvinúť už v rámci niekoľkých hodín. Ak pacient spozoruje rýchly nárast glukózy v krvi, neadekvátny nárazovej dávke inzulínu, pumpu má čo najskôr prezrieť a preskúmať vyškolený lekár. Pacientovi sa má na úpravu pretrvávajúcej hyperglykémie subkutánne podať štandardná dávka inzulínu.
Poddávkovanieinzulínu
Nahromadené zvyšky inzulínu môžu spôsobiť upchatie pumpového mechanizmu a následne tak poddávkovanie inzulínu. Aby sa tomu zabránilo, odporúča sa každých šesť mesiacov tento
mechanizmus vypláchnuť. Vyplachovanie je možné urobiť aj skôr, napríklad vtedy, ak je poddávkovanie možné očakávať, ak je vypočítaná presnosť naplnenia menšia ako 85%. Potenciálne
poddávkovanie pumpou Medtronic MiniMed Implantable môže vyústiť do zvýšenia užívania denne naprogramovaného inzulínu, ťažko udržiavateľnej euglykémie, refraktérnej hyperglykémie a trvalému
poklesu presnosti napĺňania pumpy. Ako diagnostikovať možné problémy s pumpovým systémom,
ktoré môžu spôsobiť poddávkovanie inzulínu a ako napraviť a predísť poddávkovaniu je opísané v časti 6.6 (SPC) a Návode pre lekárov (implantovateľná pumpa).
Väčšine nežiaducich reakcií spájaných s používaním Medtronic MiniMed Implantable pumpy je možné predísť vyplachovaním pumpy vykonávaným lekárom. Aby sa rozpoznala poddávkovaním spôsobená hyperglykémia a ketoacidóza, a aby sa im predišlo, pacienti by si mali starostlivo, minimálne 4 krát denne, kontrolovať glukózu v krvi. Pacient má významnú úlohu v diagnostikovaní a nápravách hyperglykémie spôsobených problémami s fungovaním pumpy. Ak sa zmení fungovanie pumpy, pacient by mal byť schopný rozpoznať zmenu v hladinách cukru v krvi.
Pre prípad poruchy pumpy by mal pacient stále mať k dispozícii injekčnú striekačku alebo pero a inzulín vhodný na subkutánne podanie.
C
estovanie
Medtronic MiniMed Implantable pumpa nie je vyvinutá na používanie v nadmorských výškach vyšších ako 2439 metrov (8000 stôp) alebo nižších ako 7,6 metra (25 stôp). Používanie pumpy v týchto výškach môže vyústiť do predávkovania alebo poddávkovania inzulínu.
Pacientom, ktorí trvale sídlia v nadmorskej výške nad 2439 metrov (8000 stôp), nesmie byť pumpa implantovaná (pozri časť 4.3).
Pacientov, ktorí sa plánujú presťahovať alebo cestovať(inak ako komerčnými tlakovými lietadlami) do
výšok nad 2439 metrov (8000 stôp) alebo sa potápať do hĺbky väčšej ako 7,6 metra (25 stôp), je potrebné informovať zákrokoch, ktoré je potrebné vykonať. Rezervoár pumpy a bočný výstup katétra
sa musia vyprázdniť a pacienti si počas trvania cesty musia sami podávať subkutánny inzulín.
Lekár má poučiť pacienta o tom, čo robiť v prípade, že sa počas cestovania vyskytne porucha pumpy, o dostupnosti inzulínu a možnosti zámeny inzulínu a o tom, koho kontaktovať v prípade núdze. Pacientovi sa má poskytnúť alternatívny prostriedok náhrady inzulínu, napr. 100 IU/ml inzulín, zariadenia a spotrebný materiál na podkožnú injekciu.
Infekciapuzdrapumpy
Všetky postupy sa musia vykonávať za sterilných podmienok. Aby nedošlo k mikrobiálnej kontaminácii a infekcii, aseptická príprava implantačného miesta na pokožke má byť vykonaná v
súlade so štandardnými sterilnými operačnými postupmi danej inštitúcie. Antibiotické preventívne
opatrenia sú takisto potrebné pred implantáciou a aj po nej, aby sa znížilo riziko infekcie opuzdrenia pumpy. Ak sa tak neurobí, môže dôjsť k infekcii opuzdrenia (obalu) pumpy a jej následnému vyňatiu (pozri časť 4.8).
Eróziapokožky
Implantovateľná pumpa môže prestúpiť cez pokožku, čo môže viesť k infekcii miesta implantátu a k vyňatiu pumpy. Riziko erózie pokožky v mieste implantátu je možné znížiť výberom vhodného implantačného miesta, dodržiavaním správnej sterilnej implantačnej techniky počas implantovania a antibiotickou profylaxiou. Je takisto potrebné do vytvorenia opuzdrenia (cca 1 mesiac) nepretržite nosiť brušný pás.
Zléhojenie
Chirurgická rana sa môže po implantácii zle hojiť. Toto riziko je možné znížiť nepretržitým nosením brušného pása až do vytvorenia opuzdrenia (cca 1 mesiac) a obmedzením pacientových aktivít ihneď po implantovaní pomôcky.
Fokálnahepatickásteatóza
Po intraperitoneálnom podaní inzulínu bola pozorovaná fokálna hepatická steatóza, ak bol katéter umiestnený veľmi blízko pečeňového puzdra, alebo priamo v ňom. Zdá sa, že po zastavení inzulínovej infúzie, odstránení alebo premiestnení peritoneálneho katétra je fokálna hepatická steatóza
reverzibilná a bez klinických následkov.
Inzulínovéprotilátky
U pacientov, ktorí boli liečení pomocou pumpy Medtronic MiniMed Implantable, bola hlásená prítomnosť inzulínových protilátok. Intraperitoneálne podanie inzulínu pravdepodobne môže spôsobiť
tvorbu inzulínových protilátok. Prítomnosť týchto protilátok môže vyžadovať úpravu dávky inzulínu, aby sa znížil sklon k hyper- alebo hypoglykémii (pozri časť 4.8).
Interkurentnéochorenia
Interkurentné ochorenia si vyžadujú intenzívne sledovanie metabolizmu. V mnohých prípadoch je indikované vyšetrenie moču na ketóny a často je potrebné upraviť dávku inzulínu. Nároky na inzulín
sú často zvýšené. Pacienti s diabetom mellitus 1.typu musia pravidelne konzumovať aspoň malé'
množstvo sacharidov, dokonca aj keď sú schopní jesť len málo, alebo vôbec nie, alebo vracajú a pod. Inzulín sa nikdy nesmie úplne vynechať.
Omylypripoužitílieku
Boli hlásené omyly pri použití lieku, vrátane zámeny medzi subkutánnymi formami Insumanu alebo zámeny s inými subkutánnymi inzulínmi. Pred každým podaním je nutné vždy skontrolovať označenie na inzulíne, aby sa zabránilo zámene Insumanu Implantable za iné inzulíny.
Pediatrickápopulácia
Pretože je pumpa veľká, je jej použitie u pediatrických pacientov, ktorí nedosiahli veľkosť dospelého človeka kontraindikované (pozri časť 4.2 a 4.4).
4.5 Liekové a iné interakcie
Niektoré látky ovplyvňujú glukózový metabolizmus a to si môže vyžiadať úpravu dávky ľudského inzulínu.
Látky, ktoré môžu stupňovať účinok znižujúci hladinu glukózy v krvi a zvýšiť náchylnosť na hypoglykémiu sú perorálne antidiabetiká, inhibítory enzýmu konvertujúceho angiotenzín (ACE), dizopyramid, fibráty, fluoxetín, inhibítory monoaminooxidázy (MAO), pentoxifylín, propoxyfén, salicyláty a sulfónamidové antibiotiká.
Látky, ktoré môžu znižovať účinok znižujúci hladinu glukózy v krvi, sú kortikosteroidy, danazol, diazoxid, diuretiká, glukagón, izoniazid, estrogény a progestagény (napr. perorálna antikoncepcia), fenotiazínové deriváty, somatropín, sympatomimetiká (napríklad epinefrín [adrenalín], salbutamol, terbutalín), tyroidné hormóny, inhibítory proteázy a atypické antipsychotické lieky (napr. olanzapín a klozapín).
Betablokátory, klonidín, soli lítia alebo alkohol môžu buď zosilňovať alebo zoslabovať glykemický účinok inzulínu. Pentamidín môže spôsobiť hypoglykémiu, po ktorej môže niekedy nasledovať hyperglykémia.
Navyše príznaky adrenergnej protiregulácie sa môžu oslabiť alebo chýbať pod vplyvom sympatolytík ako sú betablokátory, klonidín, guanetidín a rezerpín.
4.6 Fertilita, gravidita a laktácia
Gravidita
Nie sú k dispozícii žiadne klinické údaje o gravidných ženách vystavených účinku ľudského inzulínu podaného subkutánne. Inzulín neprechádza placentárnou bariérou.
Pre Insuman Implantable podávaný inzulínovou pumpou v tehotenstve nebol stanovený bezpečnostný profil. Ženy vo fertilnom veku, ktoré majú pumpu buď implantovanú, alebo na jej implantáciu čakajú, by mali informovať svojho lekára, ak tehotenstvo zvažujú.
Pri predpisovaní tohto lieku tehotným ženám je potrebná opatrnosť. Insuman Implantable by nemal byť používaný počas gravidity, pokiaľ si klinický stav ženy nevyžaduje liečbu Insumanom Implantable.
Pre pacientky s preexistujúcim alebo gestačným diabetom je dôležité udržiavať dobrú kontrolu metabolizmu počas gravidity. Nároky na inzulín môžu klesnúť počas prvého trimestra a obvykle stúpajú počas druhého a tretieho trimestra. Bezprostredne po pôrode nároky na inzulín rapídne klesnú (zvýšené riziko hypoglykémie). Nevyhnutné je dôsledne monitorovať kontrolu glukózy.
Laktácia
Neočakávajú sa žiadne účinky na dojčatá. Insuman Implantable sa počas dojčenia môže podávať. Pre dojčiace ženy býva potrebná úprava inzulínovej dávky a diéty.
Fertilita
Nie sú k dispozícii žiadne klinické údaje a údaje zo štúdií na zvieratách týkajúce sa ovplyvnenia mužskej alebo ženskej fertility ľudským inzulínom.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť pacienta sústrediť sa a reagovať môže byť následkom hypoglykémie alebo hyperglykémie, či napríklad zhoršeného videnia, narušená. Môže tak vzniknúť určité riziko v situáciách, kedy sú tieto schopnosti zvlášť dôležité (napr. vedenie vozidiel alebo obsluha strojov).
Pacienti majú byť poučení, aby urobili opatrenia na zabránenie hypoglykémie počas vedenia vozidla, čo je dôležité najmä u tých, ktorí majú zníženú alebo chýbajúcu schopnosť vnímať varovné príznaky hypoglykémie alebo majú časté hypoglykemické príhody. Za týchto okolností sa musí zvážiť, či je vedenie vozidiel alebo obsluha strojov vhodná.
4.8 Nežiaduce účinkySúhrnbezpečnostnéhoprofiluHypoglykémia, vo všeobecnosti najčastejšia nežiaduca reakcia inzulínovej liečby, sa môže objaviť, ak je dávka inzulínu v porovnaní s požadovaným množstvom inzulínu príliš vysoká. Výskyt týchto
reakcií sa líši u jednotlivých skupín pacientov a dávkovacích režimov.
ZoznamnežiaducichreakciívtabuľkovomformátePočas 6 mesačnej porovnávacej štúdie, fáza III (HUBIN_L_05335) s Insumanom Implantable podaným prostredníctvom pumpy Medtronic MiniMed Implantable vykonanej v skupine 84 pacientov
vo veku 26 až 80 rokov (pozri časť 5.1) a počas klinického používania Insulinu Human 100 IU / ml a
40 IU / ml, boli pozorované nasledujúce nežiaduce reakcie.
Nasledujúce súvisiace nežiaduce reakcie z klinických štúdií sú uvedené nižšie a to v súlade s triedami orgánových systémov a v poradí klesajúceho výskytu: veľmi časté (≥1/10); časté (≥ 1/100 až < 1/10) ; menej časté (≥ 1/1000 až < 1/100); zriedkavé (≥ 1/10 000 až < 1/1000); veľmi zriedkavé (< 1/10 000), neznáme (z dostupných údajov).
V rámci každej skupiny frekvencie sú nežiaduce reakcie uvedené v poradí klesajúcej závažnosti. Tabuľka 1: Nežiaduce reakcie pozorované počas štúdie HUBIN_L_05335 s ľudským inzulínom
400 IU/ml a počas klinického používania ľudského inzulínu 100 IU/ml and 40 IU/ml.
Trieda orgánových
systémov podľa
MedDRA
| Časté
| Menej časté
| Neznáme
|
Poruchy imunitného systému
|
| Šok
| Okamžité alergické
reakcie (hypotenzia, angioneurotický edém,
bronchospazmus,
generalizované kožné reakcie);
Inzulínové protilátky
|
Poruchy metabolizmu a výživy
| Hyperglykémia;
Hypoglykémia; Hypoglykemický
záchvat;
Hypoglykemické bezvedomie;
ketóza
Edém
|
| Hypoglykémia;
Retencia sodíka
|
Poruchy nervového
systému
|
Hypoglykemická kóma
|
|
|
P
oruchy oka
|
|
|
Proliferatívna
retinopatia;
Diabetická retinopatia; Porucha zraku
|
P
oruchy kože
a podkožného tkaniva
|
|
|
Lipodystrofia
|
H
epatobiliárne
poruchy
|
|
|
Ložisková steatóza
pečene
|
(1) Nežiaduce reakcie pozorované pri
InsuplantePočas používania Medtronic MiniMed Implantable pumpy v 2 fáze III štúdie boli hlásené nasledujúce
súvisiace nežiaduce reakcie (pozri časť 5.1)
Tabuľka 2: Nežiaduce reakcie a sťažnosti na pomôcku (product technical complaints) pozorované v súvislosti s infúznym systémom (vrátane nežiaducich reakcií súvisiacich s implantáciou a/ alebo s údržbou pomôcky).
Trieda orgánových systémov podľa MedDRA
| Časté
|
Infekcie a nákazy
| Infekcia miesta implantátu (pozri časť 4.4)
|
Poruchy gastrointestinálneho traktu
| Bolesť brucha;
pupočná hernia
|
Poruchy kože a podkožného tkaniva
| Kožná erózia na mieste implantovania pumpy
(pozri časť4.4)
|
Celkové poruchy a reakcie v mieste podania
| Upchatie pomôcky;
Bolesť v mieste zavedenia katétra
|
Chirurgické a liečebné postupy
| Výmena zdravotnej pomôcky kvôli jej poruche;
Zablokovanie pomôcky
|
OpisvybranýchnežiaducichreakciíPoruchy imunitného systémuOkamžité alergické reakcie na inzulín alebo pomocné látky môžu byť život ohrozujúce.
Inzulínové protilátky: Obmedzené údaje z klinickej štúdie s intraperitoneálne podanie Insumanu Implantable nenaznačujú, že by zvýšené hladiny inzulínových protilátok mali byť spájané so syndrómom inzulínových protilátok alebo so závažnými nežiaducimi účinkami (pozri časť 4.4).
Poruchy metabolizmu a výživyZávažné hypoglykemické záchvaty, predovšetkým ak sa opakujú, môžu viesť k neurologickému poškodeniu.
Dlhotrvajúce alebo závažné hypoglykemické príhody môžu byť život ohrozujúce.
U veľkého počtu pacientov predchádzajú príznakom a symptómom neuroglykopénie známky adrenergnej protiregulácie. Vo všeobecnosti platí, že čím väčší a rýchlejší je pokles hladiny glukózy v krvi, tým výraznejší je fenomén protiregulácie a jeho symptómov.
Inzulín môže spôsobovať retenciu sodíka a edém, predovšetkým ak sa slabá metabolická kontrola zvýšila zintezívnením inzulínovej liečby.
Poruchy okaVýrazná zmena kontroly glykémie môže spôsobovať dočasné zhoršenie zraku v dôsledku prechodnej zmeny v zdurení a indexe lomu šošoviek.
Dlhodobé zlepšenie kontroly glykémie znižuje riziko progresie diabetickej retinopatie. Avšak zintezívnenie inzulínovej liečby s náhlym zlepšením kontroly glykémie môže byť spojené s
prechodným zhoršením diabetickej retinopatie
.
Hepatobiliárne poruchyFokálna steatóza pečene bola hlásená u niekoľkých pacientov liečených Insuplantom, ak bol katéter umiestnený v tesnej blízkosti pečene.
Keď je špička katétra umiestnená v obale pečene, je intraperitoneálne podávanie inzulínu spojené so zvýšeným rizikom fokálnej steatózy pečene (pozri časť 4.4).
Hláseniepodozrenínanežiaducereakcie
Hlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného
v
Prílohe V.4.9 PredávkovaniePríznakyPredávkovanie inzulínom môže spôsobiť závažnú a niekedy dlhotrvajúcu a životu nebezpečnú hypoglykémiu.
LiečbaMierne príhody hypoglykémie je zvyčajne možné liečiť perorálnym podávaním sacharidov.
V niektorých prípadoch sa vyžaduje úprava dávkovacej schémy lieku, stravovacích návykov alebo fyzickej aktivity.
Závažnejšie príhody sprevádzané kómou, záchvatom alebo neurologickým poškodením možno liečiť intramuskulárnym/subkutánnym podaním glukagónu alebo intravenóznym podaním koncentrovaného roztoku glukózy. Môže byť nevyhnutné udržiavať príjem sacharidov a pozorovať pacienta, pretože hypoglykémia sa po zdanlivom klinickom zotavení môže navrátiť.
Lekár musí naprogramovať špecifické obmedzenia pre bazálne a bolusové inzulínové dávkovanie. Tieto obmedzenia sú potrebné na zabezpečenie určitej kontroly nad schopnosťou pacientov naprogramovať si svoje inzulínové dávkovacie schémy, a aby sa zabránilo možnosti predávkovania. Okrem toho, ak by sa pacienti snažili dodať viac ako 2,5 násobok naprogramovanej maximálnej bolusovej dávky v rámci jednej hodiny, PPC ( Personal Pump Communicator) zobrazí varovnú správu: "maximálna hodinová dávka bola prekročená".
V prípade ťažkej hypoglykémie musí byť pumpa ošetrujúcim lekárom preskúmaná kvôli prípadným upchatiam katétra vedúcim k hromadeniu inzulínu a jeho následnému uvoľneniu (pozri časť 6.6).
Počas opätovného napĺňania pumpy môže byť veľmi malé množstvo inzulínu uložené podkožne, čo môže spôsobiť hypoglykémiu. Pacientov je potrebné upozorniť, aby si starostlivejšie sledovali hladinu glukózy v krvi počas dní, kedy sa pumpa opätovne napĺňa (pozri časť 6.6).
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Antidiabetiká, inzulíny a analógy na injekciu, rýchlopôsobiace, ATC
kód: A10AB01.
SpôsobúčinkuInzulín
- znižuje hladinu krvnej glukózy, podporuje anabolické účinky a tlmí katabolické deje,
- zvyšuje transport glukózy do buniek, ako aj tvorbu glykogénu v svaloch a pečeni a zlepšuje utilizáciu pyruvátu. Inhibuje glykogenolýzu a glukoneogenézu,
- zvyšuje lipogenézu v pečeni a tukovom tkanive a inhibuje lipolýzu,
- podporuje príjem aminokyselín do buniek a podporuje proteosyntézu,
- zvyšuje príjem draslíka do buniek.
Farmakodynamickéúčinky
Insuman Implantable je inzulín s rýchlym nástupom a krátkym trvaním účinku.
Klinickáúčinnosťabezpečnosť
Zaslepená, randomizovaná, 6 mesačná kontrolovaná klinická štúdia (HUBIN_L_05335) sa uskutočnila s cieľom vyhodnotiť klinickú účinnosť a bezpečnosť Insuman Implantable v porovnaní s Insuplantom podávaným pumpou Medtronic MiniMed Implantable 168 pacientom s diabetom mellitus 1. typu, predtým liečených Insuplantom. Pred prvou implantáciou pumpy dostávalo 72,4% týchto pacientov kontinuálnu subkutánnu infúziu inzulínu (CSII) a 17,8% pacientov dostávalo niekoľkokrát denne subkutánne injekcie. Dôvodom na začatie kontinuálnej intraperitoneálnej infúzie inzulínu (CIPII) bola krehká (brittle) diabetes u 62,7%, hypoglykémia u 29,2%, periférna inzulínová rezistencia u 5,0% a hypoglykémia a krehká diabetes u 3,1% pacientov. Na začiatku štúdie polovica pacientov prešla na Insuman Implantable, zatiaľ čo druhá polovica zostala na Insuplante. Primárnym cieľom bola zmena HbA1c oproti východiskovej hodnote a presnosť naplnenia pumpy po 4 napĺňacích cykloch (162 ± 21 dní).Kontrola glykémie Insumanom Implantable bola podobná ako pri Insuplante na základe hodnôt HbA1c (zmena oproti východiskovej hodnote podľa protokolu: -0,25 -0,12 oproti; [95% CI: -0,36;
0,11]). Okrem toho pacienti s diabetom mellitus 1.typu, ktorí dostávali kontinuálnu intraperitoneálnu infúziu Insumanu Implantable, mali stabilné glykémie (podľa protokolu: priemerné zníženie: -0,25 ±
0,67; [95% CI: -0,36; 0,11]), bez zvýšenia rizika ťažkej hypoglykémie v porovnaní s Insuplantom
(14,3% oproti 13,1%).Výsledky podávania Insumanu Implantable podávaného kontinuálnou intraperitoneálnou infúziou boli podobné ako pri Insuplante, o čom svedčí správnosť opätovného naplnenia počas 4 cyklov opätovného napĺňania (podľa protokolu bola priemerná odchýlka: -3,15 ±
1,34; [95% CI: -5,81; - 0,50]).
Iná 12 mesačná otvorená randomizovaná kontrolovaná štúdia (MIP 310) sa uskutočnila s cieľom posúdiť vplyv intraperitoneálneho podávania inzulínu v porovnaní s podaním subkutánneho inzulínu na glykémiu a výskyt závažnej hypoglykémie. Všetci pacienti dostali intraperitoneálny inzulín prvý raz a u všetkých zlyhal pokus zlepšiť ich HbA1c počas 3 mesačnej intenzívnej terapie buď s injekciami podávanými niekoľkokrát denne alebo kontinuálnou subkutánnou infúziou inzulínu. Priemerná hodnota HbA1c pri vstupe do štúdie bola 8,1%. Pacientom zaradeným do skupiny s kontinuálnou intraperitoneálnou inzulínovou infúziou bol podávaný Insuplant 400 IU / ml po dobu
180 dní s následnou aplikáciou Insumanu Implantable 400 IU / ml po dobu ďalších 180 dní. Výsledky intraperitoneálneho podávania inzulínu boli podobné výsledkom subkutánneho podávania, o čom svedčí zmena HbA1c oproti východiskovej hodnote (pre kontinuálne intraperitoneálne podanie: HbA1c hodnota v deň 360 bola 7,78 ± 1,04 oproti 8,06 ± 0,77 na začiatku liečby, pri subkutánnom podávaní: HbA1c hodnota v deň 360 bola 8,19 ± 0,87 oproti 8,12 ± 0,76 na začiatku liečby).
5.2 Farmakokinetické vlastnosti
Farmakokinetické vlastnosti inzulínu sú v literatúre zvyčajne popísané tak, aby boli reprodukovateľné u pacientov s diabetes mellitus 1. typu , ktorým je podávaná krátkodobá alebo dlhodobá kontinuálna intraperitoneálna infúzia inzulínu.
Kontinuálna intraperitoneálna inzulínová infúzia spôsobuje u pacientov s diabetes 1. typu a diabetes mellitus 2. typu skoršie, kratšie a vyššie vrcholy voľného inzulínu v plazme ako kontinuálna
subkutánna infúzia inzulínu.
Kontinuálna intraperitoneálna a subkutánna infúzia (kombinované údaje) mala u pacientov s diabetes mellitus 1.typu za následok vyššie Cmax hodnoty voľného plazmatického inzulínu ako viacnásobné
každodenné podkožné injekcie a kontinuálna subkutánna infúzia inzulínu pomocou externej pumpy
(kombinované údaje).
Všetky nálezy naznačujú, že kontinuálna intraperitoneálna inzulínová infúzia u pacientov s diabetes mellitus 1. typu je viac podobná farmakokinetike endogénneho inzulínu ako kontinuálna subkutánna
inzulínová infúzia a viacnásobná denná aplikácia injekcií.
Neočakáva sa, žiadny vplyv jedla na Cmax, Tmax a AUC po CIPII podaní.
V štúdii fázy III (HUBIN_L_05335) u pacientov s diabetes mellitus 1. typu,bol hodnotený farmakokinetický profil Insumanu Implantable po intraperitoneálnom podaní bolusu inzulínu u 10 pacientov.
Vstrebávanie
Po intraperitoneálnom podaní Insumanu Implantable 0,15 IU / kg, medián Tmax 0,54 hodiny a Cmax v sére 210 ± 129 μIU / ml.
Priemerný farmakokinetický profil je znázornený na obrázku 1.
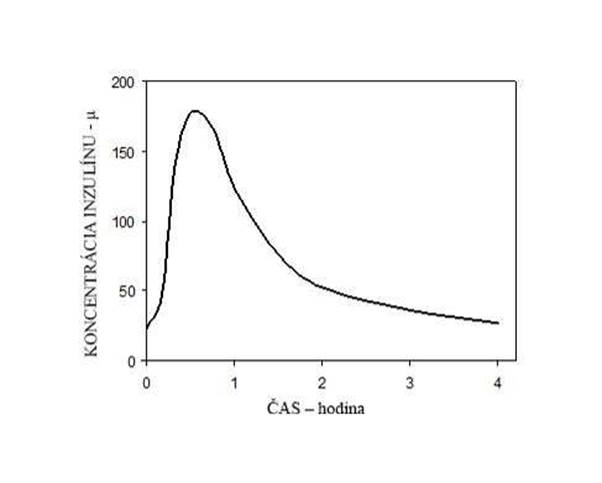
Obrázok 1: Priemerný farmakokinetický profil sérového inzulínu u pacientov s diabetes mellitus 1. typu po dávke 0,15 IU /kg Insumanu Implantable.
Eliminácia
Po intraperitoneálnom podaní 0,15 IU / kg Insuman Implantable, bol polčas eliminácie inzulínu zo séra 2,7 hodiny.
5.3 Predklinické údaje o bezpečnostiAkútna toxicita humánneho inzulínu sa sledovala u potkanov po subkutánnom podaní.Žiadne toxické účinky neboli dokázané.
Nebolo vykonané žiadne neklinické hodnotenie potenciálnej toxicity Insumanu Implantable 400 IU / ml podávaného intraperitoneálne. Uskutočnili sa však tri štúdie na laboratórnych potkanoch s cieľom zhodnotiť potenciálnu toxicitu intraperitoneálne podávaného ľudského inzulínu. V štúdii s
jednorazovým podaním u potkanov bol intraperitoneálne podaný polosyntetický ľudský inzulín s rovnakým zložením a pomocnými látkami ako má Insuman Implantable 400 IU / ml. Neboli
pozorované žiadne klinické príznaky, makroskopicky viditeľné zmeny alebo podráždenie v brušnej dutine. V inej štúdii bol krysám intraperitoneálnou infúziou pomocou implantovanej osmotickej minipumpy podaný rovnaký polosyntetický inzulínpo dobu až 6 týždňov.Steatóza pečene nebola
pozorovaná. V tretej štúdii, kde sa diabetickým potkanom podával pomocou katétra zavedeného do
obalu pečene iný ľudský inzulín zložením podobný Insumanu sa ukázalo, že intraperitoneálne podávanie vysokej lokálnej koncentrácie inzulínu v obale pečene môže vyvolať reverzibilnú fokálnu (ložiskovú) steatózu pečene.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
fenol,
chlorid zinočnatý, trometamol,
poloxamér 171,
glycerol,
kyselina chlorovodíková (na úpravu pH), hydroxid sodný (na úpravu pH),
voda na injekciu.
6.2 Inkompatibility
Tento liek sa nesmie zamieňať s inými liekmi. Miešanieinzulínov
Insuman Implantable sa nesmie miešať s inými inzulínmi ani s inzulínovými analógmi.
Treba zabezpečiť, aby sa do roztoku inzulínu nedostal žiadny alkohol, ani iné dezinfekčné látky.
6.3 Čas použiteľnosti
2 roky.
Čas použiteľnosti v pumpe
Čas použiteľnosti lieku v rezervoári implantovateľnej inzulínovej pumpy je 45 dní pri teplote 37°C.
6.4 Špeciálne upozornenia na uchovávanie
Neotvorenéinjekčnéliekovky Uchovávajte v chladničke (2°C - 8°C). Neuchovávajte v mrazničke.
Nedávajte Insuman Implantable blízko mraziacej časti ani zmrazeného balenia. Uchovávajte injekčnú liekovku vo vonkajšej škatuľkena ochranu pred svetlom.
Otvorenéinjekčnéliekovky
Čas použiteľnosti používaného lieku, pozri časť 6.3.
6.5 Druh obalu a obsah balenia
10 ml roztoku v injekčnej liekovke (bezfarebné sklo typu I) uzatvorenej tesniacim krytom (hliník), zátkou (chlorobutylová guma (typ I)) .Dostupné sú balenia po 1 a 5 injekčných liekovkách.
Nie všetky veľkosti balenia musia byť uvedené na trh.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Insuman Implantable sa musí použiť len ak je roztok číry, bezfarebný alebo takmer bezfarebný a prakticky bez viditeľných tuhých častíc.
Pred každým podaním je nutné vždy skontrolovať označenie na inzulíne, aby sa zabránilo zámene ľudského inzulínu za iné inzulíny (pozri časť 4.4).
Insuman Implantable sa nesmie používať v inej pumpe ako v Medtronic MiniMed Implantable a ani v inej zdravotnej pomôcke, vrátane ihiel (pozri časť 4.2).
Všetky postupy sa musia vykonávať za sterilných podmienok. Aby nedošlo k mikrobiálnej kontaminácii a infekcii, aseptická príprava implantačného miesta na pokožke má byť vykonaná v súlade so štandardnými sterilnými operačnými postupmi.danej inštitúcie. Antibiotické preventívne opatrenia sú takisto potrebné pred implantáciou a aj po nej, aby sa znížilo riziko infekcie vrecka pumpy. Ak sa tak neurobí, môže dôjsť k infekcii opuzdrenia pumpy a jej následnému vyňatiu (pozri časť 4.4).
Všetky roztoky, ktoré sú určené na použitie v pumpe, musia byť pred naplnením do rezervoára pumpy zbavené vzduchových bublín, aby sa zabránilo agregácii inzulínu a jeho poddávkovaniu. Inzulínové injekčné liekovky majú byť vytiahnuté z chladničky minimálne 4 hodiny a nie dlhšie ako 24 hodín pred použitím a majú sa skladovať pri izbovej teplote vo vonkajšom obale, aby boli chránené pred svetlom. Inzulínový roztok musí byť potom zbavený plynu v súlade s Návodom pre lekára. Ak sa všetky tekutinyvzduchových bublín nezbavia, môžu sa zaviesť, čo spôsobí agregáciu inzulínu a jeho následné poddávkovanie.
Opätovnénaplneniepumpy
V rezervoári pumpy sa uchováva okolo 6000 jednotiek inzulínu a opätovné naplnenie pumpy sa vyžaduje buď každých 40 až 45 dní z dôvodu stability v pumpe používaného inzulínu, alebo skôr
v závislosti od potrieb pacientov.
Táto procedúra sa vždy vopred naplánuje pacientom na základe nasledovných správ Osobného komunikátora pumpy (PPC) : „nízka hladina v rezervoári“ alebo „prázdny rezervoár“.
Na naplnenie sterilného rezervoáru pumpy sa môže použiť len Insuman Implantable, špeciálne vyvinutý na použitie v pumpe Medtronic MiniMed Implantovatable. Na úplné naplnenie a na vytesnenie vzduchu z rezervoára pumpy sú potrebné dve injekčné liekovky Insumanu Implantable (2 x
10 ml). Nepoužitý inzulín sa musí zlikvidovať v súlade s národnými požiadavkami a nesmie sa znovu použiť.
Na opätovné naplnenie rezervoára pumpy sa smie použiť iba napĺňacia súprava označená známkou kvality CE (striekačka a kohútik), ihly, sterilná šablóna na umiestnenie vývodu dodávaná firmou Medtronic MiniMed a sterilný pufrovací roztok vyrábaný firmou Sanofi-Aventis Deutschland GmbH
Počas opätovného napĺňania rezervoára nikdy netlačte na piest striekačky. Ak je napĺňacia ihla správne nasadená na ventil pumpy, potom vákuum v zásobníku pumpy pasívne nasaje inzulín z injekčnej striekačky. Ak sa inzulín do pumpy nepodarí natiahnuť, je možné, že zásobník pumpy je stále plný. Takisto je možné, že napĺňacia ihla nie je správne nasadená na ventil pumpy. Tlačenie
inzulínu za týchto okolností by mohlo spôsobiť nechcené zavedenie inzulínu do podkožného tkaniva v okolí ventilu pumpy.
Počas opätovného napĺňania pumpy môže byť veľmi malé množstvo inzulínu uložené podkožne, čo môže spôsobiť hypoglykémiu. Pacientov je potrebné upozorniť, aby si starostlivejšie sledovali hladinu
glukózy v krvi počas dní, kedy sa pumpa opätovne napĺňa.
Je dôležité vypĺňať počas opätovného napĺňania pracovné záznamy a vypočítať presnosť napĺňania, aby bolo možné vyhodnotiť funkčnosť systému. Ak je vypočítaná presnosť menšia ako 85%, ide pravdepodobne o poddávkovanie inzulínu.
Podrobné informácie o opätovnom napĺňaní nájdete v priloženom Návode pre lekára. Poddávkonieinzulínu
Je pravdepodobné, že ide o poddávkovanie inzulínu, ak :
· Pacient hlási zvýšenie dávkovania inzulínu na udržanie euglykémie. Túto skutočnosť je možné overiť pri každej návšteve pacienta kontrolou denných záznamov na PPC.
· Je prítomná refraktérna hyperglykémia.
· Ak je vypočítaná presnosť napĺňania menšia ako 85%.
Ak sa počas opätovného napĺňania poddávkovanie inzulínu odhalí, alebo sa pokladá za možné vzhľadom na nedostatočnú kontrolu glykémie, je potrebné diagnostikovať, či je problém spôsobený poruchou pumpy (napr. zablokovanie pumpy/spätný tok) alebo katétra (t.j. oklúzia katétra). Meraním výtlakový objemu sa testuje funkčnosť pumpy a priechodnosť katétra jeho preplachovaním. Pri výtlakovom objeme 0,42 - 0,58 μl bez spätného toku ide pravdepodobne o oklúziu katétra. Hodnota výtlakového objemu mimo tohto rozpätia alebo prítomnosť spätného toku sú indikátormi porúch pumpy.
Poddávkovanie inzulínu v spôsobené oklúziou katétra
K poddávkovaniu spôsobenému oklúziou bočného výstupu katétra môže dôjsť buď náhle, alebo postupne. Užívanie inzulínu a klinické príznaky môžu byť rovnaké ako pri poddávkovaní inzulínom. Okrem toho, môže tvorba biofilmu v hrote bočnému výstupu katétra vyvolať latentnú hypoglykémiu
a to tak, že inzulín sa v priebehu času navrství v podobe biofilmu a uvoľní sa, hneď ako sa ho nazbiera dostatočné množstvo. Na odstránenie oklúzie sa musí katéter vypláchnuť.
Katéter sa preplachuje 5-10 ml pufrovacieho roztoku.
Na vypláchnutie katétra sa smie použiť iba napĺňacia súprava označená známkou kvality CE (striekačka a kohútik), ihly, sterilná šablóna na umiestnenie vývodu, dodávaná firmou Medtronic MiniMed a sterilný pufrovací roztok, vyrábaný firmou Sanofi-Aventis Deutschland GmbH.
Vypláchnutie katétra sa má vykonať iba ak sa potvrdí nameranie výtlakového objemu. Ak sa tak neurobí, môže dôjsť k trvalému poškodeniu pumpy.
Počas vyplachovania sa do katétra manuálne vstrekne 13 jednotiek inzulínu. Pacient musí byť starostlivo sledovaný pre prípad, hypoglykémie a nutnosti intravenózneho podania glukózy alebo glykogénu.
Po vypláchnutí a opätovnom naplnení z pumpy inzulínom ostane asi 13 jednotiek tlmiaceho roztoku v distálnej časti bočnému výstupu katétra. V závislosti od glykemických hodnôt pacienta, sa musí bolusová dávka inzulínu naprogramovať tak, aby sa pufrovací roztok z katétra odstránil. Pacientove glykemické hodnoty sa musia po vypláchnutí sledovať minimálne každých 15 minút. Pacient smie byť prepustený, až keď sú jeho glykemické hodnoty stabilné a v bezpečnom rozsahu.
Ak je vyplachovanie neúspešné, potom sa zvyčajne katéter vymení operačne za nový. Podrobné pokyny na vypláchnutie katétra sú uvedené v priloženom Návode pre lekára.
Poddávkovanie spôsobené poruchou pumpy
Vyplachovanie pumpy sa vykonáva za účelom zvrátenia tohto stavu.
Na rozpustenie usadenín inzulínu v zásobníku pumpy, v čerpacom mechanizme a bočnom výstupe katétra sa používa 0,1 M roztok hydroxidu sodného. Táto procedúra sa má vykonať každých 6 mesiacov alebo, ak je to nevyhnutné, aj skôr.
Na vypláchnutie pumpy sa smie použiť iba napĺňacia súprava označená známkou kvality CE, ihly, sterilná šablóna na umiestnenie vývodu, sterilný 0,1 M roztok hydroxidu sodného, dodávaný firmou Medtronic MiniMed a sterilný pufrovací roztok, vyrábaný firmou Sanofi-Aventis Deutschland GmbH.
V prípade, že vyplachovanie neobnoví zdvihový objem a presnú distribúciu inzulínu, je potrebné vykonať dlhšiu vyplachovaciu procedúru.
Až po úspešnom nameraní obnovenia zdvihového objemu môže byť vypláchnutý aj katéter a pumpa opätovne naplnená inzulínom.
Podrobné pokyny na vyplachovanie pumpy sú uvedené v priloženom Návode pre lekára.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Sanofi-Aventis Deutschland GmbH, D-65926 Frankfurt am Main, Nemecko
8. REGISTRAČNÉ ČÍSLAEU/1/97/030/202
EU/1/97/030/203
9. DÁTUM PRVEJ REGISTRÁCIE/ PREDĹŽENIA REGISTRÁCIE10 DÁTUM REVÍZIE TEXTUPodrobné informácie o tomto lieku sú dostupné na internetovej stránke Európskej agentúry pre lieky
http://www.ema.europa.eu.