
účinku lieku Insulin aspart Sanofi zachovaný bez ohľadu na miesto podávania injekcie. Trvanie účinku sa môže meniť podľa dávky, miesta podávania, prietoku krvi, teploty a úrovne fyzickej aktivity.
Vzhľadom na rýchlejší nástup účinku sa má inzulín-aspartát podávať tesne pred jedlom. Ak je to potrebné, môže sa inzulín-aspartát podať hneď po jedle.
Insulin aspart Sanofi 100 jednotiek/ml injekčný roztok v injekčnej liekovke
Kontinuálna subkutánna inzulínová infúzia (CSII)
Insulin aspart Sanofi sa môže použiť na CSII v inzulínovej pumpe vhodnej na inzulínovú infúziu. CSII
musí byť podaná do brušnej steny. Miesta, do ktorých sa podáva infúzia, sa majú meniť.
Keď sa Insulin aspart Sanofi používa v inzulínovej infúznej pumpe, nemá sa miešať so žiadnymi inými inzulínovými liekmi.
Pacienti používajúci CSII majú byť podrobne oboznámení s použitím inzulínovej pumpy a použitím správneho zásobníka a infúznej hadičky (pozri časť 6.6). Infúzna súprava (hadička a kanyla) sa musia meniť podľa pokynov uvedených v návode, ktoré sú súčasťou infúznej súpravy.
Pacienti, ktorí si podávajú Insulin aspart Sanofi pomocou CSII musia mať vždy k dispozícii alternatívny spôsob podávania inzulínu pre prípad poruchy systému pumpy.
Intravenózne použitie
Ak je to potrebné, môže Insulin aspart Sanofi podať intravenózne lekár alebo zdravotnícky pracovník. Na intravenózne použitie lieku Insulin aspart Sanofi 100 jednotiek/ml sa používajú infúzne systémy s
inzulín-aspartátom s koncentráciou od 0,05 jednotky/ml do 1,0 jednotky/ml v infúznych roztokoch
0,9% chloridu sodného alebo 5% glukózy, 40 mmol/l chloridu draselného, 0,45% chloridu sodného alebo 10% glukózy v polypropylénových infúznych vakoch a sú stabilné pri izbovej teplote 24 hodín. Aj keď sú stabilné po celý čas, bude sa spočiatku určité množstvo inzulínu absorbovať do materiálu infúzneho vaku. Počas inzulínovej infúzie je potrebné monitorovanie glukózy.
Miešanie dvoch typov inzulínu
Inzulín aspart Sanofi sa nemá miešať s inými inzulínovými liekmi, vrátane inzulínu NPH (Neutral
Protamine Hagedorn), pretože neboli vykonané príslušné štúdie compatibility.
Podávanie v injekčnej striekačke
Insulin aspart Sanofi v injekčnej liekovke je určený na používanie s inzulínovými injekčnými striekačkami so zodpovedajúcim rozsahom jednotiek (pozri časť 6.6).
Insulin aspart Sanofi 100 jednotiek/ml injekčný roztok v náplni
Insulin aspart Sanofi v náplniach je vhodný len na subkutánne injekcie pomocou opakovane
použiteľného pera. Ak je potrebné podanie injekčnou striekačkou, intravenóznou injekciou alebo infúznou pumpou, má sa použiť injekčná liekovka. Majú sa použiť iné lieky obsahujúce inzulín-
aspartát, ktoré to umožňujú. Insulin aspart Sanofi v náplniach je určený na používanie v týchto perách
(pozri časť 6.6):
- JuniorSTAR poskytuje 1-30 jednotiek inzulín-aspartátu dávka sa odčítava po 0,5 jednotky
- Tactipen poskytuje 1-60 jednotiek inzulín-aspartátu a dávka sa odčítava po 1 jednotke
- AllStar a AllStar PRO poskytujú 1-80 jednotiek inzulín-aspartátu a dávka sa odčítava po
1 jednotke.
I
nsulin aspart Sanofi 100 jednotiek/ml
i
njekčný
r
o
zt
o
k
v
naplnenom
i
njekčnom
pere
Insulin aspart Sanofi 100 jednotiek/ml v naplnenom injekčnom pere je vhodný len na subkutánne
injekcie. Ak je potrebné podanie injekčnou striekačkou, intravenóznou injekciou alebo infúznou pumpou, má sa použiť injekčná liekovka. Majú sa použiť iné lieky obsahujúce inzulín-aspartát, ktoré
to umožňujú. Insulin aspart Sanofi v naplnenom injekčnom pere poskytuje 1-80 jednotiek, odčítava sa
po 1 jednotke.
Pacienti si musia vizuálne overiť počet natiahnutých jednotiek na ukazovateli dávky na pere. Preto je potrebné, aby boli pacienti, ktorí si budú sami podávať injekcie, schopní odčítať dávku na ukazovateli dávky na pere. Pacientov, ktorí sú nevidomí alebo slabozrakí, je potrebné poučiť, aby vždy požiadali
o pomoc/spoluprácu inú osobu, ktorá má dobrý zrak a vie, ako zaobchádzať s inzulínovým perom.
Podrobný návod na používanie sa nachádza v písomnej informácii pre používateľa.
4.3 Kontraindikácie
Precitlivenosť na liečivo alebo na ktorúkoľvek z pomocných látok (pozri časť 6.1).
4.4 Osobitné upozornenia a opatrenia pri používaní
Sledovateľnosť
Aby sa zlepšila (do)sledovateľnosť biologického lieku, má sa zrozumiteľne zaznamenať názov a číslo
šarže podaného lieku.
Pacienti musia byť poučení o tom, aby miesto podania injekcie neustále menili, čím sa zníži riziko vzniku lipodystrofie a kožnej amyloidózy. Na miestach s týmito reakciami existuje potenciálne riziko oneskorenej absorpcie inzulínu a zhoršenej kontroly glykémie po podaní inzulínových injekcií.
V prípade náhlej zmeny miesta podania injekcie na nepostihnutú oblasť bol hlásený vznik hypoglykémie. Po zmene miesta podania injekcie sa odporúča monitorovanie hladiny glukózy v krvi a
je možné zvážiť úpravu dávky antidiabetík.
Hyperglykémia
Neprimerané dávky alebo prerušenie liečby môžu viesť, najmä pri diabetes mellitus 1. typu,
k hyperglykémii a diabetickej ketoacidóze. Zvyčajne sa prvé príznaky hyperglykémie objavujú postupne počas hodín alebo dní. Patrí k nim smäd, časté močenie, nevoľnosť, vracanie, ospalosť, suchá začervenaná koža, sucho v ústach, nechutenstvo, ako aj acetónový dych. Neliečené hyperglykemické stavy u pacientov s diabetes mellitus 1. typu v konečnom dôsledku vedú k vzniku diabetickej ketoacidózy, ktorá je potenciálne letálna.
Hypoglykémia
Vynechanie jedla alebo neplánované, namáhavé fyzické vypätie môže viesť k hypoglykémii.
Najmä u detí treba dbať na to, aby dávky inzulínu (zvlášť v režime bazál-bolus) zodpovedali príjmu
potravy, fyzickým aktivitám a aktuálnej glykémii, aby sa minimalizovalo riziko hypoglykémie.
Hypoglykémia môže nastať, ak je dávka inzulínu veľmi vysoká v porovnaní s potrebou inzulínu. V prípade hypoglykémie alebo podozrenia na hypoglykémiu, sa inzulín-aspartát nesmie podávať. Po stabilizácii krvnej glukózy pacienta sa má uvažovať o úprave dávky (pozri časti 4.8 a 4.9).
Pacienti, u ktorých nastalo významné zlepšenie kompenzácie diabetes mellitus, napr. po intenzifikovanej inzulínovej liečbe, môžu pocítiť zmenu obvyklých varovných príznakov hypoglykémie a majú byť o nich primerane poučení. Obvyklé varovné príznaky sa môžu stratiť u pacientov dlhodobo chorých na diabetes.
Dôsledkom farmakodynamiky inzulínových analógov s rýchlym nástupom účinku je, že ak sa vyskytne hypoglykémia, tak jej nástup po podaní injekcie je rýchlejší, v porovnaní s rozpustným ľudským inzulínom.
Pretože inzulín-aspartát sa má podávať bezprostredne pred jedlom, rýchly nástup účinku lieku sa má brať do úvahy u pacientov so sprievodnými ochoreniami alebo u liečby, kde sa predpokladá spomalenie absorpcie jedla.
Sprievodné ochorenia, najmä infekcie a horúčkovité stavy si obvykle vyžadujú zvýšenie dávky inzulínu. Sprievodné ochorenia obličiek, pečene, alebo ochorenia ovplyvňujúce nadobličky, podmozgovú alebo štítnu žľazu môžu vyžadovať zmeny v dávke inzulínu.
Keď pacienti prechádzajú z jedného typu inzulínového lieku na iný, môžu sa včasné varovné príznaky hypoglykémie zmeniť alebo prichádzať oneskorene, v porovnaní s predchádzajúcim inzulínom.
Prechod ziných inzulínovýchliekov
Prechod pacientov na iný typ alebo na inú značku inzulínu sa musí uskutočniť len za prísnej lekárskej
kontroly. Zmeny v sile, značke (výrobca), type, pôvode (zvierací, ľudský inzulín alebo analóg ľudského inzulínu) a/alebo v spôsobe jeho výroby (rekombinantná DNA oproti inzulínu zvieracieho
pôvodu) môžu vyžadovať zmenu dávky. Pacienti prechádzajúci na Insulin aspart Sanofi z iného typu
inzulínu môžu vyžadovať zvýšenie počtu injekčných podaní za deň alebo zmenu dávky oproti pôvodne
používaným inzulínovým liekom. Ak je potrebná úprava dávky, môže sa vykonať pri prvej dávke, alebo počas prvých niekoľkých týždňov alebo mesiacov.
Reakcie v mieste podávaniainjekcie
Rovnako ako pri liečbe inými inzulínmi, môžu sa objaviť reakcie v mieste podávania injekcie, ktoré sa
prejavia bolesťou, začervenaním, žihľavkou, zápalom, podliatinou, opuchom a svrbením. Neustále
striedanie miesta podávania v rámci danej oblasti znižuje riziko vzniku týchto reakcií. Reakcie zvyčajne vymiznú do niekoľkých dní až niekoľkých týždňov. V zriedkavých prípadoch si reakcie v mieste podávania môžu vyžiadať prerušenie liečby inzulín-aspartátom.
Kombinácia inzulín-aspartátu s pioglitazónom
Boli zaznamenané prípady srdcového zlyhania, keď sa užíval pioglitazón v kombinácii s inzulínom,
zvlášť u pacientov s rizikovými faktormi pre rozvoj kardiálneho zlyhania srdca. Na toto sa má pamätať, ak sa uvažuje o liečbe s kombináciou pioglitazónu a inzulín-aspartátu. Ak sa používa táto kombinácia, majú sa u pacientov sledovať príznaky a symptómy zlyhania srdca, zvýšenie telesnej hmotnosti a edémy. Užívanie pioglitazónu má byť ukončené, ak sa objaví akékoľvek zhoršenie kardiálnych symptómov.
Zamedzenie náhodným zámenám/medicínskym chybám
Pacient musí byť upozornený, aby vždy pred každým injekčným podaním skontroloval obal inzulínu,
aby sa zamedzilo náhodnej zámene lieku Insulin aspart Sanofi za iné inzulíny.
Protilátky proti inzulínu
Podávanie inzulínu môže spôsobiť tvorbu protilátok proti inzulínu. V zriedkavých prípadoch
prítomnosť takých protilátok proti inzulínu, môže vyžadovať úpravu dávky inzulínu, aby sa upravila náchylnosť k hyperglykémii alebo hypoglykémii.
Cestovanie
Pred cestou medzi rôznymi časovými pásmami sa má pacient poradiť s lekárom, pretože môže nastať
zmena v čase podávania inzulínu a príjmu jedla.
Sodík
Tento liek obsahuje menej ako 1 mmol (23 mg) sodíka v jednej dávke t.j. je v podstate „bez obsahu
sodíka“.
4.5 Liekové a iné interakcie
O mnohých druhoch liekov je známe, že ovplyvňujú glukózový metabolizmus.
Látky, ktoré môžu znižovať pacientovu potrebu inzulínu, sú nasledovné:
perorálne antidiabetiká, inhibítory monoaminooxidázy (IMAO), betablokátory, ACE inhibítory, salicyláty, anabolické steroidy a sulfónamidy.
Látky, ktoré môžu zvyšovať pacientovu potrebu inzulínu, sú nasledovné:
perorálne antikoncepčné prípravky, tiazidy, glukokortikoidy, tyroidálne hormóny, sympatomimetiká,
rastový hormón a danazol.
Betablokátory môžu maskovať príznaky hypoglykémie. Oktreotid/lanreotid môžu zvyšovať alebo znižovať potrebu inzulínu. Alkohol môže zosilňovať alebo redukovať hypoglykemický efekt inzulínu.
4.6 Fertilita, gravidita a laktácia
Gravidita
Insulin aspart Sanofi (inzulín-aspartát) sa môže používať počas gravidity. Údaje z dvoch
randomizovaných kontrolovaných klinických štúdií (322 a 27 gravidných žien) nepreukázali žiadne nežiaduce reakcie inzulín-aspartátu na graviditu alebo na zdravie plodu/novorodenca v porovnaní
s ľudským inzulínom (pozri časť 5.1).
Intenzívna kontrola glukózy v krvi a sledovanie gravidných žien s diabetom mellitus (1. typu, 2. typu alebo gestačný diabetes mellitus) sa odporúča počas gravidity a pri plánovaní gravidity. Potreba inzulínu v prvom trimestri obvykle poklesne a následne sa zvyšuje počas druhého a tretieho trimestra. Po pôrode sa potreba inzulínu rýchlo vracia na hodnoty pred graviditou.
Dojčenie
Nie sú žiadne obmedzenia na liečbu liekom Insulin aspart Sanofi počas dojčenia. Liečba dojčiacich
matiek inzulínom nepreukazuje žiadne riziko pre dojča. Predsa len, môže byť potrebné dávku lieku
Insulin aspart Sanofi upraviť.
Fertilita
Štúdie na zvieratách nepreukázali žiadne rozdiely medzi inzulín-aspartátom a ľudským inzulínom, čo
sa týka fertility (pozri časť 5.3).
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Schopnosť koncentrácie ako aj reakčná schopnosť u pacientov môže byť znížená v dôsledku hypoglykémie. Táto skutočnosť vytvára riziko v situáciách, ktoré si vyžadujú mimoriadnu pozornosť (napr. pri vedení vozidiel alebo pri obsluhe strojov).
Pacienti musia byť upozornení na vplyv hypoglykémie na vedenie vozidiel. Dôležité je to u tých
pacientov, ktorí si znížene, alebo nedostatočne uvedomujú varovné signály hypoglykémie, alebo majú
časté hypoglykémie. V týchto situáciách treba zvážiť vhodnosť vedenia vozidiel.
4.8 Nežiaduce účinkyPrehľad bezpečnostnéhoprofiluNežiaduce reakcie spozorované u pacientov používajúcich inzulín-aspartát sú spôsobené hlavne
farmakologickým účinkom inzulínu.
Hypoglykémia je najčastejšie pozorovaná nežiaduca reakcia. Frekvencia hypoglykémie sa mení s populáciou pacientov, dávkovacími schémami a úrovňou glykemickej kontroly (pozri časť 4.8 Opis vybraných nežiaducich reakcií).
Na začiatku liečby inzulínom sa môžu objaviť refrakčné poruchy, edémy a reakcie v mieste podávania injekcie (bolesť, začevenanie, žihľavka, zápal, podliatina, opuch, a svrbenie v mieste podávania). Tieto reakcie majú obvykle prechodný charakter. Náhle zlepšenie glykémie môže byť spojené s akútnou bolestivou neuropatiou, ktorá je zvyčajne reverzibilná. Intenzifikácia liečby inzulínom s prudkým zlepšením glykemickej kontroly môže byť spojená s prechodným zhoršením diabetickej retinopatie, kým dlhodobé zlepšenie kontroly glykémie znižuje riziko progresie diabetickej retinopatie.
Tabuľkový zoznam nežiaducichreakciíNežiaduce reakcie uvedené nižšie na základe údajov z klinickej štúdie, sú klasifikované podľa
MedDRA frekvencie a triedy orgánových systémov. Kategórie frekvencií sú definované podľa nasledovnej konvencie: veľmi časté (≥ 1/10); časté (≥ 1/100 až < 1/10); menej časté (≥ 1/1000 až
< 1/100); zriedkavé (≥ 1/10 000 až < 1/1 000); veľmi zriedkavé (< 1/10 000); neznáme (nemôžu byť
stanovené z dostupných údajov).
Triedy orgánových
systémov MedDRA
| Veľmi
časté
| Menej
časté
| Zriedkavé
| Veľmi
zriedkavé
| Nezná
me
|
Poruchy imunitného
systému
|
| žihľavka,
vyrážka, výsev
|
| anafylaktické
reakcie*
|
|
Poruchy metabolizmu a výživy
| hypoglykém ia*
|
|
|
|
|
Poruchy nervového systému
|
|
| periférna neuropatia
(bolestivá neuropatia)
|
|
|
Poruchy oka
|
| refrakčné poruchy, diabetická retinopatia
|
|
|
|
Poruchy kože a
podkožného tkaniva
|
| lipodystrofi
a*
|
|
| Kožná
amyloi dóza
|
Celkové poruchy a reakcie v mieste
podania
|
| reakcie v mieste
podania injekcie, edém
|
|
|
|
* pozri časť 4.8 Opis vybraných nežiaducich reakcií
Opisvybranýchnežiaducichreakcií
Anafylaktické reakcie
Výskyt generalizovaných hypersenzitívnych reakcií (zahŕňajúcich generalizovanú kožnú vyrážku, svrbenie, potenie, gastrointestinálne ťažkosti, angioneurotický edém, ťažkosti s dýchaním, palpitácie a pokles krvného tlaku) sú veľmi zriedkavé, ale môžu byť potenciálne život ohrozujúce.
HypoglykémiaHypoglykémia je najčastejšie pozorovaná nežiaduca reakcia. Môže sa objaviť vtedy, keď je dávka
inzulínu veľmi vysoká v porovnaní s potrebnou dávkou inzulínu. Závažná hypoglykémia môže viesť
k bezvedomiu a/alebo kŕčom, čoho výsledkom môže byť prechodné alebo trvalé poškodenie funkcií mozgu alebo až smrť. Príznaky hypoglykémie sa objavujú zvyčajne náhle. Môžu zahŕňať studený pot, studenú bledú pokožku, vyčerpanosť, nervozitu alebo triašku, úzkosť, nezvyčajnú únavu alebo slabosť, zmätenosť, problémy s koncentráciou, ospalosť, nadmerný hlad, zmeny videnia, bolesť hlavy, nauzeu,
a búšenie srdca.
V klinických štúdiách sa frekvencia hypoglykémie mení s populáciou pacientov, dávkovacími schémami a úrovňou glykemickej kontroly. Počas klinických štúdií celkové množstvo hypoglykémií nebolo rozdielne v porovnaní medzi pacientami liečenými inzulín-aspartátom a ľudským inzulínom.
PoruchykožeapodkožnéhotkanivaV mieste podania injekcie sa môže vyskytnúť lispodystrofia (vrátane lipohypertrofie, lipoatrofie)
a kožná amyliodóza, čím sa môže oneskoriť lokálna absorpcia inzulínu. Pravidelné striedanie miesta podania injekcie v danej oblasti môže pomôcť pri zmiernení týchto reakcií alebo môže týmto reakciám zabrániť (pozri časť 4.4).
Pediatrická populáciaNa základe údajov po uvedení na trh a údajov z klinických štúdií, frekvencia, typ a závažnosť

nežiaducich reakcií pozorovaných v pediatrickej populácii nenaznačujú žiadne rozdiely vo
všeobecných skúsenostiach v porovnaní s bežnou populáciou.
Ďalšie osobitné skupiny pacientovNa základe údajov získaných po uvedení na trh a z klinických štúdií, frekvencia, typ a závažnosť
nežiaducich reakcií pozorovaných u starších pacientov a pacientov s poškodením obličiek alebo pečene
nenaznačujú žiadne rozdiely vo všeobecných skúsenostiach v porovnaní s bežnou populáciou.
Hlásenie podozrení na nežiaduce reakcieHlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné

monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili
akékoľvek podozrenia na nežiaduce reakcie na národné centrum hlásenia uvedené v
Prílohe V.4.9 PredávkovanieŠpecifiká predávkovania inzulínom nie je možné definovať, hoci sa hypoglykémia môže vyvinúť cez nasledujúce štádiá, ak sú pacientovi podané veľmi vysoké dávky v porovnaní s potrebou:
• V prípade miernej hypoglykémie, je možné podať perorálne pacientovi glukózu alebo potravu obsahujúcu cukor. Preto sa odporúča, aby diabetik mal vždy pri sebe výrobky obsahujúce cukor.
• Pri závažnej hypoglykémii, ak je pacient v bezvedomí, môže mu byť podaný intramuskulárne alebo subkutánne glukagón (0,5 až 1 mg) osobou oboznámenou s podávaním injekcie, alebo glukóza, ktorú môžu podávať intravenózne lekári alebo iní zdravotnícki pracovníci. Ak pacient do 10 až 15 minút nezareagoval na glukagón, musí sa mu podať intravenózne glukóza. Po nadobudnutí vedomia sa odporúča podať pacientovi perorálne cukor, ako prevenciu proti recidíve.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: Lieky používané na liečbu diabetu. Inzulíny a analógy na injekciu,
rýchlo pôsobiace, ATC kód: A10AB05.
Insulin aspart Sanofi je biologicky podobný (biosimilárny) liek. Podrobné informácie sú k dispozícii na webovej stránke Európskej liekovej agentúry
http://www.ema.europa.eu.Mechanizmus účinkuafarmakodynamickéúčinkyÚčinok inzulín-aspartátu na znižovanie cukru v krvi je dôsledkom uľahčeného vychytávania glukózy
väzbou na inzulínové receptory vo svale a tukových bunkách a súčasne prebieha inhibícia produkcie glukózy v pečeni.
Pri sledovaní znižovania koncentrácie glukózy za prvé štyri hodiny po jedle má inzulín-aspartát rýchlejší nástup účinku v porovnaní s rozpustným ľudským inzulínom. Pri podkožnom podaní má inzulín-aspartát kratšiu dobu účinku ako rozpustný ľudský inzulín.

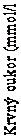
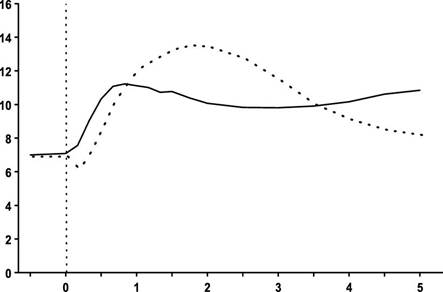
Čas (h)
Obr. I. Koncentrácia glukózy v krvi po jednorazovej dávke inzulín-aspartát podanej bezprostredne pred
jedlom (plná krivka) alebo po podaní rozpustného ľudského inzulínu podaného 30 minút pred jedlom
(čiarkovaná krivka) u pacienta s diabetes mellitus 1. typu.
Keď sa inzulín-aspartát podá podkožne, začiatok účinku je do 10 až 20 minút po podaní. Maximálny účinok sa dosiahne medzi 1. a 3. hodinou po podaní. Celkový čas trvania účinku je 3 až 5 hodín.
Klinická účinnosťKlinické skúšky u pacientov s diabetes mellitus 1. typu dokázali nižšie hodnoty postprandiálnej
glukózy v krvi po podaní inzulín-aspartátu v porovnaní s rozpustným ľudským inzulínom (obrázok 1.).
V dvoch dlhodobých otvorených štúdiách na pacientoch s cukrovkou 1. typu pozostávajúcich z 1070 a
884 pacientov, inzulín-aspartát znižoval glykovaný hemoglobín o 0,12 [95% C.I. 0,03; 0,22] percentných bodov a o 0,15 [95% C.I. 0,05; 0,26] percentných bodov v porovnaní s ľudským inzulínom: rozdiel má obmedzený klinický význam.
Klinické štúdie s inzulín-aspartátom u pacientov s diabetom 1. typu preukázali znížené riziko nočnej hypoglykémie v porovnaní s rozpustným ľudským inzulínom. Riziko dennej hypoglykémie sa výrazne nezvýšilo.
Inzulín-aspartát je ekvivalentný s rozpustným ľudským inzulínom v molárnom základe. Osobitnéskupinypacientov
Starší ľudia (vo veku ≥ 65 rokov)
Randomizovaná, dvojito zaslepená skrížená PK/PD štúdia porovnávajúca inzulín-aspartát s
rozpustným ľudským inzulínom, uskutočnená na starších pacientoch s cukrovkou 2. typu (19 pacientov vo veku 65–83 rokov, priemerný vek 70 rokov). Porovnateľné rozdiely vo farmakodynamických vlastnostiach (GIRmax,AUCGIR, 0-120 min) medzi inzulín-aspartátom a rozpustným ľudským inzulínom u starších pacientov boli podobné s tými, ktoré sa pozorovali u zdravých subjektov a u mladších pacientov s diabetom.
Pediatrická populácia
Klinická štúdia porovnávajúca preprandiálny rozpustný ľudský inzulín s postprandiálnym inzulín-
aspartátom bola vykonaná na malých deťoch (20 pacientov vo veku od 2 do menej ako 6 rokov, vykonávaná 12 týždňov, medzi ktorými boli štyria mladší ako 4-roční) a štúdia PK/PD jednotlivej
dávky bola vykonaná u detí (6–12 rokov) a mladistvých (13–17 rokov). Farmakodynamický profil
inzulín-aspartátu u detí bol podobný ako u dospelých.
Účinnosť a bezpečnosť inzulín-aspartátu, ktorý bol podávaný ako bolusový inzulín v kombinácii, buď s inzulínom detemirom, alebo s inzulínom degludekom, ako bazálnym inzulínom, bola sledovaná
v dvoch randomizovaných kontrolovaných klinických skúšaniach počas obdobia až do 12 mesiacov
u dospievajúcich a detí vo veku od 1 do menej ako 18 rokov (n=712). Skúšania zahŕňali 167 detí vo veku 1–5 rokov, 260 vo veku 6–11 a 285 vo veku 12–17. Pozorované zlepšenie HbA1c a bezpečnostné profily boli porovnateľné v rámci všetkých vekových skupín.
Gravidita
Klinická štúdia porovnávajúca bezpečnosť a účinnosť inzulín-aspartátu proti ľudskému inzulínu
v liečbe gravidných žien s diabetes mellitus 1. typu (322 gravidných žien (inzulín-aspartát: 157; ľudský
inzulín: 165)) nepreukázala žiadne nežiaduce reakcie na graviditu alebo na zdravie plodu/novorodenca.
Na doplnenie, údaje z klinickej štúdie zahŕňajúcej 27 žien s gestačným diabetes mellitus randomizovaných na liečbu s inzulín-aspartátom proti ľudskému inzulínu (inzulín-aspartát: 14; ľudský inzulín: 13) preukázali podobné bezpečnostné profily medzi liečbami.
5.2 Farmakokinetické vlastnosti
Absorpcia, distribúciaaeliminácia
V inzulín-aspartáte je aminokyselina prolín nahradená v polohe B 28 kyselinou asparágovou, čím sa
znižuje možnosť vytvárania hexamérov, ktoré boli pozorované u rozpustného ľudského inzulínu. Preto
sa inzulín-aspartát v porovnaní s rozpustným ľudským inzulínom rýchlejšie absorbuje z podkožnej
vrstvy.
Čas do získania maximálnej koncentrácie je v priemere polovičný ako pre rozpustný ľudský inzulín. Priemerná maximálna koncentrácia v plazme 492±256 mmol/l bola dosiahnutá za 40 (v rozmedzí
30 -40) minút po podkožnom podaní dávky 0,15 jednotky/kg telesnej hmotnosti, u pacientov s diabetes
mellitus 1. typu. Koncentrácie inzulínu sa vracajú k základnej línii za 4 až 6 hodín po podaní. Rýchlosť absorpcie bola o niečo nižšia u pacientov s diabetes mellitus 2. typu z čoho vyplýva nižšie Cmax (352 ±
240 pmol/l) a neskorší tmax /60 (v rozmedzí 50 – 90) minút. Variabilita v čase dosiahnutia maximálnej koncentrácie u jednotlivých osôb je významne nižšia pri inzulín-aspartáte ako pri rozpustnom ľudskom inzulíne, aj keď naopak variabilita v Cmax je pri inzulín-aspartáte vyššia.
O
s
obitné skupiny pacientov
Starší ľudia (vo veku ≥ 65 rokov)
Porovnateľné rozdiely vo farmakokinetických vlastnostiach medzi inzulín-aspartátom a rozpustným ľudským inzulínom u starších pacientov (65–83 rokov, priemerný vek 70 rokov) s diabetom 2. typu boli podobné, ako tie ktoré sa pozorovali u zdravých subjektov a mladších pacientov s diabetom. Znížená absorpčná rýchlosť sa spozorovala u starších pacientov, vyplývajúca z neskoršieho tmax
(82 (medzikvartilový intreval: 60–120) minút), zatiaľ čo Cmax bolo podobné ako to, ktoré sa
pozorovalo u mladších pacientov s diabetom 2. typu a nepatrne nižšie ako u pacientov s diabetom
1. typu.
Porucha funkcie pečene
Jednodávková farmakokinetická štúdia inzulín-aspartátu bola vykonaná u 24 subjektov s poruchou funkcie pečene v rozmedzí od normálnej po závažnú poruchu. U pacientov s poruchou funkcie pečene
bola absorpčná rýchlosť znížená a variabilnejšia, vyplývajúca zo spomaleného tmax z asi 50 minút
u subjektov s normálnou funkciou pečene po asi 85 minút u pacientov s miernou a vážnou poruchou funkcie pečene. AUC, C max a CL/F boli podobné u pacientov s poruchou funkcie pečene v porovnaní
so subjektami s normálnou funkciou pečene.
Porucha funkcie obličiek
Jednodávková farmakokinetická štúdia inzulín-aspartátu bola vykonaná u 18 subjektov s poruchou funkcie obličiek v rozmedzí od normálnej po závažne poškodenú. Žiadny zrejmý vplyv hodnôt
kreatinín klírensu na AUC, Cmax, CL/F a tmax inzulín-aspartátu nebol zistený. Dáta boli obmedzené u pacientov so strednou a závažnou poruchou funkcie obličiek. Pacienti so zlyhávaním obličiek
vyžadujúcim si liečbu dialýzou neboli skúmaní.
Pediatrická populácia
Farmakokinetické a farmakodynamické vlastnosti inzulín-aspartátu boli skúmané u detí (6 – 12 rokov)
a dospievajúcich (13 – 17 rokov) s diabetom 1. typu. Inzulín-aspartát bol rýchlo absorbovaný u oboch
vekových skupín s podobným tmax ako u dospelých. Avšak Cmax sa líšilo medzi vekovými skupinami s
dôrazom na význam individuálnej titrácie inzulín-aspartátu.
5.3 Predklinické údaje o bezpečnosti
Predklinické údaje získané na základe obvyklých farmakologických štúdií bezpečnosti, toxicity po opakovanom podaní, genotoxicity a reprodukčnej toxicity a vývinu nedokázali žiadne osobitné riziko pre ľudí.
V in vitro testoch, zahrňujúcich väzby na inzulínové a IGF-1 receptorové miesta a pri sledovaní vplyvu na rast buniek sa inzulín-aspartát správal podobne ako ľudský inzulín. Štúdie tiež dokázali, že disociácia väzieb medzi inzulínovými receptormi a inzulín-aspartátom je rovnaká ako u ľudského inzulínu.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Fenol Metakrezol Chlorid zinočnatý Polysorbát 20
Chlorid sodný
Kyselina chlorovodíková (na úpravu pH)
Hydroxid sodný (na úpravu pH) Voda na injekciu
6.2 Inkompatibility
Látky pridávané k lieku Insulin aspart Sanofi môžu zapríčiniť rozklad inzulín-aspartátu. InsulinaspartSanofi100jednotiek/ml injekčnýroztokvinjekčnejliekovke
Tento liek sa nesmie riediť alebo miešať s inými liekmi s výnimkou infúznych roztokov, ako je
uvedené v časti 4.2.
Insulin aspart Sanofi 100 jednotiek/ml injekčnýroztokvnáplniavnaplnenompere
Tento liek sa nesmie riediť ani miešať s inými liekmi.
Neodporúča sa miešať Insulin aspart Sanofi s NPH inzulínom, pretože neboli vykonané príslušné štúdie kompatibility.
6.3 Čas použiteľnosti
Pred prvým použitím
30 mesiacov.
Po prvompoužití
4 týždne.
6.4 Špeciálne upozornenia na uchovávanie
Insulin aspart Sanofi 100 jednotiek/ml injekčnýroztokvinjekčnejliekovke
Pred prvým použitím
Uchovávajte v chladničke (2°C - 8°C). Neuchovávajte v mrazničke.
Injekčnú liekovku uchovávajte vo vonkajšom obale na ochranu pred svetlom.
Po prvom použití
Uchovávajte pri teplote do 30°C. Neuchovávajte v chladničke. Neuchovávajte v mrazničke. Injekčnú liekovku uchovávajte vo vonkajšom obale na ochranu pred svetlom.
Insulin aspart Sanofi 100 jednotiek/ml injekčnýroztokvnáplni
Pred prvým použitím
Uchovávajte v chladničke (2°C – 8°C). Neuchovávajte v mrazničke. Uchovávajte náplň vo vonkajšom obale na ochranu pred svetlom.
Po prvom použití
Uchovávajte pri teplote do 30°C. Neuchovávajte v chladničke. Neuchovávajte v mrazničke. Po každej injekcii sa musí na pero opäť nasadiť vrchnák na ochranu pred svetlom.
Insulin aspart Sanofi 100 jednotiek/ml injekčnýroztokvnaplnenominjekčnom pere
Pred prvým použitím
Uchovávajte v chladničke (2°C – 8°C). Neuchovávajte v mrazničke.
Naplnené injekčné pero uchovávajte vo vonkajšom obale na ochranu pred svetlom.
Po prvom použití
Uchovávajte pri teplote do 30 °C. Neuchovávajte v chladničke. Neuchovávajte v mazničke. Po každej injekcii sa musí na pero opäť nasadiť vrchnák na ochranu pred svetlom.
6.5 Druh obalu a obsah balenia
I
nsulin aspart Sanofi 100 jednotiek/ml injekčnýroztokvinjekčnejliekovke
Bezfarebná sklenená viacdávková injekčná liekovka typu I s tesniacim krytom (hliník) s odlamovacím
viečkom (polypropylén) a laminátovým diskom (laminát z izoprénu a bromobutylovej gumy). Každá injekčná liekovka obsahuje 10 ml roztoku.
Veľkosť balenia: 1 alebo 5 injekčných liekoviek.
Na trh nemusia byť uvedené všetky veľkosti balenia.
Insulin aspart Sanofi 100 jednotiek/ml injekčnýroztokvnáplni
Bezfarebná sklenená náplň typu 1 so šedým piestom (bromobutylová guma) a tesniacim krytom
(hliník) so zátkou (izoprénový laminát a bromobutylová guma). Každá náplň obsahuje 3 ml roztoku. Veľkosť balenia: 5 alebo 10 náplní.
Na trh nemusia byť uvedené všetky veľkosti balenia.
Insulin aspart Sanofi 100 jednotiek/ml injekčnýroztokvnaplnenominjekčnom pere
Bezfarebná sklenená náplň typu 1 so šedým piestom (bromobutylová guma) a tesniacim krytom
(hliník) so zátkou (izoprénový laminát a bromobutylová guma) zaplombovaná do jednorazového injekčného pera (SoloStar).'
Každé naplnené injekčné pero obsahuje 3 ml roztoku. Veľkosti balenia: 1, 5 alebo 10 naplnených injekčných pier.
Na trh nemusia byť uvedené všetky veľkosti balenia.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekom
Pred použitím je potrebné roztok Insulin aspart Sanofi skontrolovať. Tento liek sa nesmie použiť, ak roztok nie je číry, bezfarebný a vodný.
Insulin aspart Sanofi, ktorý bol zmrazený, sa nesmie použiť.
Všetok nepoužitý liek alebo odpad vzniknutý z lieku sa má zlikvidovať v súlade s národnými požiadavkami.
Insulin aspart Sanofi 100 jednotiek/ml injekčnýroztokvinjekčnejliekovke
Aby sa zabránilo možnému prenosu choroby, injekčnú liekovku smie používať vždy len ten istý jeden
pacient a nikto iný, a to aj vtedy, ak by si vymenil ihlu.
Insulin aspart Sanofi v injekčnej liekovke možno používať v infúznych pumpách (CSII) tak, ako je uvedené v časti 4.2. Hadičky, v ktorých sú vnútorné povrchové materiály vyrobené z polyetylénu, boli posúdené ako kompatibilné na použitie v pumpách.
Insulin aspart Sanofi v injekčnej liekovke možno používať intravenózne, ako je opísané v časti 4.2. Na každú injekciu sa má vždy použiť nová ihla.
Injekčné striekačky a ihly nie sú súčasťou balenia.
Insulin aspart Sanofi 100 jednotiek/ml injekčnýroztokvnáplni
Aby sa zabránilo možnému prenosu choroby, každú náplň smie používať len jeden pacient, a to aj
vtedy, ak by si vymenil ihlu na injekčnom pere.
Insulin aspart Sanofi v náplniach sa majú používať s perami JuniorSTAR, Tactipen, AllStar alebo
AllStar PRO, ako sa odporúča (pozri časť 4.2 a 4.4).
Pero s vloženou náplňou sa nemá uchovávať s nasadenou ihlou. Pri každej injekcii sa má použiť nová ihla.
Pri každom pere je nutné dodržiavať pokyny výrobcu týkajúce sa vloženia náplne, upevnenia ihly a podania inzulínovej injekcie.
Insulin aspart Sanofi 100 jednotiek/ml injekčnýroztokvnaplnenominjekčnom pereAby sa zabránilo možnému prenosu choroby, každé pero smie používať len jeden pacient, a to aj
vtedy, ak by si vymenil ihlu.
Naplnené injekčné pero s vloženou náplňou sa nemá uchovávať s nasadenou ihlou. Pri každej injekcii sa má použiť nová ihla.
Ihly nie sú súčasťou balenia.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCIIsanofi-aventis groupe
54, rue La Boétie F - 75008 Paris Francúzsko
8. REGISTRAČNÉ ČÍSLAEU/1/20/1447/001
EU/1/20/1447/002
EU/1/20/1447/003
EU/1/20/1447/004
EU/1/20/1447/005
EU/1/20/1447/006
EU/1/20/1447/007
9. DÁTUM PRVEJ REGISTRÁCIE/PREDĹŽENIA REGISTRÁCIEDátum prvej registrácie: 25. jún 2020
10. DÁTUM REVÍZIE TEXTUPodrobné informácie o tomto lieku sú dostupné na internetovej stránke Európskej agentúry pre lieky
http://www.ema.europa.eu
Insulin aspart Sanofi injekčný roztok v naplnenom injekčnom pere (SoloStar)
NÁ
VO
D NA POUŹÍVANIE Najskôr si prečítajte toto Dôležité informácie
• Nezdieľajte pero s inou osobou – toto pero je určené len pre vás.
• Nikdy nepoužívajte pero, ak je poškodené alebo ak si nie ste istý, či funguje správne.
• Vždy urobte skúšku bezpečnosti.
• Pre prípad straty alebo poškodenia vždy noste so sebou náhradné pero aj náhradnú ihlu.
• Nikdy nepoužívajte ihly opakovane. Ak tak urobíte, mohli by ste si podať nižšiu dávku, ako potrebujete (poddávkovanie) alebo príliš vysokú dávku (predávkovanie), pretože ihla sa môže upchať.
Naučte sa podávať si injekciu
• O tom, ako si treba podávať injekciu, sa poraďte so svojím lekárom, lekárnikom alebo zdravotnou sestrou predtým, ako začnete pero používať.
• Ak máte problémy pri zaobchádzaní s perom, napríklad ak máte problémy so zrakom, požiadajte
o pomoc.
• Predtým, ako začnete používať pero, prečítajte si písomnú informáciu pre používateľa a návod na používanie pera. Ak nebudete postupovať podľa neho, môžete si podať príliš veľa alebo príliš málo inzulínu.
Potrebujete pomoc?
Ak máte akékoľvek ďalšie otázky týkajúce sa pera alebo cukrovky, opýtajte sa svojho lekára alebo lekárnika alebo zdravotnej sestry alebo zavolajte na telefónne číslo lokálneho zastúpenia spoločnosti sanofi-aventis, ktoré je uvedené na prednej strane tejto písomnej informácii.
Ďalšie veci, ktoré budete potrebovať:
• novú sterilnú ihlu (pozri KROK 2).
• odpadovú nádobu na použité ihly a perá zabezpečenú proti prepichnutiu (pozri Likvidácia pera).
Z
oznámte sa s perom
Držiak na náplne
Názov inzulínu Okienko zobrazujúce dávku
Ukazovateľ dávky
Vrchnák pera
Gumenné tesnenie
Stupnica inzulínu
Piest*
Volič dávky
Injekčné tlačidlo
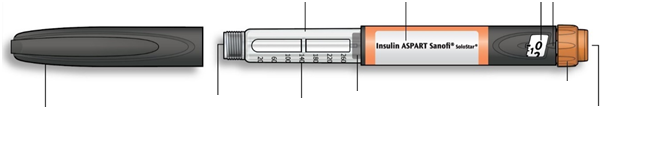
* Piest uvidíte až po podaní niekoľkých dávok.
K
RO
K 1: Skontrolujte si pero
• Vyberte nové pero z chladničky aspoň 1 hodinu pred podaním injekcie. Vpichnutie chladného inzulínu je bolestivejšie.
1A Skontrolujte si názov a dátum exspirácie na štítku vášho pera.• Presvedčte sa, či máte správny inzulín. Je to dôležité najmä vtedy, ak máte aj iné injekčné perá.
• Nikdy nepoužite pero po dátume exspirácie.
 1B Odstráňte vrchnák z pera.
1B Odstráňte vrchnák z pera. 1C Skontrolujte, či je inzulín číry.
1C Skontrolujte, či je inzulín číry.• Nepoužívajte pero, ak je inzulín zakalený, zafarbený alebo obsahuje častice.
STEP 2: Nasaďte novú ihlu• Na každú injekciu použite vždy novú sterilnú ihlu. Pomôže to predísť upchatiu ihly,
K
RO
K 3: Urobte skúšku bezpečnosti
• Pred každou injekciou urobte vždy skúšku bezpečnosti – jej účelom je:
• skontrolovať správne fungovanie pera a ihly.
• uistiť sa, že si podáte správnu dávku inzulínu.
3A Nastavte dávku 2 jednotky tak, že otočíte voličom dávky, aby ukazovateľ dávky bol na značke 2.3B Úplne zatlačte injekčné tlačidlo dovnútra.• Ak inzulín vystrekne cez hrot ihly, pero funguje správne.
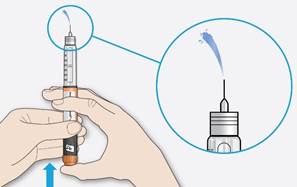 Ak inzulín nevystrekne:
Ak inzulín nevystrekne:• Možno budete musieť opakovať skúšku bezpečnosti až 3-krát, kým neuvidíte inzulín.
• Ak nevystrekne inzulín ani po treťom raze, ihla môže byť upchatá. Ak sa to stane:
- vymeňte ihlu (pozri KROK 6 a KROK 2),
- potom zopakujte skúšku bezpečnosti (KROK 3).
• Ak ani potom inzulín nevystrekne z hrotu ihly, toto pero už nepoužívajte. Použite nové pero.
• Nikdy nepoužívajte injekčnú striekačku a nenaťahujte do nej inzulín z pera.
 Ak spozorujete vzduchové bubliny
Ak spozorujete vzduchové bubliny• V inzulíne môžete spozorovať vzduchové bubliny. Je to normálne a nijako vám to neuškodí.
KROK 4: Nastavte si dávku• Nikdy nenastavujte dávku ani nestláčajte injekčné tlačidlo bez toho, aby ste mali na pere nasadenú ihlu. Mohli by ste pero poškodiť.
4A Presvedčte sa, či máte nasadenú ihlu a či je dávka nastavená na ‘0’.
 4B Otočte voličom dávky tak, aby bol ukazovateľ dávky v jednej rovine s tou dávkou, ktorú si chcete nastaviť.
4B Otočte voličom dávky tak, aby bol ukazovateľ dávky v jednej rovine s tou dávkou, ktorú si chcete nastaviť.
• Ak voličom otočíte viac, ako je dávka, ktorú si chcete nastaviť, môžete ním otočiť naspäť.
• Ak v pere nezostalo dosť jednotiek potrebných na vašu dávku, volič dávky sa zastaví na čísle s počtom dávok, ktoré zostali v pere.
• Ak si nemôžete nastaviť celú predpísanú dávku, použite nové pero alebo si podajte tú dávku, ktorá v pere zostáva a doplňte na úplnú dávku inzulínom z nového pera.
•
 Ako čítať okienko zobrazujúce dávku
Ako čítať okienko zobrazujúce dávkuPárne čísla sú zobrazené pri čiarke zarovno s ukazovateľom dávky:

nastavená dávka
20 jednotiek
Nepárne čísla sú zobrazené ako čiarka medzi jednotlivými párnymi číslami:

nastavená je dávka
21 jednotiek
Jednotky inzulínu v pere
• Pero obsahuje celkovo 300 jednotiek inzulínu. Môžete si nastaviť dávky od 1 do 80 jednotiek v krokoch po 1 jednotke. Každé pero obsahuje viac ako jednu dávku.
• To, koľko jednotiek inzulínu približne zostalo v pere, môžete vidieť podľa toho, kde sa na inzulínovej stupnici nachádza piest.
KROK 5: Podajte si injekciou dávku inzulínu• Ak ide ťažko zatlačiť injekčné tlačidlo, nepoužívajte na to silu, pretože môžete pero zlomiť.
Prečítajte si časť nižšie označenú ako
 5A Vyberte si miesto, do ktorého si podáte injekciu, ako je to zobrazené na obrázku
5A Vyberte si miesto, do ktorého si podáte injekciu, ako je to zobrazené na obrázku horná časť ramena
5B Zatlačte si ihlu do kože, ako vám to ukázal lekár, lekárnik alebo zdravotná sestra.
• Zatiaľ sa nedotýkajte injekčného tlačidla.

 5C Palec si dajte na injekčné tlačidlo. Potom zatlačte až nadoraz a držte.
5C Palec si dajte na injekčné tlačidlo. Potom zatlačte až nadoraz a držte.• Netlačte pod uhlom – palcom by ste mohli brániť otáčaniu voličom dávky.
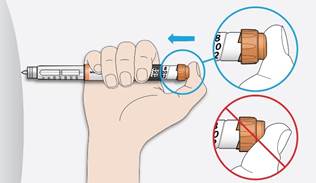 5D Nechajte injekčné tlačidlo zatlačené a keď uvidíte "0" v okienku zobrazujúcom dávku,
5D Nechajte injekčné tlačidlo zatlačené a keď uvidíte "0" v okienku zobrazujúcom dávku,
pomaly rátajte do 10.
• Týmto si zabezpečíte podanie celej dávky.
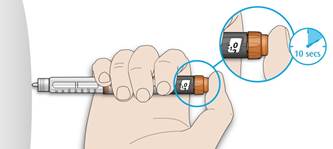 5E Keď dokončíte počítanie do 10, uvoľnite injekčné tlačidlo. Potom vytiahnite ihlu z kože.Ak ide ťažko zatlačiť injekčné tlačidlo:
5E Keď dokončíte počítanie do 10, uvoľnite injekčné tlačidlo. Potom vytiahnite ihlu z kože.Ak ide ťažko zatlačiť injekčné tlačidlo:• Vymeňte ihlu (pozri KROK 6 a KROK 2), potom urobte skúšku bezpečnosti (pozri KROK 3).
• Ak aj potom ide ťažko zatlačiť tlačidlo, vezmite si nové pero.
• Nikdy nepoužívajte injekčnú striekačku a nenaťahujte do nej inzulín z pera.
KROK 6: Odstráňte ihlu• S ihlami zaobchádzajte opatrne kvôli predchádzaniu poraneniam ihlami a prenosu infekcie.
• Nikdy nedávajte na ihlu naspäť vnútorný kryt.
6A Vonkajší kryt ihly nasaďte späť na ihlu a pomocou neho odskrutkujte ihlu z pera.
• Na zníženie rizika náhodného poranenia ihlou, nikdy nedávajte na ihlu naspäť vnútorný kryt.
• V prípade, že vám injekciu podáva iná osoba, alebo vy podávate injekciu inej osobe, vyžaduje sa špeciálna opatrnosť pri odstraňovaní ihly a jej likvidácii.
• Dodržiavajte odporúčané bezpečnostné pokyny pre odstraňovanie ihly a jej likvidácii (opýtajte sa svojho lekára, lekárnika alebo zdravotnej sestry), aby sa znížilo riziko náhodných poranení ihlou a prenosu infekčných ochorení.
6B Použitú ihlu odhoďte do odpadovej nádoby zabezpečenej proti prepichnutiu alebo juzlikvidujte tak, ako vám povedal lekárnik alebo v súlade s národnými požiadavkami.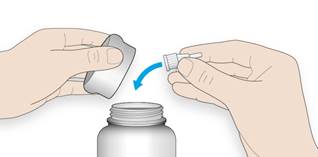
6C Na pero opäť nasaďte vrchnák.
• Nedávajte pero naspäť do chladničky.
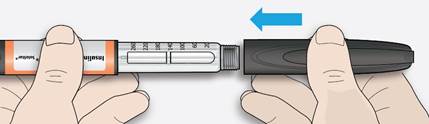 Ako uchovávať a ako sa treba o pero starať
Ako uchovávať a ako sa treba o pero starať• Pero môžete zvonka čistiť vlhkou handričkou (navlhčenou iba vo vode). Pero nenamáčajte, neumývajte ani nemastite, môže sa tým poškodiť.
• Odstráňte ihlu a použité pero zlikvidujte tak, ako vám povedal lekárnik alebo podľa požiadaviek štátneho úradu.
• Ďalšie informácie týkajúce sa uchovávania a používania pera sú uvedené v častiach 2 a 5
písomnej informácie pre používateľa.