u>Geriatrickí pacienti
Obmedzené údaje nenaznačujú potrebu úpravy dávkovania u starších pacientov (pozri časť 4.4)
Pacienti s poruchou funkcie pečeneU pacientov s poruchou funkcie pečene sa neuskutočnili žiadne formálne štúdie. Použitie Nebida je kontraindikované u pacientov s existujúcimi nádormi pečene alebo ich výskytom v minulosti (pozri časť 4.3).
Pacienti s poruchou funkcie obličiekU pacientov s poruchou funkcie obličiek sa neuskutočnili žiadne formálne štúdie.
Spôsob podávaniaNa intramuskulárne použitie.
Injekcie sa musia podávať veľmi pomaly (viac ako dve minúty). Nebido sa podáva výlučne intramuskulárne. Pri injekčnej aplikácii Nebida hlboko do gluteálneho svalu je potrebné postupovať opatrne a dodržiavať zvyčajné preventívne opatrenia týkajúce sa intramuskulárnej aplikácie. Obzvlášť treba dávať pozor, aby nedošlo k intravazálnej injekčnej aplikácii (pozri „Podávanie“ v časti 4.4). Obsah ampulky/liekovky treba podávať intramuskulárne ihneď po jej otvorení (pokyny na bezpečné otvorenie ampulky sú uvedené v časti 6.6).
4.3 Kontraindikácie
Použitie Nebida je kontraindikované u mužov s:
· androgén-dependentným karcinómom prostaty alebo mužskej prsnej žľazy,
· nádorom pečene (súčasným alebo prekonaným),
· precitlivenosťou na liečivo alebo ktorúkoľvek z pomocných látok uvedených v časti 6.1 .
U žien je použitie Nebida kontraindikované.
4.4 Osobitné upozornenia a opatrenia pri používaní
Nebido sa neodporúča používať u detí a dospievajúcich.
Nebido sa má používať iba po preukázaní hypogonadizmu (hyper- a hypogonadotropného typu) a ak bola pred začatím liečby vylúčená iná etiológia zodpovedná za príznaky. Nedostatočná hladina testosterónu sa musí zreteľne preukázať klinickými príznakmi (potlačenie sekundárnych pohlavných znakov, zmena kompozície tela, asténia, znížené libido, erektilná dysfunkcia a podobne) a musia ju potvrdiť dve samostatné merania hladiny testosterónu v krvi.
Skúsenosti s používaním Nebida u pacientov starších ako 65 rokov sú obmedzené. V súčasnosti neexistuje zhoda názorov ohľadom referenčných hodnôt hladiny testosterónu v krvi podľa veku. Treba však vziať do úvahy, že fyziologicky sa hladina testosterónu v sére so zvyšovaním veku znižuje.
Lekárske vyšetreniePred začiatkom liečby testosterónom musia všetci pacienti podstúpiť podrobné vyšetrenie, aby sa vylúčilo riziko preexistujúceho karcinómu prostaty. U pacientov liečených testosterónom treba dôkladne a pravidelne sledovať prostatu a prsníky v súlade s odporúčanými metódami (palpačné rektálne vyšetrenie a stanovenie hodnoty PSA v sére) aspoň raz ročne, u starších a rizikových pacientov (s klinickými alebo rodinnými faktormi) dvakrát ročne. Do úvahy sa majú vziať miestne odporúčania pre sledovanie bezpečnosti náhradnej liečby testosterónom.
Okrem laboratórnych testov koncentrácií testosterónu u pacientov dlhodobo liečených androgénmi treba pravidelne kontrolovať nasledujúce laboratórne parametre: hemoglobín, hematokrit a pečeňové testy (pozri časť 4.8).
Z dôvodu kolísania laboratórnych hodnôt treba všetky merania testosterónu vykonávať v rovnakom laboratóriu.
NádoryAndrogény môžu urýchľovať rozvoj subklinického karcinómu prostaty a benígnej hyperplázie prostaty.
Nebido treba používať opatrne u onkologických pacientov ohrozených hyperkalciémiou (a pridruženou hyperkalciúriou) z dôvodu metastáz v kostiach. U týchto pacientov sa odporúča vykonávať pravidelné sledovanie koncentrácií vápnika v sére.
U užívateľov hormonálnych liečiv typu androgénnych látok sa hlásili prípady benígnych a malígnych nádorov pečene. Ak sa u používateľov Nebida vyskytnú závažné ťažkosti v nadbruší, zväčšenie pečene alebo znaky vnútrobrušného krvácania, v diferenciálnej diagnóze sa má rátať s možnosťou nádoru pečene.
Ďalšie stavyU pacientov trpiacich závažnou insuficienciou srdca, pečene alebo obličiek alebo s ischemickou chorobou srdca môže liečba testosterónom spôsobiť vážne komplikácie charakterizované vznikom edému s možným kongestívnym zlyhaním srdca. V takomto prípade sa liečba musí okamžite zastaviť. U pacientov so zníženou funkciou obličiek alebo pečene sa doteraz nevykonali žiadne štúdie za účelom preukázania účinnosti a bezpečnosti tohto lieku. U týchto pacientov preto treba testosterónovú substitučnú liečbu používať obozretne.
U pacientov predisponovaných na edémy je potrebná opatrnosť, pretože liečba androgénmi môže zvýšiť retenciu sodíka (pozri časť 4.8).
Vo všeobecnosti platí, že u pacientov so získanou alebo dedičnou poruchou zrážania krvi treba vždy dodržiavať obmedzenia týkajúce sa používania intramuskulárnych injekcií.
Nebido treba používať opatrne u pacientov s epilepsiou a migrénou, pretože môže spôsobiť zhoršenie týchto stavov.
Nebido treba používať opatrne u pacientov s epilepsiou a migrénou, pretože môže spôsobiť zhoršenie týchto stavov.
U pacientov liečených androgénmi, u ktorých sa po substitučnej liečbe dosiahla normálna koncentrácia testosterónu v plazme, môže dôjsť k zlepšeniu citlivosti na inzulín.
Niektoré klinické príznaky, ako napríklad podráždenosť, nervozita, prírastok hmotnosti, dlhotrvajúce alebo časté erekcie, môžu signalizovať nadmernú dávku androgénu vyžadujúcu jej upravenie.
Môže dôjsť k zhoršeniu spánkového apnoe.
Športovcov podstupujúcich testosterónovú substitučnú liečbu pri primárnom alebo sekundárnom mužskom hypogonadizme treba upozorniť, že tento liek obsahuje liečivo, ktoré môže spôsobiť pozitívnu reakciu pri antidopingových testoch.
Androgény nie sú vhodné na zvyšovanie svalového rozvoja u zdravých jedincov ani na zvyšovanie fyzických schopností.
Ak príznaky nadmernej dávky androgénov pretrvávajú alebo ak sa znova objavia počas liečby odporúčanými dávkami, Nebido treba natrvalo vysadiť.
PodávanieTak ako všetky olejové roztoky, aj Nebido sa musí vpichovať prísne intramuskulárne a veľmi pomaly (viac ako dve minúty). Pulmonálna mikroembólia spojená s aplikáciou olejových roztokov môže v zriedkavých prípadoch viesť k znakom a príznakom, ako je kašeľ, dýchavičnosť, nevoľnosť, hyperhidróza, bolesť v hrudníku, závrat, parestézia alebo synkopa.Tieto reakcie sa môžu vyskytnúť počas aplikácie alebo ihneď po aplikácii a sú reverzibilné. Pacienta je preto potrebné počas injekcie a krátko po nej pozorovať s cieľom umožniť skoré rozpoznanie možných znakov a príznakov pulmonárnej mikroembólie spojenej s aplikáciou olejových roztokov. Liečba je zvyčajne podporná, napr. doplnkovým podaním kyslíka.
Po podaní Nebida sa hlásili suspektné anafylaktické reakcie.
4.5 Liekové a iné interakcie
Perorálne antikoagulanciáTestosterón a jeho deriváty podľa skúseností zvyšujú účinok perorálnych antikoagulancií. Pacienti užívajúci perorálne antikoagulanciá vyžadujú pozorné sledovanie, najmä na začiatku a konci liečby androgénmi. Odporúča sa častejšie sledovanie protrombínového času a určovanie medzinárodného normalizovaného pomeru (INR).
Iné interakcieSúbežné podávanie testosterónu s ACTH alebo kortikosteroidmi môže zvýšiť tvorbu edémov, a preto treba tieto liečivá podávať obozretne, najmä u pacientov s ochoreniami srdca a pečene alebo u pacientov s predispozíciou na vznik edému.
Interakcie, ktoré môžu ovplyvniť výsledky laboratórnych testov: Androgény môžu znižovať hladinu globulínu viažuceho tyroxín, čo následne spôsobuje zníženie celkovej hladiny T4 v sére a zvýšenú absorpciu T3 a T4 na živicu. Hladiny voľných hormónov štítnej žľazy však zostávajú nezmenené a neexistuje žiadny klinický dôkaz poruchy činnosti štítnej žľazy.
4.6 Fertilita, gravidita a laktácia
FertilitaSubstitučná liečba testosterónom môže reverzibilne redukovať spermatogenézu (pozri časti 4.8 a 5.3).
Gravidita a laktáciaNebido nie je určený pre ženy a nesmú ho používať tehotné alebo dojčiace ženy, pozri časť 4.3.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať stroje
Nebido nemá žiadny alebo má zanedbateľný vplyv na schopnosť viesť vozidlá a obsluhovať stroje.
4.8 Nežiaduce účinky
Ohľadom nežiaducich účinkov, spojených s užívaním androgénov, prosím pozri tiež časť 4.4.
Najčastejšie hlásenými nežiaducimi účinkami počas liečby Nebidom boli akné a bolesť v mieste vpichu.
Pulmonálna mikroembólia spojená s aplikáciou olejových roztokov môže v zriedkavých prípadoch viesť k znakom a príznakom, ako je kašeľ, dýchavičnosť, nevoľnosť, hyperhidróza, bolesť v hrudníku, závrat, parestézia alebo synkopa. Tieto reakcie sa môžu vyskytnúť počas aplikácie alebo ihneď po aplikácii a sú reverzibilné. Prípady podozrenia spoločnosti alebo hlásiaceho na pulmonálnu olejovú mikroembóliu boli ojedinele zaznamenané v klinických štúdiách (≥1/10 000 až <1/1 000 injekcií) rovnako ako aj v post-marketingovom sledovaní (pozri časť
4.4 Osobitné upozornenia a opatrenia pri používaní).
Po podaní Nebida boli hlásené suspektné anafylaktické reakcie.
Androgény môžu urýchliť progresiu subklinického karcinómu prostaty a benígnej hyperplázie prostaty.
V tabuľke 1 nižšie sa uvádzajú nežiaduce reakcie (ADRs) podľa tried orgánových systémov podľa MedDRA ( MedDRA SOCs). Frekvencie sú založené na údajoch z klinického skúšania a sú definované ako časté (³1/100 až <1/10) a menej časté (³1/1 000 až <1/100). ADRs boli zaznamenané v 6 klinických štúdiách (n=422) a boli prinajmenšom považované za nežiaduce reakcie s možnou príčinnou súvislosťou s podaním Nebida .
Tabuľka 1: Frekvencia mužov s ADRs, usporiadaná podľa MedDRA SOC – založené na zhromaždených údajoch zo šiestich klinických skúšaní, n=422 (100,0 %), t.j. n=302 mužov s hypogonadizmom, liečených 4 ml i.m. injekciami a n=120 mužov liečených 3 ml TU (testosterónundekanoátu) 250 mg/mlTrieda orgánových systémov
| Časté
(³1/100 až <1/10)
| Menej časté
(³1/1 000 až <1/100)
|
Poruchy krvi a lymfatického systému
| Polycytémia
| Zvýšený hematokrit
Zvýšený počet erytrocytov
Zvýšená hladinahemoglobínu
|
Poruchy imunitného systému
|
| Precitlivenosť
|
Poruchy metabolizmu a výživy
| Zvýšená telesná hmotnosť
| Zvýšená chuť do jedla
Zvýšená hladina glykozylovaného hemoglobínu
Hypercholesterolémia
Zvýšená hladina triglyceridov v krvi
Zvýšená hladina cholesterolu v krvi
|
Psychické poruchy
|
| Depresia
Emotívne poruchy
Nespavosť
Nepokoj
Agresivita
Podráždenosť
|
Poruchy nervového systému
|
| Bolesť hlavy
Migréna
Tras
|
Poruchy ciev
| Nával horúčavy
| Kardiovaskulárna porucha
Hypertenzia
Závrat
|
Poruchy dýchacej sústavy, hrudníka a mediastína
|
| Bronchitída
Sinusitída
Kašeľ
Dýchavica
Chrápanie
Dysfónia
|
Poruchy gastro-intestinálneho traktu
|
| Hnačka
Nevoľnosť
|
Poruchy pečene a žlčových ciest
|
| Abnormálne funkčné pečeňové testy
Zvýšená hladina aspartátaminotransferázy
|
Poruchy kože a podkožného tkaniva
| Akné
| Alopécia
Sčervenenie kože
Vyrážka 1
Pruritus
Suchá koža
|
Poruchy kostrovej a svalovej sústavy a spojivového tkaniva
|
| Artralgia
Bolesť v končatine
Svalové poruchy 2
Muskuloskeletárna stuhnutosť
Zvýšená hladina kreatínfosfokinázy v krvi
|
Poruchy obličiek a močových ciest
|
| Zoslabenie prúdu moču
Zadržiavanie moču
Poruchy močových ciest
Noktúria
Dyzúria
|
Poruchy reprodukčného systému a prsníkov
| Zvýšená hladina prostatického špecifického antigénu
Abnormálny výsledok vyšetrenia prostaty
Benígna hyperplázia prostaty
| Intraepitelový nádor prostaty
Indurácia prostaty
Prostatitída
Poruchy prostaty
Zmeny libida
Bolesť semenníkov
Indurácia prsníkov
Bolesť prsníkov
Gynekomastia
Zvýšená hladina estradiolu
Zvýšená hladina testosterónu
|
Celkové poruchy a reakcie v mieste podania
| Rozličné druhy reakcií v mieste vpichu3
| Únava
Asténia
Hyperhidróza 4
|
Na popis určitej nežiaducej reakcie sa uvádza najvhodnejší termín MedDRA (verzia 11.0). Synonymá a pridružené stavy nie sú uvedené, ale musia sa takisto vziať do úvahy.
1 Vyrážka vrátane papulárneho exantému
2 Poruchy svalov: svalové spazmy, napätie svalov a svalová bolesť
3 Rozličné druhy reakcií v mieste vpichu: Bolesť v mieste vpichu, diskomfort v mieste vpichu, pruritus v mieste vpichu, erytém v mieste vpichu , hematóm v mieste vpichu, podráždenie v mieste vpichu, reakcia v mieste vpichu
4 Hyperhidróza: Hyperhidróza a nočné potenie
Pulmonálna mikroembólia spojená s aplikáciou olejových roztokov môže v zriedkavých prípadoch viesť k znakom a príznakom, ako je kašeľ, dýchavičnosť, nevoľnosť, hyperhidróza, bolesť v hrudníku, závrat, parestézia a synkopa. Tieto reakcie sa môžu vyskytnúť počas aplikácie alebo ihneď po aplikácii a sú reverzibilné. V klinických skúšaniach, ako aj v rámci sledovania po uvedení lieku na trh sa hlásili zriedkavé (≥ 1/10 000 až <1/1 000 aplikácií) prípady, o ktorých sa spoločnosť alebo ohlasovateľ domnievali, že predstavujú pulmonálnu mikroembóliu spojenú s aplikáciou olejových roztokov (pozri časť 4.4 Osobitné upozornenia a opatrenia pri používaní).
Počas liečby liekmi s obsahom testosterónu sa okrem vyššie uvedených nežiaducich reakcií hlásila nervozita, nevraživosť, spánkové apnoe, rozličné kožné reakcie vrátane seborey, zvýšená frekvencia erekcií, a vo veľmi zriedkavých prípadoch žltačka.
Liečba vysokými dávkami liekov s obsahom testosterónu zvyčajne reverzibilne prerušuje alebo redukuje spermatogenézu, čím zmenšuje veľkosť semenníkov. Substitučná liečba hypogonadizmu testosterónom može v zriedkavých prípadoch vyvolať pretrvávajúce, bolestivé erekcie (priapizmus). Podávanie vysokých dávok testosterónu alebo dlhodobá liečba testosterónom niekedy zvyšujú výskyt zadržiavania vody a edémov.'
Hlásenie podozrení na nežiaduce reakcieHlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.
4.9 Predávkovanie
Po predávkovaní nie sú potrebné žiadne špeciálne terapeutické opatrenia okrem ukončenia liečby týmto liekom alebo zníženia dávky lieku.
5. FARMAKOLOGICKÉ VLASTNOSTI
5.1 Farmakodynamické vlastnosti
Farmakoterapeutická skupina: androgény, 3-oxoandrostén-4-deriváty
ATC kód: G03B A03
Testosterónundekanoát je ester prirodzene sa vyskytujúceho androgénu, testosterónu. Účinná forma, testosterón, sa tvorí odštiepením postranného reťazca.
Testosterón predstavuje najdôležitejší mužský androgén, ktorý sa tvorí hlavne v semenníkoch a v určitom malom množstve v kôre nadobličiek.
Testosterón je zodpovedný za prejav maskulínnej charakteristiky počas vývoja plodu, raného detstva a pubertálneho vývoja a následne za zachovanie mužského fenotypu a androgén-dependentných funkcií (napríklad spermatogenéza, prídavné pohlavné žľazy). Vykonáva aj ďalšie funkcie napríklad v koži, vo svaloch, v kostre, obličkách, pečeni, kostnej dreni a CNS.
V závislosti od cieľového orgánu je spektrum činností testosterónu hlavne androgénne (napr. prostata, semenníky, nadsemenníky) a proteínovo-anabolické (svaly, kosti, hematopoéza, obličky, pečeň).
Účinky testosterónu v niektorých orgánoch sa zvyšujú po periférnej premene testosterónu na estradiol, ktorý sa následne naviaže na estrogénové receptory v jadre cieľovej bunky, napr. hypofýzy, tuku, mozgu, kosti a Leydigových bunkách v semenníkoch.
5.2 Farmakokinetické vlastnosti
AbsorpciaNebido je intramuskulárne podávaný depotný prípravok s obsahom testosterónundekanoátu, a preto u neho nedochádza k first-pass efektu. Po intramuskulárnej injekčnej aplikácii testosterónundekanoátu vo forme olejového roztoku sa zlúčenina postupne uvoľňuje z miesta podania a takmer úplne sa rozštiepi sérovými esterázami na testosterón a kyselinu undecylénovú. Jeden deň po podaní je možné pozorovať zvýšenie hladiny testosterónu v sére nad bazálne hodnoty.
Ustálené stavyPo prvej intramuskulárnej injekčnej aplikácii 1 000 mg testosterónundekanoátu mužom trpiacim hypogonadizmom sa po siedmich dňoch dosiahli priemerné hodnoty C
max 38 nmol/l (11 ng/ml). Druhá dávka bola podaná šesť týždňov po prvej injekčnej aplikácii a dosiahli sa maximálne koncentrácie testosterónu približne 50 nmol/l (15 ng/ml). Počas nasledujúcich troch podaní bol udržiavaný konštantný dávkovací interval 10 týždňov a ustálené stavy sa dosiahli medzi tretím a piatym podaním. Priemerné hodnoty C
max a C
min hladiny testosterónu v ustálenom stave boli približne 37 nmol/l (11 ng/ml) resp. 16 nmol/l (5 ng/ml). Medián intra- a interindividuálnej variability (variačný koeficient, %) hodnôt C
min bol 22 % (rozsah: 9‑28 %) resp. 34 % (rozsah: 25‑48 %).
DistribúciaV sére mužov je približne 98 % cirkulujúceho testosterónu naviazaného na globulín viažuci pohlavné hormóny (SHBG) a albumín. Iba voľná frakcia testosterónu sa považuje za biologicky aktívnu. Po intravenóznej infúzii testosterónu starším mužom bol polčas vylučovania testosterónu približne jedna hodina a zistil sa zdanlivý objem distribúcie približne 1,0 l/kg.
BiotransformáciaTestosterón, ktorý sa tvorí odštiepením esteru z testosterónundekanoátu, sa metabolizuje a vylučuje rovnakým spôsobom ako endogénny testosterón. Kyselina undecylénová sa metabolizuje ß-oxidáciou rovnakým spôsobom ako ostatné alifatické karboxylové kyseliny. Hlavnými aktívnymi metabolitmi testosterónu sú estradiol a dihydrotestosterón.
ElimináciaTestosterón podlieha rozsiahlemu hepatálnemu a extrahepatálnemu metabolizmu. Po podaní rádioaktívne označeného testosterónu sa približne 90 % rádioaktivity objaví v moči ako konjugáty kyseliny glukorónovej a sírovej a 6 % sa objaví v stolici po enterohepatálnej cirkulácii. Medzi urologické lieky patrí androsterón a etiocholanolón. Po intramuskulárnej aplikácii tohoto depotného prípravku dosahuje rýchlosť uvoľňovania polčas 90±40 dní.
5.3 Predklinické údaje o bezpečnosti
Toxikologické štúdie neodhalili iné účinky než tie, ktoré je možné vysvetliť na základe hormonálneho profilu Nebida.
Pri testosteróne sa in vitro použitím reverzného mutačného modelu (Amesov test) alebo buniek vaječníkov škrečkov zistilo, že nemá mutagénne účinky. V pokusoch na laboratórnych zvieratách sa zistila súvislosť medzi liečbou androgénmi a určitými karcinómami. Experimentálne údaje z pokusov na potkanoch preukázali po liečbe testosterónom zvýšený výskyt karcinómu prostaty.
O pohlavných hormónoch je známe, že podporujú rast niektorých nádorov vyvolaných známymi karcinogénmi. Klinická platnosť tohto pozorovania nie je známa.
Štúdie plodnosti hlodavcov a primátov ukázali, že liečba testosterónom môže v závislosti od dávky znížiť plodnosť z dôvodu potlačenia spermatogenézy.
6. FARMACEUTICKÉ INFORMÁCIE
6.1 Zoznam pomocných látok
Benzylbenzoát
Ricínový olej rafinovaný
6.2 Inkompatibility
Keďže neboli vykonané žiadne štúdie kompatibility, tento liek sa nesmie miešať s inými liekmi.
6.3 Čas použiteľnosti
5 rokov
Tento liek sa musí použiť ihneď po prvom otvorení.
6.4 Špeciálne upozornenia na uchovávanie
Žiadne zvláštne upozornenia na uchovávanie.
6.5 Druh obalu a obsah balenia
Ampulka5 ml ampulky zo skla hnedej farby (typ I) s objemom náplne 4 ml.
Veľkosť balenia: 1 x 4 ml
Liekovka6 ml liekovky zo skla hnedej farby (typ I) so šedou brómbutylovou injekčnou zátkou (potiahnutá ETFE fóliou) a viečkom s obrubou s objemom náplne 4 ml.
Veľkosť balenia: 1 x 4 ml
Roztok na intramuskulárnu injekčnú aplikáciu treba pred použitím vizuálne skontrolovať. Používať sa môžu iba číre roztoky bez akýchkoľvek častíc.
Tento liek je určený iba na jedno použitie. Nepoužitý liek alebo odpad vzniknutý z lieku treba vrátiť do lekárne.
AmpulkaPoznámky o zaobchádzaní s OPC (One-Point-Cut) ampulkou:Aby sa na otvorenie ampulky nemusel použiť pilník, je na jej hrdle pod farebným bodom označená ryha. Pred otvorením zabezpečte, aby tekutina z vrchnej časti ampulky stiekla dolu do spodnej časti ampulky. Na otvorenie použite obe ruky; jednou rukou držte spodnú časť ampulky a druhou rukou o
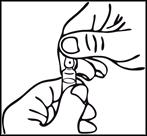
dlomte vrchnú časť smerom dozadu od farebného bodu.
LiekovkaLiekovka je len na jedno použitie.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCII
Bayer Pharma AG
D-13342 Berlín
Nemecko
8. REGISTRAČNÉ ČÍSLO
56/0144/05-S
9. DÁTUM PRVEJ REGISTRÁCIE/PREDĹŽENIA REGISTRÁCIE
Dátum prvej registrácie: 15.06.2005
Dátum posledného predĺženia registrácie: 07.07.2009
10. DÁTUM REVÍZIE TEXTU
Január 2015