bu pokročilého alebo metastatického (vzniknutého metastázovaním) karcinómu prsníka u žien po menopauze (prechode).
2. Čo potrebujete vedieť predtým, ako použijete Fulvestrant TevaNEPOUŽÍVAJTE Fulvestrant Teva, ak:- ste alergická na fulvestrant alebo na ktorúkoľvek z ďalších zložiek tohto lieku (uvedených v časti 6)
- ste tehotná alebo dojčíte (pozri časť „Tehotenstvo, dojčenie a plodnosť“)
- máte
závažné ťažkosti s pečeňou.
Upozornenia a opatreniaPredtým, ako začnete používať Fulvestrant Teva, obráťte sa na svojho lekára, lekárnika alebo zdravotnú sestru, ak sa vás týka ktorékoľvek z nasledujúceho:
- ťažkosti s obličkami alebo s pečeňou
- nízky počet krvných doštičiek (ktoré pomáhajú pri zrážaní krvi) alebo poruchy zrážania krvi
- problémy s krvnými zrazeninami v minulosti
- osteoporóza (úbytok kostnej hmoty, „rednutie kostí“)
- alkoholizmus (pozri časť „Fulvestrant Teva obsahuje etanol (96 %) (alkohol)“).
Deti a dospievajúciFulvestrant Teva NIE je určený na použitie u detí a dospievajúcich mladších ako 18 rokov.
Iné lieky a Fulvestrant TevaAk teraz užívate, alebo ste v poslednom čase užívali, či práve budete užívať ďalšie lieky, povedzte to svojmu lekárovi, lekárnikovi alebo zdravotnej sestre.
Svojho lekára informujte najmä vtedy, ak užívate antikoagulanciá (lieky používané na predchádzanie tvorby krvných zrazenín).
Tehotenstvo, dojčenie a plodnosťFulvestrant Teva NESMIETE používať, ak ste tehotná. Ak by ste mohli otehotnieť, počas liečby Fulvestrantom Teva musíte používať účinný spôsob antikoncepcie (zabránenia počatiu).
Počas liečby Fulvestrantom Teva NESMIETE dojčiť.
Vedenie vozidiel a obsluha strojovNeočakáva sa, že by Fulvestrant Teva ovplyvnil vašu schopnosť viesť vozidlá alebo obsluhovať stroje. Ak však po podaní tohto lieku pociťujete únavu, NEVEĎTE vozidlá ani NEOBSLUHUJTE stroje.
Fulvestrant Teva obsahuje etanol (96 %) (alkohol), t.j. až do 1 000 mg na dávku, čo zodpovedá 20 ml piva alebo 8 ml vína na dávku.
Je škodlivý pre osoby, ktoré trpia alkoholizmom.
Má sa to vziať to do úvahy u tehotných alebo dojčiacich žien, u detí a u vysokorizikových skupín, akými sú pacientky s ochorením pečene alebo s epilepsiou.
Fulvestrant Teva obsahuje benzylalkohol, pričom množstvo benzylalkoholu na dávku je 500 mg v 5 ml (100 mg v 1 ml) a môže vyvolať alergické reakcie.
Fulvestrant Teva obsahuje rafinovaný ricínový olej, ktorý môže vyvolať závažné alergické reakcie.
3. Ako používať Fulvestrant TevaOdporúčaná dávka je 500 mg fulvestrantu (dve injekcie, z ktorých každá obsahuje 250 mg fulvestrantu v 5 ml roztoku) podávaných raz za mesiac, pričom 2 týždne po úvodnej dávke sa podá dodatočná dávka 500 mg.
Váš lekár alebo zdravotná sestra vám podá obidve injekcie Fulvestrantu Teva vo forme pomalej vnútrosvalovej injekcie, jednu do pravého a druhú do ľavého sedacieho svalu.
Ak máte akékoľvek ďalšie otázky týkajúce sa použitia tohto lieku, opýtajte sa svojho lekára, lekárnika alebo zdravotnej sestry.
4. Možné vedľajšie účinkyTak ako všetky lieky, aj tento liek môže spôsobovať vedľajšie účinky, hoci sa neprejavia u každého.
BEZODKLADNE informujte svojho lekára, lekárnika alebo zdravotnú sestru, ak sa u vás objaví ktorýkoľvek z nasledujúcich vedľajších účinkov:· alergické reakcie (reakcie z precitlivenosti), ktoré zahŕňajú opuch tváre, pier, jazyka a/alebo hrdla
· tromboembolizmus (zvýšené riziko tvorby krvných zrazenín)*
· zápal pečene (hepatitída)
· zlyhávanie pečene.
Tieto vedľajšie účinky sú závažné. Môžete potrebovať okamžité lekárske ošetrenie.
Informujte svojho lekára, lekárnika alebo zdravotnú sestru, ak spozorujete ktorýkoľvek z nasledujúcich vedľajších účinkov:Veľmi časté: môžu postihovať viac ako 1 z 10 osôb
· reakcie v mieste vpichu, napríklad bolesť a/alebo zápal
· abnormálne (mimo normy) hladiny pečeňových enzýmov (z vyšetrenia krvi )*
· nauzea (napínanie na vracanie)
· slabosť, únava*.
Časté: môžu postihovať menej ako 1 z 10 osôb
· bolesť hlavy
· návaly tepla
· vracanie (dávenie), hnačka alebo nechutenstvo*
· vyrážka
· infekcie močových ciest
· bolesť chrbta*
· zvýšená hladina bilirubínu (žlčové farbivo tvorené v pečeni).
Menej časté: môžu postihovať menej ako 1 zo 100 osôb
· znížený počet krvných doštičiek (trombocytopénia)
· krvácanie z pošvy, hustý belavý výtok z pošvy a kandidóza (kvasinková infekcia) sliznice pošvy
· krvná podliatina a krvácanie v mieste vpichu
· zvýšená hladina pečeňového enzýmu nazývaného gamaglutamyltransferáza, ktorá je zistená vyšetrením krvi.
* Vrátane vedľajších účinkov, pri ktorých sa kvôli základnému ochoreniu nedá presne stanoviť, v akej miere sa na ich vzniku podieľa fulvestrant.
Hlásenie vedľajších účinkovAk sa u vás vyskytne akýkoľvek vedľajší účinok, obráťte sa na svojho lekára, lekárnika alebo zdravotnú sestru. To sa týka aj akýchkoľvek vedľajších účinkov, ktoré nie sú uvedené v tejto písomnej informácii. Vedľajšie účinky môžete hlásiť aj priamo prostredníctvom národného systému hlásenia uvedeného v
Prílohe V. Hlásením vedľajších účinkov môžete prispieť k získaniu ďalších informácií o bezpečnosti tohto lieku.
5. Ako uchovávať Fulvestrant TevaTento liek uchovávajte mimo dohľadu a dosahu detí.Nepoužívajte tento liek po dátume exspirácie, ktorý je uvedený na škatuľke alebo na označení injekčnej striekačky po „EXP“. Dátum exspirácie sa vzťahuje na posledný deň v danom mesiaci.
Nepoužívajte tento liek, ak pred podaním spozorujete, že obsahuje cudzorodé častice alebo že má zmenenú farbu.
Naplnenú injekčnú striekačku uchovávajte v pôvodnom balení na ochranu pred svetlom.
Uchovávajte a prepravujte v chladničke (2 °C ‑ 8 °C).
Je potrebné obmedziť výskyt teplotných odchýlok mimo rozmedzia 2 °C ‑ 8 °C. V tomto zmysle sa treba vyhnúť uchovávaniu lieku pri teplotách prevyšujúcich 25 °C a pokiaľ je priemerná teplota uchovávania lieku nižšia ako 25 °C (ale vyššia ako 2 °C ‑ 8 °C), takéto uchovávanie nemá trvať dlhšie ako 28 dní. Po výskyte teplotnej odchýlky sa treba ihneď vrátiť k odporúčaným podmienkam uchovávania lieku (uchovávanie a prepravovanie v chladničke pri 2 °C ‑ 8 °C). Teplotné odchýlky majú kumulatívny vplyv na kvalitu lieku a nesmú trvať súvisle dlhšie ako 28 dní počas celého 2-ročného času použiteľnosti Fulvestrantu Teva. Vystavenie lieku teplotám nižším ako 2 °C nespôsobí jeho poškodenie, pokiaľ nie je uchovávaný pri teplote nižšej ako ‑20 °C.
Váš zdravotnícky pracovník bude zodpovedný za správne uchovávanie, použitie a likvidáciu Fulvestrantu Teva.
6. Obsah balenia a ďalšie informácieČo Fulvestrant Teva obsahuje- Liečivo je fulvestrant. Každá naplnená injekčná striekačka obsahuje 250 mg fulvestrantu. Každý ml roztoku obsahuje 50 mg fulvestrantu.
- Ďalšie zložky (pomocné látky) sú etanol (96 %), benzylalkohol, benzylbenzoát a rafinovaný ricínový olej.
Ako vyzerá Fulvestrant Teva a obsah baleniaFulvestrant Teva je číry, bezfarebný až žltý, viskózny roztok v naplnenej injekčnej striekačke vybavenej poistným uzáverom, ktorá obsahuje 5 ml injekčného roztoku. Musia sa použiť dve injekčné striekačky, aby sa podala odporúčaná mesačná 500 mg dávka.
Fulvestrant Teva sa dodáva v 2 veľkostiach balenia:
1 balenie obsahuje 1 sklenenú naplnenú injekčnú striekačku a 1 bezpečnostnú ihlu, ktorá sa má pripojiť k valcu injekčnej striekačky.
1 balenie obsahuje 2 sklenené naplnené injekčné striekačky a 2 bezpečnostné ihly, ktoré sa majú pripojiť k valcom injekčných striekačiek.
Na trh nemusia byť uvedené všetky veľkosti balenia.
Držiteľ rozhodnutia o registrácii a výrobcaDržiteľ rozhodnutia o registráciiTEVA Pharmaceuticals Slovakia s.r.o.
Teslova 26, 821 02 Bratislava
Slovenská republika
VýrobcaPliva Croatia Ltd.
Prilaz baruna Filipovica 25
10000 Zagreb
Chorvátsko
Teva Pharmaceutical Works Private Limited Company
Táncsics Mihály út 82
H-2100 Gödöllő
Maďarsko
Teva Operations Poland Sp. z o.o.
Ul. Mogilska 80,
31-546 Krakow
Poľsko
Liek je schválený v členských štátoch Európskeho hospodárskeho priestoru (EHP) pod nasledovnými názvami:Belgicko Fulvestrant Teva 250 mg oplossing voor injectie/solution injectable/ Injektionslösung
Bulharsko Фулвестрант Тева 250 mg нжекционен разтвор в предварително напълнена спринцовка
Česká republika Fulvestrant Teva 250 mg/5ml, injekční roztok v předplněné injekční stříkačce
Dánsko Fulvestrant Teva
Estónsko Fulvestrant Teva
Fínsko Fulvestrant Teva 250 mg injektioneste, liuos, esitäytetty ruisku
Francúzsko Fulvestrant Teva 250 mg solution injectableen seringue préremplie
Holandsko Fulvestrant Teva 250 mg/5 ml, oplossing voor injectie in een voorgevulde spuit
Chorvátsko Fulvestrant Pliva 250 mg otopina za injekciju u napunjenoj štrcaljki'
Írsko Fulvestrant Teva 250mg Solution for injection in Pre-filled Syringe
Island Fulvestrant Teva 250 mg stungulyf, lausn í áfylltri sprautu
Litva Fulvestrant Teva 250 mg injekcinis tirpalas užpildytame švirkšte
Lotyšsko Fulvestrant Teva 250 mg šķīdums injekcijām pilnšļircē
Luxembursko Fulvestrant Teva 250 mg oplossing voor injectie/solution injectable/ Injektionslösung
Maďarsko Fulvestrant Teva 250 mg/5 ml oldatos injekció előretöltött fecskendőben
Malta Fulvestrant Teva 250mg Solution for injection in Pre-filled Syringe
Nemecko Fulvestrant Teva 250 mg Injektionslösung in einer Fertigspritze
Poľsko Fulvestrant Teva
Portugalsko Fulvestrant Teva
Rakúsko Fulvestrant ratiopharm 250 mg Injektionslösung
Rumunsko Fulvestrant Teva 250 mg soluţie injectabilă în seringă preumplută
Slovenská republika Fulvestrant Teva 250 mg
Slovinsko Fulvestrant Teva 250 mg raztopina za injiciranje v napolnjeni injekcijski brizgi
Spojené kráľovstvo Fulvestrant Teva 250mg solution for injection in pre-filled syringe
Španielsko Fulvestrant Teva 250 mg Solución inyectable EFG
Švédsko Fulvestrant Teva
Taliansko Fulvestrant Teva
Táto písomná informácia bola naposledy aktualizovaná v 4/2016.
----------------------------------------------------------------------------------------------------------------------------------
Nasledujúca informácia je určená len pre zdravotníckych pracovníkov:Fulvestrant Teva v dávke 500 mg (2 x 250 mg/5 ml injekčný roztok) sa má podať s použitím dvoch naplnených injekčných striekačiek.
Pokyny na podávanieUpozornenie ‑ bezpečnostnú ihlu pred použitím neautoklávujte. Počas používania a pri likvidácii musia ruky stále zostať za ihlou.
Pri každej z dvoch injekčných striekačiek:
· Vyberte sklenený valec injekčnej striekačky z vaničky a skontrolujte, či nie je poškodený.
· Zlomte plombu priehľadného plastového uzávera na prípojke Luer‑Lock (t.j. na kónuse so závitom) injekčnej striekačky a snímte uzáver s pripojenou gumovou zátkou (pozri obrázok 1).
| Obrázok 1

|
· Odstráňte vonkajší obal bezpečnostnej ihly. Nasaďte bezpečnostnú ihlu na prípojku Luer‑Lock (pozri obrázok 2).
· Otáčajte ihlu, pokým pevne nedosadne.
|
Obrázok 2

|
· Pootočením ju zafixujte v prípojke Luer-Lock.
· Stiahnite puzdro z ihly v priamom smere, aby ste zabránili poškodeniu hrotu ihly (pozri obrázok 3).
| Obrázok 3

|
· Preneste naplnenú injekčnú striekačku na miesto, kde ju budete podávať.
· Parenterálne podávané roztoky sa pred podaním musia zrakom skontrolovať na prítomnosť cudzorodých častíc a zmenu farby.
· Vytlačte z injekčnej striekačky prebytočný vzduch.
· Podajte pomaly intramuskulárne (1 ‑ 2 minúty/injekcia) do sedacieho svalu. Pri aplikácii je pre používateľa výhodnejšie, ak je skosená hrana ihly orientovaná smerom k páčke ramena (pozri obrázok 4).
| Obrázok 4
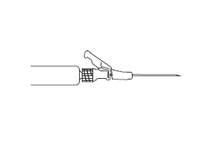
|
· Ihneď po podaní injekcie využite ťah jedného prsta na aktiváciu ramena páčky, čím aktivujete ochranný (bezpečnostný) mechanizmus ihly (pozri obrázok 5).
POZNÁMKA: Aktivujte mechanizmus smerom od seba a iných. Musíte počuť cvaknutie a zrakom sa presvedčte, že hrot ihly je úplne zakrytý.
|
Obrázok 5
|
LikvidáciaNaplnené injekčné striekačky sú určené
len na jednorazové použitie.
Všetok nepoužitý liek alebo odpad vzniknutý z lieku sa má zlikvidovať v súlade s národnými požiadavkami.