lnému intervalu bez užívania, tým vyššie je riziko gravidity.
·
2. týždeňŽena má užiť poslednú vynechanú tabletu hneď, ako si spomenie, aj keby to znamenalo užitie dvoch tabliet súčasne. Potom pokračuje v užívaní tabliet vo zvyčajnom čase. Ak žena užívala tablety počas 7 dní pred prvou vynechanou tabletou správne, ďalšie antikoncepčné opatrenia nie sú potrebné. Ak však vynechala viac ako 1 tabletu, má sa jej odporučiť použitie ďalšieho ochranného opatrenia počas 7 dní nasledujúcich po poslednej vynechanej tablete.
·
3. týždeňVzhľadom na nastávajúci sedemdňový interval bez užívania tabliet je veľké nebezpečenstvo zníženia spoľahlivosti antikoncepcie. Upravením schémy užívania tabliet možno aj napriek tomu predísť zníženiu antikoncepčnej ochrany. Pri dodržaní niektorého z dvoch nasledujúcich postupov nie je potrebné používať ďalšie antikoncepčné opatrenia za predpokladu, že počas 7 dní pred vynechaním prvej tablety žena užila všetky tablety správne. Ak to tak nie je, žena má postupovať podľa prvej z týchto dvoch možností a počas nasledujúcich 7 dní navyše použiť ďalšie antikoncepčné opatrenia.
1. Žena má užiť poslednú vynechanú tabletu hneď, ako si spomenie, aj keby to znamenalo užitie dvoch tabliet súčasne. Potom pokračuje v užívaní tabliet vo zvyčajnom čase. Užívanie tabliet z nasledujúceho blistra potom musí začať okamžite po využívaní predchádzajúceho, t.j. medzi baleniami nie je žiadna prestávka. Krvácanie z vysadenia sa pravdepodobne nedostaví pred doužívaním všetkých tabliet z druhého balenia, ale počas užívania tabliet môže nastať špinenie alebo medzimenštruačné krvácanie.
2. Žene možno tiež poradiť, aby prerušila užívanie tabliet zo súčasného blistrového balenia. Tým vznikne interval najviac siedmich dní bez užívania tabliet vrátane dní, kedy sa tablety vynechali a nasleduje užívanie tabliet z ďalšieho blistrového balenia.
Ak žena zabudne užiť tablety a následne sa nedostaví krvácanie z vysadenia v prvom normálnom intervale bez užívania tabliet, musí sa zvážiť možnosť gravidity.
Odporúčania v prípade gastrointestinálnych porúchV prípade závažných gastrointestinálnych ťažkostí (napr. vracania alebo hnačky) nemusí byť vstrebávanie úplné a musia sa použiť ďalšie antikoncepčné opatrenia. Ak počas 3 ‑ 4 hodín po užití tablety dôjde k vracaniu, má sa čo najskôr užiť nová tableta. Ak je to možné, tableta sa má užiť do 12 hodín od zvyčajného času užívania tablety. V prípade, že uplynulo viac ako 12 hodín, platí odporúčanie týkajúce sa vynechaných tabliet, uvedené v časti 4.2. „Postup pri vynechaní tabliet“. Ak žena nechce zmeniť zvyčajnú schému užívania tabliet, musí užiť dodatočnú tabletu (tablety) z ďalšieho blistrového balenia.
Ako posunúť krvácanie z vysadeniaAk si žena želá oddialiť menštruáciu, má pokračovať v užívaní tabliet z ďalšieho blistrového balenia lieku Baradly bez prestávky. Oddialiť menštruáciu je možné na tak dlhý čas, ako si žena želá, až do doužívania tabliet z druhého balenia. Počas tohto obdobia odďaľovania menštruácie sa u ženy môže objaviť medzimenštruačné krvácanie alebo špinenie. Po sedemdňovom intervale bez užívania tabliet sa potom obnoví pravidelné užívanie lieku Baradly.
Ak si žena želá presunúť menštruáciu na iný deň v týždni, než na aký je zvyknutá v doterajšej schéme užívania, možno jej odporučiť, aby skrátila interval bez užívania tabliet o toľko dní, o koľko si praje. Čím kratší bude tento interval, tým väčšie je riziko, že nedôjde ku krvácaniu z vysadenia a že počas užívania nasledujúceho balenia sa vyskytne medzimenštruačné krvácanie a špinenie (podobne ako pri oddialení menštruácie).
4.3 KontraindikácieKombinovaná perorálna antikoncepcia (CHC) sa nemá používať, v prípade výskytu niektorého z nižšie uvedených stavov. Ak sa niektorý z týchto stavov objaví prvý raz v priebehu používania CHC, užívanie sa má okamžite ukončiť:
• Prítomnosť alebo riziko vzniku venóznej tromboembólie (VTE)
○ Venózna tromboembólia - prítomná VTE (liečená antikoagulanciami) alebo v anamnéze (napr. trombóza hĺbkových žíl [DVT] alebo pľúcna embólia [PE]).
○ Známa dedičná alebo získaná predispozícia na vznik venóznej tromboembólie, ako napríklad rezistencia voči APC (vrátane faktora V Leiden), deficiencia antitrombínu-III, deficiencia proteínu C, deficiencia proteínu S.
○ Závažný chirurgický zákrok s dlhodobou imobilizáciou (pozri časť 4.4).
○ Vysoké riziko vzniku venóznej tromboembólie z dôvodu prítomnosti viacerých rizikových faktorov (pozri časť 4.4).
• Prítomnosť alebo riziko vzniku arteriálnej tromboembólie (ATE)
○ Arteriálna tromboembólia - prítomná arteriálna tromboembólia, arteriálna tromboembólia v anamnéze (napríklad infarkt myokardu) alebo stav, ktorý je jej skorým príznakom (napríklad
angina pectoris).
○ Cievne mozgové ochorenie - prítomná cievna mozgová príhoda, cievna mozgová príhoda v anamnéze alebo stav, ktorý je jej skorým príznakom (napríklad prechodný ischemický záchvat, TIA).
○ Známa vrodená alebo získaná predispozícia na vznik arteriálnej tromboembólie, ako napríklad hyperhomocysteinémia a antifosfolipidové protilátky (antikardiolipínové protilátky, lupusové antikoagulancium).
○ Migréna s ložiskovými neurologickými symptómami v anamnéze.
○ Vysoké riziko vzniku arteriálnej tromboembólie z dôvodu viacerých rizikových faktorov (pozri časť 4.4) alebo prítomnosti jedného závažného rizikového faktora, ako napríklad:
• diabetes mellitus s cievnymi symptómami,
• závažná hypertenzia,
• závažná dyslipoproteinémia.
· Závažné ochorenie pečene, prítomné alebo v anamnéze, až do návratu pečeňových funkcií na normálne hodnoty
· Závažná obličková nedostatočnosť alebo akútne zlyhávanie obličiek
· Nádory pečene, prítomné alebo v anamnéze (benígne alebo malígne)
· Diagnostikované malignity závislé od pohlavných steroidov alebo podozrenie na ne (napr. pohlavných orgánov alebo prsníka)
· Vaginálne krvácanie s nediagnostikovanou príčinou
· Precitlivenosť na liečivá alebo na ktorúkoľvek z pomocných látok uvedených v časti 6.1.
4.4 Osobitné upozornenia a opatrenia pri používaníUpozorneniaAk je prítomný ktorýkoľvek zo stavov alebo rizikových faktorov uvedených nižšie, vhodnosť užívania lieku Baradly sa má s danou ženou prekonzultovať. Ženu treba upozorniť, že ak dôjde k zhoršeniu alebo prvému prejavu ktoréhokoľvek z týchto stavov alebo rizikových faktorov, má sa obrátiť na svojho lekára, ktorý určí, či má ukončiť užívanie lieku Baradly.
V prípade suspektnej alebo potvrdenej VTE alebo ATE, užívanie kombinovanej hormonálnej antikoncepcie sa má ukončiť. Ak sa začne s antikoagulačnou liečbou, má sa začať s adekvátnou alternatívnou antikoncepciou kvôli teratogenite antikoagulačnej liečby (kumaríny).
Riziko vzniku venóznej tromboembólie (VTE)Používanie ktorejkoľvek kombinovanej hormonálnej antikoncepcie (CHC) zvyšuje riziko vzniku venóznej tromboembólie (VTE) v porovnaní s jej nepoužívaním.
Lieky, ktoré obsahujú levonorgestrel, norgestimát alebo noretisterón, sú spojené s najnižším rizikom vzniku VTE. Iné lieky, ako je liek Baradly, môžu mať toto riziko až dvojnásobne vyššie. Rozhodnutie používať ktorýkoľvek iný liek, ako liek s najnižším rizikom vzniku VTE, sa má urobiť len po konzultácii s danou ženou, aby sa zaručilo, že rozumie riziku vzniku VTE pri používaní lieku Baradly, tomu, ako jej aktuálne rizikové faktory ovplyvňujú toto riziko, a že riziko vzniku VTE je najvyššie v prvom roku používania CHC. Sú taktiež aj určité dôkazy o tom, že sa toto riziko zvyšuje pri opätovnom začatí používania kombinovanej hormonálnej antikoncepcie po prerušení používania trvajúcom 4 týždne alebo dlhšie.U približne 2 z 10 000 žien, ktoré nepoužívajú kombinovanú hormonálnu antikoncepciu a nie sú gravidné, vznikne VTE v priebehu jedného roka. Avšak u každej jednej ženy môže byť toto riziko oveľa vyššie v závislosti od prítomných rizikových faktorov (pozri nižšie).
Odhaduje sa
1, že VTE sa vyskytne v priebehu jedného roka u 9 až 12 žien z 10 000 žien, ktoré používajú kombinovanú hormonálnu antikoncepciu obsahujúcu drospirenón, v porovnaní s približne 6
2 ženami, ktoré používajú kombinovanú hormonálnu antikoncepciu obsahujúcu levonorgestrel.
V oboch prípadoch je počet výskytov VTE za rok nižší ako počet očakávaný u žien počas gravidity alebo v období po pôrode.
VTE sa môže v 1 až 2 % prípadov skončiť smrťou.
1 Tieto incidencie boli odhadnuté zo všetkých dát z epidemiologických štúdií, použitím relatívnych rizík pre rôzne lieky v porovnaní s kombinovanou hormonálnou antikoncepciou obsahujúcimi levonorgestrel.
2 Stredný bod rozpätia 5-7 (prípadov) na 10 000 ženských rokov (ŽR), založený na relatívnom riziku kombinovanej hormonálnej antikoncepcie obsahujúcej levonorgestrel oproti 2,3 až 3,6 u nepoužívateliek.
Počet prípadov VTE na 10 000 žien v priebehu jedného roka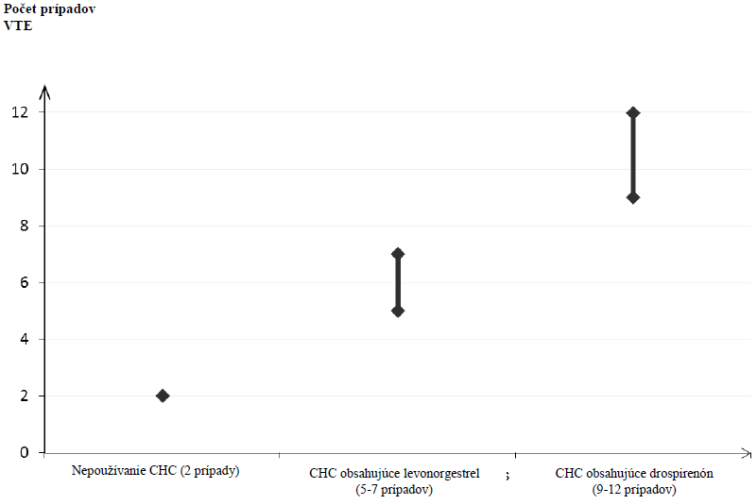
_________________
U používateliek CHC bol mimoriadne zriedkavo hlásený výskyt trombózy v iných krvných cievach, napr. v pečeňových, mezenterických, obličkových alebo sietnicových žilách a tepnách.
Rizikové faktory vzniku VTE Riziko vzniku venóznych tromboembolických komplikácií u používateliek kombinovanej hormonálnej antikoncepcie sa môže značne zvýšiť v prípade ženy s ďalšími rizikovými faktormi, najmä ak má viacero rizikových faktorov (pozri tabuľku).
Liek Baradly je kontraindikovaný, ak má žena viacero rizikových faktorov, ktoré ju vystavujú vysokému riziku vzniku venóznej trombózy (pozri časť 4.3). Ak má žena viac ako jeden rizikový faktor, zvýšenie rizika môže byť väčšie než súčet jednotlivých faktorov - v takomto prípade sa má zvážiť jej celkové riziko výskytu VTE. Ak sa pomer prínosov a rizík považuje za negatívny, kombinovaná hormonálna antikoncepcia sa nemá predpisovať (pozri časť 4.3).
Tabuľka: Rizikové faktory pre vznik VTERizikový faktor
| Komentár
|
Obezita (index telesnej hmotnosti nad 30 kg/m²)
| Riziko sa výrazne zvyšuje so zvyšovaním BMI.
Obzvlášť dôležité je to zvážiť, ak sú prítomné aj ďalšie rizikové faktory.
|
Dlhodobá imobilizácia, závažný chirurgický zákrok, akýkoľvek chirurgický zákrok na nohách alebo panve, neurochirurgický zákrok alebo závažný úraz.
Poznámka: dočasná imobilizácia vrátane cestovania leteckou dopravou trvajúcou >4 hodiny môže byť tiež rizikovým faktorom pre vznik VTE, najmä u žien s ďalšími rizikovými faktormi.
| V týchto prípadoch sa odporúča prerušiť používanie náplasti/tablety/krúžku (v prípade plánovaného chirurgického zákroku najmenej štyri týždne pred zákrokom) a pokračovať v ňom najskôr dva týždne po
úplnom obnovení pohyblivosti. Má sa používať iný spôsob antikoncepcie, aby sa zabránilo neželanej gravidite.
Ak sa užívanie lieku Baradly nepreruší včas, má sa zvážiť antitrombotická liečba.
|
Pozitívna rodinná anamnéza (akýkoľvek výskyt venóznej tromboembólie u súrodenca alebo rodiča, najmä v relatívne skorom veku, napr. do 50 rokov).
| Ak existuje podozrenie na dedičnú predispozíciu, žena sa má pred rozhodnutím o používaní ktorejkoľvek kombinovanej hormonálnej antikoncepcie poradiť s odborným lekárom.
|
Iné zdravotné stavy spojené s VTE
| Rakovina, systémový lupus erythematosus, hemolyticko-uremický syndróm, chronické zápalové ochorenie čriev (Crohnova choroba alebo ulcerózna kolitída) a kosáčikovitá anémia
|
Zvyšujúci sa vek
| Najmä nad 35 rokov
|
Neexistuje žiadna zhoda ohľadom možnej úlohy kŕčových žíl a povrchovej tromboflebitídy pri vzniku alebo progresii venóznej trombózy.
Musí sa zvážiť zvýšené riziko vzniku tromboembólie počas gravidity a najmä počas 6-týždňového obdobia šestonedelia (informácie o „Fertilite, gravidite a laktácii“, pozri časť 4.6).
Príznaky VTE (trombóza hĺbkových žíl a pľúcna embólia) Žená má byť poučená, aby v prípade príznakov vyhľadala okamžitú lekársku pomoc a informovala zdravotníckeho pracovníka, že používa kombinovanú hormonálnu antikoncepciu.
Príznaky trombózy hĺbkových žíl (DVT) môžu zahŕňať:
– jednostranný opuch nohy a/alebo chodidla alebo pozdĺž žily v nohe,
– bolesť alebo citlivosť v nohe, ktorú možno pociťovať iba v stoji alebo pri chôdzi,
– zvýšené teplo v postihnutej nohe, sčervenanie alebo zmena sfarbenia pokožky na nohe.
Príznaky pľúcnej embólie (PE) môžu zahŕňať:
– náhly nástup nevysvetliteľnej dýchavičnosti alebo rýchleho dýchania,
– náhly kašeľ, ktorý môže súvisieť s hemoptýzou,
– ostrú bolesť v hrudníku,
– závažný pocit točenia hlavy alebo závrat,
– rýchly alebo nepravidelný srdcový rytmus.
Niektoré z týchto príznakov (napríklad „dýchavičnosť“, „kašeľ“) sú nešpecifické a môžu byť nesprávne interpretované ako častejšie alebo menej závažné udalosti (napríklad infekcie dýchacích ciest).
Medzi ďalšie prejavy vaskulárnej oklúzie môžu patriť: náhla bolesť, opuch a mierne zmodranie niektorej končatiny.
Ak dôjde k oklúzii v oku, medzi symptómy môžu patriť bezbolestné rozmazané videnie, ktoré môže postupne prechádzať až do straty zraku. Niekedy môže dôjsť k strate zraku takmer okamžite.
Riziko vzniku arteriálnej tromboembólie (ATE) Epidemiologické štúdie spájajú používanie kombinovanej hormonálnej antikoncepcie so zvýšeným rizikom vzniku arteriálnej tromboembólie (infarkt myokardu) alebo cievnej mozgovej udalosti (napr. prechodný ischemický záchvat, cievna mozgová príhoda). Arteriálne tromboembolické udalosti sa môžu končiť smrťou.
Rizikové faktory pre vznik ATE Riziko vzniku arteriálnych tromboembolických komplikácií alebo cerebrovaskulárnej udalosti u používateliek kombinovanej hormonálnej antikoncepcie sa zvyšuje u žien s rizikovými faktormi (pozri tabuľku). Liek Baradly je kontraindikovaný, ak má žena jeden závažný alebo viacero rizikových faktorov vzniku ATE, ktoré ju vystavujú vysokému riziku vzniku arteriálnej trombózy (pozri časť 4.3). Ak má žena viac než jeden rizikový faktor, zvýšenie rizika môže byť väčšie než súčet jednotlivých faktorov - v takomto prípade sa má zvážiť jej celkové riziko. Ak sa pomer prínosov a rizík považuje za negatívny, kombinovaná hormonálna antikoncepcia sa nemá predpisovať (pozri časť 4.3).
Tabuľka: Rizikové faktory vzniku ATERizikový faktor
| Komentár
|
Zvyšujúci sa vek
| Najmä nad 35 rokov
|
Fajčenie
| Ženám sa má odporučiť, aby nefajčili, ak chcú používať kombinovanú hormonálnu antikoncepciu. Ženám vo veku nad 35 rokov, ktoré pokračujú vo fajčení, sa má dôrazne odporučiť, aby používali iný spôsob antikoncepcie.
|
Hypertenzia
|
|
Obezita (index telesnej hmotnosti nad 30 kg/m²).
| Riziko sa výrazne zvyšuje so zvyšovaním BMI.
To je dôležité najmä u žien s ďalšími rizikovými faktormi.
|
Pozitívna rodinná anamnéza (akýkoľvek výskyt arteriálnej tromboembólie u súrodenca alebo rodiča, najmä v relatívne mladom veku, napr. do 50 rokov).
| Ak existuje podozrenie na dedičnú predispozíciu, ženu musí pred rozhodnutím o používaní ľubovoľnej kombinovanej hormonálnej antikoncepcie vyšetriť odborný lekár.
|
Migréna
| Zvýšenie frekvencie alebo závažnosti migrény v priebehu používania kombinovanej hormonálnej antikoncepcie (čo môžu byť skoré príznaky cievnej mozgovej príhody) môže byť dôvodom na okamžité prerušenie používania lieku.
|
Ďalšie zdravotné stavy spojené s nežiaducimi vaskulárnymi udalosťami.
| Diabetes mellitus, hyperhomocysteinémia, ochorenie srdcových chlopní a atriálna fibrilácia, dyslipoproteinémia a systémový lupus erythematosus.
|
Príznaky ATE V prípade príznakov sa má žene odporučiť, aby bezodkladne vyhľadala lekársku pomoc a informovala zdravotníckeho pracovníka, že používa kombinovanú hormonálnu antikoncepciu.
Príznaky cievnej mozgovej príhody môžu zahŕňať:
– náhla strata citlivosti alebo slabosť tváre, ruky alebo nohy, najmä na jednej strane tela,
– náhle problémy s chôdzou, závrat, strata rovnováhy alebo koordinácie,
– náhla zmätenosť, problémy s rečou alebo jej porozumením,
– náhle problémy so zrakom u jedného alebo oboch očí,
– náhla, závažná alebo dlhodobá bolesť hlavy bez známej príčiny,
– strata vedomia alebo mdloba so záchvatom alebo bez neho.
Dočasné príznaky naznačujú, že udalosťou je prechodný ischemický záchvat (TIA).
Príznaky infarktu myokardu (MI) môžu zahŕňať:
– bolesť, nepohodlie, tlak, ťažoba, pocit stláčania alebo plnosti v hrudi, ruke alebo pod hrudnou kosťou,
– nepohodlie vyžarujúce do chrbta, čeľuste, hrdla, ruky, žalúdka,
– pocit plnosti, zažívacích problémov alebo dusenia sa,
– potenie, nevoľnosť, vracanie alebo závrat,
– extrémna slabosť, úzkosť alebo dýchavičnosť,
– rýchly alebo nepravidelný srdcový rytmus.
·
NádoryV niektorých epidemiologických štúdiách bolo hlásené zvýšené riziko rakoviny krčka maternice u žien, ktoré dlhodobo (> 5 rokov) užívali COC. Pretrváva však rozdielnosť názorov na to, do akej miery sa dajú tieto nálezy pripísať následkom sexuálneho správania a iným faktorom, ako je napríklad ľudský papilomavírus (HPV).
Metaanalýza 54 epidemiologických štúdií uvádza, že sa mierne zvýšilo relatívne riziko (RR = 1,24) diagnostikovania rakoviny prsníka u žien počas užívania COC. Zvýšené riziko postupne klesá v priebehu 10 rokov po ukončení užívania COC. Pretože výskyt rakoviny prsníka je u žien do 40 rokov zriedkavý, zvýšený počet prípadov diagnostikovanej rakoviny prsníka u žien, ktoré užívajú alebo užívali COC, je v pomere k celkovému riziku rakoviny prsníka malý. Kauzalitu tieto štúdie nedokazujú. Pozorované zvýšenie rizika môže byť zapríčinené skoršou diagnózou rakoviny prsníka u žien užívajúcich COC, biologickým účinkom COC alebo ich kombináciou. Rakovina prsníka diagnostikovaná u žien, ktoré v minulosti užívali COC, býva klinicky menej rozvinutá ako u žien, ktoré COC neužívali nikdy.
V zriedkavých prípadoch boli u žien užívajúcich COC hlásené benígne a ešte zriedkavejšie malígne nádory pečene. V ojedinelých prípadoch viedli tieto nádory k život ohrozujúcemu intraabdominálnemu krvácaniu. V prípade výskytu závažných bolestí v hornej časti abdominálnej oblasti, zväčšenia pečene alebo príznakov intraabdominálneho krvácania u žien užívajúcich COC sa má v diferenciálnej diagnóze uvažovať o nádore pečene.
Riziko výskytu endometriálneho a ovariálneho karcinómu je znížené pri užívaní vysokodávkovej COC (50 µg etinylestradiolu). Zatiaľ sa nepotvrdilo, či sa to týka aj nízkodávkovej COC.
·
Ostatné stavyGestagénová zložka lieku Baradly je antagonistom aldosterónu s vlastnosťami šetriacimi draslík. Vo väčšine prípadov sa nepredpokladá zvýšenie hladín draslíka. V klinickej štúdii sa však mierne, ale nevýznamne zvýšili hladiny draslíka v sére u niektorých pacientok s miernym alebo stredne závažným poškodením obličiek, ktoré počas užívania drospirenónu užívali súbežne lieky šetriace draslík. U pacientok s obličkovou nedostatočnosťou a hodnotami sérového draslíka pred liečbou blížiacimi sa k hornej hranici referenčného rozpätia, a najmä pri súbežnom užívaní liekov šetriacich draslík sa preto počas prvého liečebného cyklu odporúča sledovať sérové hodnoty draslíka. Pozri tiež časť 4.5.
U žien s hypertriglyceridémiou alebo u žien, ktoré majú toto ochorenie v rodinnej anamnéze, sa v priebehu užívania COC môže zvýšiť riziko pankreatitídy.
Aj keď sa u mnohých žien užívajúcich COC zaznamenalo malé zvýšenie krvného tlaku, klinicky významný vzostup je zriedkavý. Okamžité vysadenie COC je iba v týchto zriedkavých prípadoch. Ak sa COC užíva v prípade existujúcej hypertenzie a konštantne zvýšené hodnoty krvného tlaku alebo signifikantne zvýšený krvný tlak neodpovedajú adekvátne v priebehu užívania COC na antihypertenznú liečbu, COC sa musí vysadiť. Ak sa uzná za vhodné, užívanie COC je možné obnoviť po dosiahnutí normálnych hodnôt krvného tlaku antihypertenznou liečbou.
V súvislosti s graviditou a užívaním COC sa hlásil výskyt alebo zhoršenie nasledujúcich stavov, ale potvrdenie súvislosti s užívaním COC je nepreukázané: žltačka a/alebo svrbenie súvisiace s cholestázou, žlčové kamene, porfýria, systémový lupus erythematosus, hemolyticko-uremický syndróm, Sydenhamova chorea, herpes gestationis, strata sluchu spôsobená otosklerózou.
U žien s hereditárnym angioedémom môžu exogénne estrogény vyvolať alebo zhoršiť jeho symptómy.
Pri akútnych a chronických poruchách pečeňových funkcií može byť nevyhnutné, aby sa užívanie COC prerušilo dovtedy, kým sa markery pečeňových funkcií vrátia na normálne hodnoty. Recidíva cholestatickej žltačky a/alebo svrbenia spojeného s cholestázou, ktoré sa predtým objavili v tehotenstve alebo počas predchádzajúceho užívania pohlavných steroidov, si vyžadujú prerušenie užívania COC.
Napriek tomu, že COC môže mať vplyv na periférnu rezistenciu na inzulín a na glukózovú toleranciu, neexistuje dôkaz o tom, že by bolo potrebné meniť terapeutický režim u diabetičiek užívajúcich nízkodávkovú COC (s obsahom etinylestradiolu < 0,05 mg). Diabetičky užívajúce COC musia však byť starostlivo sledované, najmä na začiatku užívania COC.
Počas užívania COC sa hlásilo zhoršenie endogénnej depresie, epilepsie, Crohnovej choroby a ulceróznej kolitídy.
Niekedy sa môže objaviť chloazma a to najmä u žien, ktoré majú v anamnéze chloasmu gravidarum. Ženy so sklonom ku chloazme sa majú počas užívania COC vyhýbať expozícii slnečnému alebo ultrafialovému žiareniu.
Každá tableta tohto lieku obsahuje 62 mg laktózy. U pacientok so zriedkavými dedičnými problémami galaktózovej intolerancie, lapónskeho deficitu laktázy alebo glukózo-galaktózovej malabsorpcie, ktoré majú diétu bez obsahu laktózy, sa musí vziať do úvahy množstvo laktózy.
Lekárske vyšetrenia/konzultáciePred začatím používania alebo opätovným nasadením lieku Baradly sa má vyšetriť kompletná zdravotná anamnéza (vrátane rodinnej anamnézy) a musí sa vylúčiť gravidita. Má sa zmerať krvný tlak a vykonať zdravotná prehliadka na základe kontraindikácií (pozri časť 4.3) a upozornení (pozri časť 4.4). Je dôležité ženu upozorniť na informácie o venóznej a arteriálnej trombóze vrátane rizika používania lieku Baradly v porovnaní s inými kombinovanými hormonálnymi kontraceptívami, o príznakoch VTE a ATE, o známych rizikových faktoroch a o tom, čo robiť v prípade podozrenia na trombózu.
Žena má byť poučená, aby si pozorne prečítala písomnú informáciu pre používateľku a dodržiavala odporúčania uvedené v nej.
Frekvencia a druh vyšetrení sa majú robiť na základe stanovených postupov a majú sa prispôsobiť individuálnym potrebám ženy.
Ženy majú byť upozornené, že hormonálna antikoncepcia nechráni pred infekciami vírusom HIV (AIDS) ani inými ochoreniami prenášanými pohlavným stykom.
Zníženie účinnostiÚčinnosť COC sa môže znížiť napríklad v prípade vynechania tabliet (pozri časť 4.2), gastrointestinálnych ťažkostí (pozri časť 4.2) alebo súbežneho užívania ďalších liekov (pozri časť 4.5).
Zníženie kontroly cykluPri užívaní ktorejkoľvek COC sa môže objaviť nepravidelné krvácanie (špinenie alebo medzimenštruačné krvácanie), a to predovšetkým počas prvých mesiacov užívania. Z tohto dôvodu má posúdenie nepravidelného krvácania zmysel až po adaptačnom intervale približne troch cyklov.
Ak nepravidelné krvácanie pokračuje alebo sa objaví po období pravidelných cyklov, majú sa zvážiť nehormonálne príčiny a sú indikované zodpovedajúce diagnostické kroky na vylúčenie malignity alebo gravidity. Môžu zahŕňať kyretáž.
U niektorých žien nemusí dôjsť počas intervalu bez užívania tabliet ku krvácaniu z vysadenia. Ak sa COC užíva podľa pokynov opísaných v časti 4.2, je nepravdepodobné, že je žena gravidná. Ak sa však pred prvým vynechaným krvácaním z vysadenia COC neužívala podľa týchto pokynov alebo ak nedošlo ku krvácaniu z vysadenia dva razy, musí sa pred ďalším užívaním COC vylúčiť gravidita.
4.5 Liekové a iné interakciePoznámka: V záujme zistenia potenciálnych interakcií si treba preštudovať odborné informácie súbežne užívaných liekov.
· Vplyv ďalších liekov na liek Baradly
Interakcie medzi perorálnou antikoncepciou a inými liekmi môžu viesť k medzimenštruačnému krvácaniu a/alebo zlyhaniu antikoncepcie. V literatúre boli opísané nasledovné interakcie.
Metabolizmus pečene
Môžu sa vyskytnúť interakcie pri súbežnej liečbe liečivami indukujúcimi pečeňové enzýmy, ktoré môže viesť k zvýšenému klírensu pohlavných hormónov (napr. fenytoín, barbituráty, primidón, karbamazepín, rifampicín, bosentan a liečivá na liečbu HIV (napr. ritonavir, nevirapin) a prípadne aj oxkarbazepín, topiramát, felbamát, grizeofulvín a rastlinné lieky obsahujúce ľubovník bodkovaný (
Hypericum perforatum)). Maximálna enzýmová indukcia sa zvyčajne prejaví po približne 10 dňoch, ale potom môže pretrvávať minimálne 4 týždne po ukončení liečby.
Interferencia s enterohepatálnou cirkuláciou
Zlyhanie antikoncepcie sa hlásilo aj pri antibiotikách, ako sú penicilíny a tetracyklíny. Mechanizmus tohto účinku sa nevysvetlil.
Manažment liečby
Ženy krátkodobo liečené niektorým liekom z vyššie uvedených skupín liečiv alebo jednotlivými liečivami (lieky indukujúce pečeňové enzýmy) okrem rifampicínu, musia dočasne t.j. v priebehu súbežného podávania lieku a nasledujúcich 7 dní po ukončení podávania, navyše k COC používať bariérovú metódu.
Ženy liečené rifampicínom majú počas podávania rifampicínu a 28 dní po jeho vysadení používať okrem COC aj bariérovú metódu.
Ženám dlhodobo liečeným liečivami indukujúcimi hepatálne enzýmy sa odporúča používať inú spoľahlivú, nehormonálnu metódu antikoncepcie.
Ženy liečené antibiotikami (s výnimkou rifampicínu, pozri vyššie) majú používať bariérovú metódu antikoncepcie počas 7 dní po ukončení liečby.
Ak súbežné podávanie lieku trvá aj po využívaní tabliet z blistrového balenia COC, užívanie z ďalšieho balenia COC sa musí začať bez zvyčajného intervalu bez užívania tabliet.
Hlavné metabolity drospirenónu sa v ľudskej plazme vytvárajú bez účasti systému cytochrómu P450. Inhibítory tohto enzýmového systému preto pravdepodobne nemajú vplyv na metabolizmus drospirenónu.
· Vplyv lieku Baradly na iné lieky
Perorálna antikoncepcia môže ovplyvňovať metabolizmus niektorých iných liečiv. Ich koncentrácie v plazme a tkanivách môže teda buď zvyšovať (napr. cyklosporín) alebo znižovať (napr. lamotrigín).
Na základe inhibičných štúdií
in vitro a interakčných štúdií
in vivo s dobrovoľníčkami užívajúcimi omeprazol, simvastatín a midazolam ako označené substráty, interakcia drospirenónu v dávkach 3 mg s metabolizmom iných liečiv nie je pravdepodobná.
· Iné interakcie
U pacientok, ktoré nemajú obličkovú nedostatočnosť, súbežné užívanie drospirenónu a inhibítorov ACE alebo nesteroidných antiflogistík (NSAID) nepreukázalo signifikantný vplyv na hladinu draslíka v sére. Súbežné užívanie lieku Baradly a antagonistov aldosterónu alebo diuretík šetriacich draslík sa však neskúmalo. V tomto prípade sa má koncentrácia draslíka v sére stanoviť počas prvého liečebného cyklu. Pozri tiež časť 4.4.
· Laboratórne vyšetrenia
Užívanie antikoncepčných steroidov môže ovplyvniť výsledky niektorých laboratórnych testov vrátane biochemických parametrov pečeňových, tyreoidálnych, adrenálnych a obličkových funkcií, plazmatických koncentrácií (transportných) proteínov, napr. globulínu viažuceho kortikosteroidy a lipidových/lipoproteínových frakcií, parametrov metabolizmu sacharidov a parametrov koagulácie a fibrinolýzy. Zmeny však zvyčajne zostávajú v rozmedzí normálnych laboratórnych hodnôt. Drospirenón svojím miernym antimineralokortikoidným pôsobením zapríčiňuje zvýšenie aktivity renínu v plazme a aldosterónu v plazme.
4.6 Fertilita, gravidita a laktáciaGraviditaLiek Baradly nie je indikovaný počas gravidity.
Ak v priebehu užívania lieku Baradly žena otehotnie, antikoncepcia sa má okamžite vysadiť. Rozsiahle epidemiologické štúdie neodhalili zvýšené riziko vrodených chýb u detí narodených ženám, ktoré užívali COC pred otehotnením, ani teratogénny vplyv COC užívanej nedopatrením počas gravidity.
Štúdie na zvieratách preukázali nežiaduce účinky počas gravidity a laktácie (pozri časť 5.3). Nežiaduce účinky v dôsledku hormonálneho účinku týchto liečiv sa na základe výsledkov týchto štúdií na zvieratách nedajú vylúčiť. Celkové skúsenosti s použitím COC počas gravidity však neposkytujú dôkazy o konkrétnom nežiaducom pôsobení na ľudí. '
Dostupné údaje o použití lieku Baradly počas gravidity sú príliš obmedzené na to, aby sa mohli vyvodiť závery týkajúce sa negatívneho pôsobenia lieku Baradly na graviditu, na zdravie plodu alebo novorodenca. V súčasnosti nie sú dostupné žiadne významné epidemiologické údaje.
Pri opätovnom začatí užívania lieku Baradly treba vziať do úvahy zvýšené riziko VTE v období po pôrode. (pozri časti 4.2 a 4.4).
LaktáciaCOC môže ovplyvniť laktáciu, pretože môže znižovať množstvo a meniť zloženie materského mlieka. Z tohto dôvodu sa užívanie COC vo všeobecnosti nemá odporúčať, až kým matka úplne neprestane dieťa dojčiť. V priebehu užívania COC sa do materského mlieka môžu vylučovať malé množstvá antikoncepčných steroidov a/alebo ich metabolitov. Tieto množstvá môžu mať vplyv na dieťa.
4.7 Ovplyvnenie schopnosti viesť vozidlá a obsluhovať strojeNeuskutočnili sa žiadne štúdie o účinkoch na schopnosť viesť vozidlá a obsluhovať stroje. U žien užívajúcich COC sa nepozorovali žiadne vplyvy na schopnosť viesť vozidlo alebo obsluhovať stroje.
4.8 Nežiaduce účinkyZávažné nežiaduce účinky u používateliek COC, pozri časť 4.4.
V priebehu užívania lieku Baradly sa hlásili nasledovné nežiaduce reakcie:
Trieda orgánových systémov
| Frekvencia výskytu nežiaducich reakcií
|
časté
≥ 1/100 až < 1/10
| menej časté
≥ 1/1 000 až < 1/100
| zriedkavé
≥ 1/10 000 až < 1/1 000
|
Poruchy imunitného systému
|
|
| hypersenzitivita
astma
|
Psychické poruchy
| depresívna nálada
|
|
|
Poruchy nervového systému
| bolesť hlavy
|
|
|
Poruchy ucha a labyrintu
|
|
| hypoakúzia
|
Poruchy ciev
| migréna
| hypertenzia
hypotenzia
| venózna tromboembólia (VTE),
arteriálna tromboembólia (ATE)
|
Poruchy gastrointestinálneho traktu
| nauzea
| vracanie
hnačka
|
|
Poruchy kože a podkožného tkaniva
|
| akné
ekzém
pruritus
alopécia
| nodózny erytém,
multiformný erytém
|
Poruchy reprodukčného systému a prsníkov
| menštruačné poruchy,
medzimenštruačné
krvácanie,
bolesť prsníkov,
citlivosť prsníkov,
leukorea,
vaginálna kandidóza
| zväčšenie prsníkov,
zmeny libida,
vaginitída
| sekrécia z prsníkov
|
Celkové poruchy a reakcie v mieste podania
|
| zadržiavanie tekutín,
zmeny telesnej
hmotnosti
|
|
Popis vybraných nežiaducich reakcií U žien používajúcich kombinovanú hormonálnu antikoncepciu sa pozorovalo zvýšené riziko vzniku arteriálnych a venóznych trombotických a tromboembolických udalostí vrátane infarktu myokardu, cievnej mozgovej príhody, prechodných ischemických záchvatov, venóznej trombózy a pľúcnej embólie, ktoré sú podrobnejšie uvedené v časti 4.4.
Nasledovné závažné nežiaduce udalosti, ktoré sa hlásili u žien užívajúcich COC, sú analyzované v časti 4.4 Osobitné upozornenia a opatrenia pri používaní:
• hypertenzia
• nádory pečene
• výskyt alebo zhoršenie stavov, pri ktorých súvislosť s užívaním COC nie je presvedčivá: Crohnova choroba, ulcerózna kolitída, epilepsia, maternicové myómy, porfýria, systémový lupus erythematosus, herpes gestationis, Sydenhamova chorea, hemolyticko-uremický syndróm, cholestatická žltačka
• chloazma
• akútne alebo chronické poruchy funkcie pečene si môžu vyžadovať prerušenie užívania COC, až kým
sa markery funkcie pečene nevrátia do normálu.
• u žien s hereditárnym angioedémom môže podávanie exogénnych estrogénov vyvolať alebo zhoršiť
jeho symptómy.
U žien, ktoré užívajú perorálnu antikoncepciu je veľmi mierne zvýšená frekvencia diagnózy rakoviny prsníka. Pretože výskyt rakoviny prsníka je u žien do 40 rokov zriedkavý, zvýšený počet diagnostikovanej rakoviny prsníka je v pomere k celkovému riziku rakoviny prsníka malý. Kauzalita vzhľadom na užívanie COC nie je známa. Ďalšie informácie sa uvádzajú v častiach 4.3 a 4.4.
Hlásenie podozrení na nežiaduce reakcieHlásenie podozrení na nežiaduce reakcie po registrácii lieku je dôležité. Umožňuje priebežné monitorovanie pomeru prínosu a rizika lieku. Od zdravotníckych pracovníkov sa vyžaduje, aby hlásili akékoľvek podozrenia na nežiaduce reakcie prostredníctvom národného systému hlásenia uvedeného v
Prílohe V.
4.9 PredávkovanieS predávkovaním lieku Baradly ešte nie sú skúsenosti. Na základe celkových skúseností s kombinovanou perorálnou antikoncepciou by sa mohli v prípade predávkovania vyskytnúť tieto príznaky: nauzea, vracanie a u mladých dievčat slabé vaginálne krvácanie. Antidotá neexistujú a ďalšia liečba má byť symptomatická.
5. FARMAKOLOGICKÉ VLASTNOSTI5.1 Farmakodynamické vlastnostiFarmakoterapeutická skupina: Hormonálne kontraceptíva na systémové použitie; Gestagény a estrogény, fixné kombinácie, ATC kód: G03AA12
Pearlov index zlyhania antikoncepčnej metódy: 0,09 (95% obojstranný interval spoľahlivosti, horná medza: 0,32).
Celkový Pearlov index (zlyhanie antikoncepčnej metódy + zlyhanie pacientky): 0,57 (95% obojstranný interval spoľahlivosti, horná medza: 0,90).
Antikoncepčný účinok lieku Baradly je založený na spolupôsobení rôznych faktorov. Najdôležitejšie z nich sú inhibícia ovulácie a zmeny endometria.
Liek Baradly je kombinovaná perorálna antikoncepcia obsahujúca etinylestradiol a gestagén drospirenón. V terapeutickom dávkovaní má drospirenón tiež antiandrogénne a mierne antimineralokortikoidné vlastnosti. Nemá estrogénny, glukokortikoidný ani antiglukokortikoidný účinok. Na základe toho je farmakologický profil drospirenónu veľmi podobný prirodzenému hormónu progesterónu.
Z klinických štúdií vyplýva, že mierne antimineralokortikoidné vlastnosti lieku Baradly vedú k miernemu antimineralokortikoidnému účinku.
5.2 Farmakokinetické vlastnostiDrospirenónAbsorpciaDrospirenón sa po perorálnom podaní rýchlo a takmer úplne absorbuje. Maximálne koncentrácie liečiva v sére okolo 38 ng/ml sa dosiahnu asi za 1 ‑ 2 hodiny po jednorazovom užití. Biologická dostupnosť drospirenónu je od 76 do 85 %. Súbežný príjem potravy nemá na biologickú dostupnosť drospirenónu žiadny vplyv.
DistribúciaPo perorálnom podaní sérové hladiny drospirenónu klesajú s terminálnym polčasom 31 hod.
Drospirenón sa viaže na sérový albumín a neviaže sa na globulín viažuci pohlavné hormóny (sex hormone binding globulin, SHBG) ani na globulín viažuci kortikoidy (corticoid binding globulin, CBG). Len 3 ‑ 5 % z celkovej sérovej koncentrácie liečiva je vo forme voľného steroidu. Zvýšenie SHBG indukované etinylestradiolom neovplyvňuje väzbu drospirenónu na sérové proteíny. Priemerný zdanlivý distribučný objem drospirenónu je 3,7 ± 1,2 l/kg.
BiotransformáciaDrospirenón sa po perorálnom podaní metabolizuje v rozsiahlej miere. Hlavnými metabolitmi v plazme sú kyslá forma drospirenónu, ktorá vzniká otvorením laktónového kruhu a 4,5-dihydrodrospirenón-3-sulfát. Obidva metabolity vznikajú bez účasti systému P450. Drospirenón je v malom rozsahu metabolizovaný cytochrómom P450 3A4 a
in vitro prejavil schopnosť inhibovať tento enzým a cytochróm P450 1A1, cytochróm P450 2C9 a cytochróm P450 2C19.
ElimináciaMetabolický klírens drospirenónu v sére je 1,5 ± 0,2 ml/min/kg. Drospirenón sa vylučuje v nezmenenej forme len v stopových množstvách. Metabolity drospirenónu sa vylučujú stolicou a močom s vylučovacím koeficientom približne 1,2 až 1,4. Polčas vylúčenia metabolitov močom a stolicou je asi 40 hod.
Rovnovážny stavV priebehu liečebného cyklu sa maximálna rovnovážna koncentrácia drospirenónu v sére asi 70 ng/ml dosiahne po približne 8 dňoch liečby. V dôsledku pomeru terminálneho polčasu a dávkovacieho intervalu sa hladiny drospirenónu v sére zvýšli približne trojnásobne.
Osobitné skupiny pacientokVplyv poruchy funkcie obličiekU žien s miernym poškodením obličiek (klírens kreatinínu CL
cr 50 ‑ 80 ml/min) boli sérové koncentrácie drospirenónu v rovnovážnom stave porovnateľné s koncentráciami u žien s normálnou funkciou obličiek. Koncentrácie drospirenónu v sére boli v priemere o 37 % vyššie u žien so stredne závažným poškodením obličiek (CL
cr 30 ‑ 50 ml/min) v porovnaní s hladinami u žien s normálnou funkciou obličiek. Liečba drospirenónom bola dobre tolerovaná u žien s miernym a stredne závažným poškodením obličiek. Liečba drospirenónom nepreukázala žiadny klinicky významný vplyv na koncentráciu draslíka v sére.
Vplyv poruchy funkcie pečeneU dobrovoľníčok so stredne závažným poškodením pečene bol v štúdii s jednorazovou dávkou pozorovaný približne 50 % pokles v perorálnom klírense (CL/F) v porovnaní s dobrovoľníčkami s normálnou funkciou pečene. Pozorované zníženie klírensu drospirenónu u dobrovoľníčok so stredne závažným poškodením pečene nevyústilo do žiadnych zjavných rozdielov koncentrácií sérového draslíka. Zvýšenie koncentrácií sérového draslíka nad hornú hranicu referenčného rozpätia nebolo pozorované dokonca ani u diabetičiek a pri súbežnej liečbe spironolaktónom (dva predispozičné faktory hyperkaliémie). To vedie k záveru, že drospirenón je u pacientok s miernym alebo stredne závažným poškodením pečene (trieda B Childovho-Pughovho skóre) dobre tolerovaný.
Etnické skupinyNeboli pozorované klinicky významné rozdiely vo farmakokinetike drospirenónu alebo etinylestradiolu medzi Japonkami a ženami bielej rasy.
EtinylestradiolAbsorpciaEtinylestradiol sa po užití absorbuje rýchlo a úplne. Maximálne plazmatické koncentrácie, približne 100 pg/ml, sa dosiahnu za 1 ‑ 2 hodiny po podaní 30 µg. Etinylestradiol vo veľkom rozsahu podlieha first-pass efektu, čo vyvoláva veľké interindividuálne rozdiely. Absolútna biologická dostupnosť je približne 45 %.
DistribúciaZdanlivý distribučný objem etinylestradiolu je približne 5 l/kg a väzba na plazmatické bielkoviny približne 98 %. Etinylestradiol indukuje hepatálnu syntézu SHBG a CBG (globulínu viažuceho kortikoidy). Počas liečby s 30 µg etinylestradiolu sa plazmatická koncentrácia SHBG zvýšila zo 70 na približne 350 nmol/l.
Etinylestradiol prechádza v malých množstvách do materského mlieka (0,02 % dávky).
BiotransformáciaEtinylestradiol sa úplne metabolizuje (metabolický klírens z plazmy je 5 ml/min/kg).
ElimináciaEtinylestradiol sa v nezmenenej forme nevylučuje vo významnom množstve. Metabolity etinylestradiolu sa vylučujú močom a žlčou v pomere 4:6. Polčas vylučovania metabolitov je asi 1 deň. Polčas eliminácie je 20 hodín.
Rovnovážny stavRovnovážny stav sa dosiahne v druhej polovici liečebného cyklu a sérové hladiny etinylestradiolu sa zvýšia 1,4 až 2,1-násobne.
5.3 Predklinické údaje o bezpečnostiU laboratórnych zvierat sa účinky drospirenónu a etinylestradiolu obmedzili na tie, ktoré sa spájajú so známym farmakologickým pôsobením. Najmä štúdie reprodukčnej toxicity preukázali u zvierat embryotoxické a fetotoxické účinky, ktoré sú považované za druhovo špecifické. Pri expozíciách drospirenónu prekračujúcich tie, ktoré sú prítomné u žien užívajúcich Baradly sa pozorovali účinky na pohlavnú diferenciáciu u plodov potkanov, ale nie u opíc.
6. FARMACEUTICKÉ INFORMÁCIE6.1 Zoznam pomocných látokJadro tablety: monohydrát laktózy
kukuričný škrob
predželatínovaný škrob (kukuričný)
krospovidón typ B
povidón K-30 (E 1201)
polysorbát 80 (E 433)
magnéziumstearát (E 470b)
Filmový obal tablety: polyvinylalkoholoxid titaničitý (E 171)
makrogol 3350
mastenec (E 553b)
žltý oxid železitý (E 172)
6.2 InkompatibilityNeaplikovateľné.
6.3 Čas použiteľnosti3 roky.
6.4 Špeciálne upozornenia na uchovávanieUchovávajte pri teplote do 30 °C.
6.5 Druh obalu a obsah baleniaPriehľadný až mierne nepriehľadný, transparentný PVC/PVDC/Alu blister.
Veľkosti balenia:
1 x 21 filmom obalených tabliet
2 x 21 filmom obalených tabliet
3 x 21 filmom obalených tabliet
6 x 21 filmom obalených tabliet
13 x 21 filmom obalených tabliet
Na trh nemusia byť uvedené všetky veľkosti balenia.
6.6 Špeciálne opatrenia na likvidáciu a iné zaobchádzanie s liekomNepoužitý liek alebo odpad vzniknutý z lieku treba vrátiť do lekárne.
7. DRŽITEĽ ROZHODNUTIA O REGISTRÁCIILaboratorios Liconsa, S.A.
Gran Vía Carlos III, 98, 7th floor
08028 – Barcelona
Španielsko
8. REGISTRAČNÉ ČÍSLO Reg. č.: 17/0201/15-S
9. DÁTUM PRVEJ REGISTRÁCIE/PREDĹŽENIA REGISTRÁCIEDátum prvej registrácie:
10. DÁTUM REVÍZIE TEXTUSeptember 2015